m+n 3 или 4. Процесс протекает при температуре 20-250°С (преимущественно 70- 170°С) и давлении СО 7,5-100,0 МПа (преимущественно 30,0-70,0 МПа). Выход 5-циклооктенкарбоновой кислоты составляет 48,0-51,0% 2.
Указанные способы характеризуются невысокими выходами целевых продуктов.
Наиболее близким по технической сущности и достигаемым результатам является спо сбб получения кислоты I гидрокарбок- силированием циклооктадиена-1,5 в присутствии смешанного катализатора, состоящего из Pd-содержащего комплекса состава Р(СбН5) PdClz и хлорида алюминия AICI3.
Процесс синтеза протекает при 105-108°С и давлении СО 13,6 МПа в течение 2 ч. Концентрация Н20 1 моль/моль углеводорода, Pd металлического в жидкой фазе 0,2 моль, соотношение AI:Pd 10,5 моль/моль. Выход 5-циклооктенкар- кислоты составляет 88,0% на исходы .и углеводород 3 (прототип).
Кислота II по аналогии с кислотой I может быть получена гидрокарбоксилировани- ем соответствующего циклодиолефина - 3,7-диметилциклооктадиена-1,5. Последний синтезируется в промышленных условиях каталитической циклодимеризацией пипе- рилена, который является побочным продуктом крупнотоннажного производства изопрена, а также может быть выделен из С5-фракции продуктов пиролиза бензина. Авторы установили, что выход кислоты II, полученной по способам , практически не отличаются от выходов кислоты I в аналогичных условиях синтеза.
Недостатком способа-прототипа 3 является относительно небольшой выход целевых кислот, затрудняющий внедрение способа в промышленности.
Кроме того, недостатками всех описанных способов, в том числе и прототипа, являются сложность синтеза исходных катализаторов, а также невозможность избежать потерь при их регенерации, что усугубляется дефицитностью и высокой стоимостью применяемого в составе катализаторов Pd. Наличие в катализаторах галоидов вызывает значительную коррозию аппаратуры, вследствие чего ее необходимо изготавливать из таких дорогостоящих, стойких к коррозии сплавов, как хастеллой.
Цель изобретения - увеличение выхода циклооктенкарбоновых кислот.
Для получения указанных кислот методом гидрокарбоксилирования применение в качестве катализаторов карбонилов кобальта, возможно модифицированных третичными аминами (предпочтительно пиридином), наиболее целесообразно. Преимущества указанного катализатора заключаются в том, что Со является более
доступным металлом, чем Pd, синтез Со-ка- тализатора и его регенерация освоены в промышленности, происходят с минимальными потерями и процесс менее коррозион- но-активен,
Найдено, что при гидрокарбоксилиро- вании циклооктадиена-1,5 и 3,7-диметил- циклооктадиена-1,5 не происходит в значительной степени перемещение двойных связей, ведущее к образованию системы сопряженных двойных связей. Поэтому закономерности присоединения СООН- группы к двойным связям указанных диенов должны быть такими же, как и для монооле- финов. Отсюда вытекает, что для гидрокарбоксилирования указанных циклодленов в непредельные кислоты I и II могут быть использованы способы гидрокарбоксилирования о/ ефинов в монокарбоновые кислоты. Описан ряд способов гидрокарбоксилирования олефинов в монокарбоновые кислоты в присутствии карбонилов кобальта, модифицированных пиридином. Так, известен способ получения высших монокарбо- новых кислот гидрокарбоксилированием
олефинов Сю и выше в присутствии каталитической системы диоктакарбонил кобальта (ДОК)+пиридин при постоянной температуре в интервале 120-180°С и дае- лении СО 7,0-25,0 МПа. Соотношение
Н20:олефин 1-6 моль/моль, Со:олефин 0,001-0,2 моль/моль, пиридин.Со 1- 10 моль/моль. Время реакции составляет 0,25-3,0 ч, выход СЖК при 100%-ной конверсии олефина 61,4-72,8% на исходный
олефин 4. Однако, как показывают приведенные выше данные по выходу целевого продукта, замена палладиевого катализатора на ДОК, модифицированный пиридином, решая некоторые технологические и аппаратурные проблемы, не позволяет получить целевой продукт с высоким выходом.
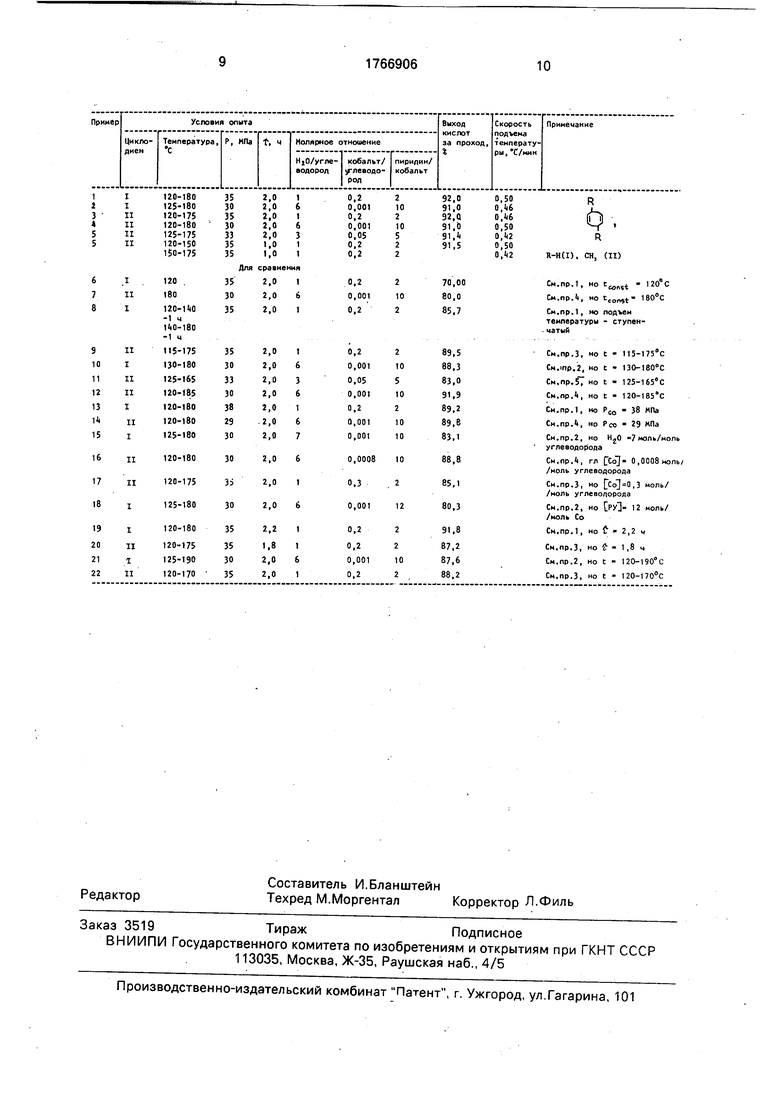
Цель достигается проведением процесса гидрокарбоксилирования циклооктадиена-1,5 или 3,7-диметилциклооктадиена-1,5 до 5-циклооктенкарбоновой или 3 7-диме- тил-5-циклооктенкарбоновой кислоты также в присутствии ДОК с добавкой пиридина, но не при постоянной температуре а в переменном температурном режиме с постепенным повышением температуры от 120-125 до 175-180°С при скорости подъема от 0,42 до 0,50°С/мин. ВыходЧ.елевых кислот составляет 91-92% на исходное сырье.
Отличие предлагаемого способа от способа-прототипа заключается в том, что процесс проводят не при постоянной, а при переменной, постепенно повышающейся в течение опыта температуре от 120-125 до 175-180°С со скоростью подъема от 0,42 до 0,50°С/мин и в присутствии в качестве катализатора вместо Pd-содержащего комплекса в смеси с галогенидом металла кобальтпиридинового соединения в виде карбонилов кобальта, модифицированных пиридином. Процесс ведут при молярном соотношении Н20:П (1:6):1; кобальт:П (0,001-0,2):1; пиридин:кобальт (2-10):1.
Преимуществом предлагаемого способа по сравнению со способом-прототипом является увеличение выхода целевых продуктов с 88,0 до 91,0-92,0%. Дополнительные преимущества заключаются в возможности использования менее дорогостоящего катализатора и типовой аппаратуры высокого давления.
Установлено, что проведение процесса с изменением режима нагрева реагентов, .а именно при постоянной температуре 120 и 180°С, при ступенчатом подъеме температуры в интерзале от 120 до 180°С со скоростью подъема вне предлагаемых пределов, при равномерном подъеме температуры от
Тнач 120 ДО 175°С, ОТТнач 125 ДО 180°Си
от начальной температуры 120-125° до Хкон 175°С уменьшает выходы целевых кислот. Равномерный нагрев от -120 до 185°С не влияет на показатели процесса, увеличение Ткон до 190°С приводит к снижению выхода целевых продуктов.
Изменение давления СО 35,0 МПа и 30,0 МПа вызывает уменьшение выхода целевых кислот.
Увеличение соотношения Н20:углево- дород 6 моль/моль приводит к снижению выхода целевых кислот.
Изменение соотношения Со:углеводо- род 0,001 моль/моль и 0,2 моль/моль вызывает уменьшение выхода целевых кислот.
Увеличение соотношения пири- дин:Со 10 моль/моль приводит к снижению выхода целевых кислот.
Увеличение времени реакции 2 ч не влияет на выход целевых продуктов, однако экономически нецелесообразно. Уменьшение времени реакции 2ч вызывает снижение выхода кислот.
Следующие примеры иллюстрируют предлагаемый способ.
П р и м е р 1. В реактор, снабженный перемешивающим устройством, помещают 122 мл (108 г) циклооктадиена-1,5, 18 мл НаО, 34,5 г Со2(СО)з и 32 мл пиридина. Соотношение НаО:углеводород 1 моль/моль. кобальт:углеводород 0,2 моль/моль, пири- дин:кобальт 2 моль/моль. Реактор продувают СО и под давлением СО 10 МПа
нагревают до 120°С. Затем поднимают давление СО до 35,0 МПа и включают мешалку. Реакцию проводят при переменной температуре 120-180°С с равномерным ее подъемом в течение 2 ч.
0
После окончания реакции охлаждают реактор и стравливают СО. Продукты реакции разделяют на две фазы - водную и углеводородную. Последнюю анализируют на
5 содержание 5-циклооктенкарбоновой кислоты методом ГЖХ. Количество указанной кислоты составляет 141,7 г, что соответствует выходу 92,0% в расчете на исходный углеводород.
0П р и м е р 2. Проводят в условиях
примера 1, но в интервале температур 125- 180°С, Рсо 30,0 МПа, время реакции 2 ч, соотношение НаО: циклодиен 6 моль/моль: Со:циклодиен
5 0,001 моль/моль, пиридин:Со - 1 О моль/моль.
Выход 5-циклооктенкарбоновой кислоты составляет 91 %.
П р и м е р 3. Проводят в УСЛОВИЯХ
0 примера 1, но в качестве исходного сырья используют 3,7-диметилциклооктадиен-1,5. Интервал температур 120-175°С. РСО 35,0 МПа, концентрация НаО 1 моль/моль углеводорода Со 5 0.02 моль/моль углеводорода, пиридина- 2 моль/моль кобальта. Выход 3.7-диметил- 5-циклооктенкарбоновой кислоты составляет 92%.
П р и м е р 4. Проводят в условиях
0 примера 3, но в интервале температур 120- 180°С, при Рсо 30,0 МПа. Концентрация НаО 6 моль/моль циклодиена, Со - 0,001 моль/моль циклодиена, пиридина - 10 моль/моль Со. Выход 3,7-диметил-5-цик5 лооктенкарбоновой кислоты составляет 91,0%.
П р и м е р 5. Проводят в условиях примера 3, но в интервале температур 125- 175°С при Рсо 33,0 МПа. Концентрация
0 НаО 3 3 моль/моль углеводорода, Со - 0,05 моль/моль углеводорода, пиридина - 5 моль/моль кобальта. Выход 3,7-диметил- 5-циклооктенкарбоновой кислоты составляет 91,4%.
5П р и м е р 5. Проводят аналогично
примеру 3, но подъем температуры ступенчатый: 120-150°С 1 ч. 150-175°С 1 ч Скорости подъема температуры соответственно 0,50°С/мин и 042°С/мин. Выход целевой кислоты 91,5%.
П р и м е ры 5-22 для сравнения.
Примерб. Проводят гидрокарбокси- лирование циклооктадиена-1,5 в условиях примера 1, но tconst 120°С.
Пример. Проводят гидрокарбокси- лирование 3,7-диметилциклооктадиена-1,5 в условиях примера 4, но tconst 180°C.
Примере. Проводят аналогично примеру 1, но подъем температуры ступенчатый: 120-140°С 1 ч, 140-180°С 1 ч.
П р и м е р 9. Проводят аналогично примеру 3, но подъем температуры в интервале 115-175°С.
П р и м е р 10. Проводят аналогично примеру 2, но подъем температуры в интер- вале 130-180°С.
П р и м е р 11. Проводят аналогично примеру 5, но подъем температуры в интервале 125-165°С.
П р и м е р 12. Проводят аналогично примеру 4, но подъем температуры в интервале 120-185°С.
Пример 13. Проводят аналогично примеру 1, но Рсо 38 МПа.
П р и м е р 14. Проводят аналогично примеру 4, но Рсо 29 МПа.
П р и м е р 15. Проводят аналогично примеру 3, но соотношение Н20:углеводо- род 7 моль/моль.
П р и м е р 16. Проводят аналогично примеру 4, но соотношение Со:углеводород 0,0008 моль/моль.
П р и м е р 17. Проводят аналогично примеру 3, но соотношение Со:углеводород 0,3 моль/моль.
П р и м е р 18. Проводят аналогично примеру 2, но соотношение Со:пиридин 12 моль/моль
П р и м е р 19. Проводят аналогично примеру 1, но время реакции 2,2 ч.
П р и м е р 20. Проводят аналогично примеру 3, но время реакции 1,8 ч.
П р и м е р 21. Проводят в условиях примера 2, но в пределах температур 125- 190°С. Выход целевого продукта 87,6%.
П р и м е р 22. Проводят в условиях примера 3, но в пределах температур 120- 170°С. Выход целевого продукта 88,2.
Полученные результаты приведены в таблице.
Формула изобретения
Способ получения циклооктенкарбоно- вой кислоты общей формулы
R
НООС
$.
где R-H, СНз; гидрокарбоксилированием циклооктадиена общей формулы
R (ы)
где R имеет указанные значения, при повышенных температуре и давлении в присутствии катализатора, отличающийся тем, что, с целью повышения выхода, процесс проводят при 30-35 МПа и равномерно повышающейся температуре в интервале от 120-125°С до 175-180°С со скоростью подъема 0,42-0,50 град/мин, в качестве кгтализа- тора используют диоктакарбонил кобальта, модифицированный пиридином, процесс ведут при молярном соотношении НгО:угле- водород; 1-6:1; кобальт:углеводород 0,001- 0,2:1; пиридинжобальт 2-10:1.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения циклооктенкарбоновой кислоты | 1990 |
|
SU1766907A1 |
| Способ получения @ -оксиэтиловых эфиров циклогексенкарбоновых кислот | 1989 |
|
SU1680687A1 |
| Способ получения монокарбоновых кислот С @ - С @ | 1990 |
|
SU1768576A1 |
| Способ получения олигомеров этилена | 1983 |
|
SU1154258A1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-ПЕНТЕНОВОЙ КИСЛОТЫ | 1966 |
|
SU185900A1 |
| Способ выделения алифатических спиртов С @ из побочных продуктов гидроформилирования пропилена | 1989 |
|
SU1684272A1 |
| Этиленгликолевые эфиры алкиларилциклогексанкарбоновых кислот в качестве пластификаторов поливинилхлорида | 1981 |
|
SU979331A1 |
| Способ получения нафтеновых кислот | 1980 |
|
SU1154266A1 |
| Способ совместного получения метиловых эфиров высших карбоновых кислот и внутренних олефинов С @ -С @ | 1989 |
|
SU1694570A1 |
| Способ приготовления металлокомплексного катализатора для олигомеризации моно-и диолефинов | 1977 |
|
SU695696A1 |


Авторы
Даты
1992-10-07—Публикация
1990-07-31—Подача