Изобретение относится к получению фосфорорганических соединений, которые могут быть интересны как инсектициды, пластификаторы, полупродукты для синтеза других соединений.
Предложен способ получения О-имин-О(S)-β-хлорэтилхлорфосфатов, заключающийся в том, что гликольхлорфосфиты или монотноэтиленгликольхлорфосфит подвергают взаимодействию с α-хлорнитрозоалканами. Процесс проводят в среде инертного растворителя при температуре 0-20°С.
Пример 1. О-Фторхлорформимин-О-β-хлорэтилхлорфосфат. 5,6 г (0,044 моль) этиленгликольхлорфосфита растворяют в 30 мл сухого серного эфира и в полученный раствор при 0-10°С в течение 1 час пропускают фтордихлорнитрозометан до прекращения обесцвечивания реакционной массы (5,4 г, 0,041 моль), затем смесь выдерживают сутки при комнатной температуре и перегоняют. Выделяют 5,7 г (54%) О-фторхлорформимин-О-β-хлорэтилхлорфосфата; т. кип. 73-75°С (10-2 мм рт. ст.);
 1,598;
1,598; 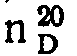 1,4600; MRD найдено 44,20;
1,4600; MRD найдено 44,20;
вычислено 44,58.
Найдено, %: С 14,70; 15,20; Н 1,78; 1,86; F 8,20; 8,35; Cl 39,97; 40,05; N 5,66; 5,63; Р 13,42; 13,50.
C3H4FCl3NO3P.
Вычислено, %: С 13,92; Н 1,55; F 7,35; Cl 41,2; N 5,41; Р 12,0.
ИК-спектр: νшкс, см-1 1250 с (Р=0); 1660 с. (N=C).
Пример 2. О-Фторхлорформимин-О-β-хлор-(α,β-диметил-)-этилхлорфосфат. 4,7 г (0,036 моль) дихлорфторнитрозометана пропускают в смесь 5,5 г (0,036 моль) 2,3-бутиленгликольхлорфосфита и 20 мл сухого серного эфира. Реакцию проводят в токе азота при перемешивании и температуре 5-20°С. Перегонкой выделяют 8,5 г (84%) О-фторхлор-формимин-О-β-хлор-(α,β-диметил) - этилхлорфосфата; т. кип.84-85°С (0,3 мм рт. ст.);  1,4811;
1,4811;  1,4552; MRD найдено 52,50; вычислено 53,42.
1,4552; MRD найдено 52,50; вычислено 53,42.
Найдено, %: F 6,68; 6,79; Cl 36,61; 36,44; N 5,00; 4,94; Р 10,79; 11,03.
C5H8FCl2NOP.
Вычислено, %: F 6,64; Cl 37,18; N 4,88; Р 10,81.
Пример 3. О-Фторхлорформимин-S-β-хлорэтилхлорфосфат. 5,3 г (0,04 моль) фтордихлорнитрозометана при 0-10°С в токе азота пропускают в раствор 5,7 г (0,04 моль) монотиоэтиленгликольхлорфосфита в 30 мл сухого серного эфира до прекращения обесцвечивания реакционной массы. После выдержки в течение ночи при перегонке выделяют 9,2 г (84%) О-фторхлорформимин-S-β-хлорэтилхлорфосфата; т. кип. 101-105°С (10-2 мм рт. ст.);  1,6760;
1,6760;  1,5190. MRD найдено 49,7; вычислено 51,78.
1,5190. MRD найдено 49,7; вычислено 51,78.
Найдено, %: F 6,90; 6,95; Cl 38,41; 38,45; Р 11,20; 11,27; S 11,40; 11,50.
C3H4FCl3NO2PS.
Вычислено, %: F 6,92; Cl 38,8; Р 11,30; S 11,60.
Ик-спектр: νмакс, см-1 538 ср. (Р-S), 555 ср. (Р -С1), 590 с. (Р-Cl), 1250 с. (Р=0), 1665 с. (N=C).
1. Способ получения О-имин-О(S)-β-хлорэтилхлорфосфатов, отличающийся тем, что гликольхлорфосфит или монотиоэтиленгликольхлорфосфит подвергают взаимодействию с α-хлорнитрозоалканом в среде инертного растворителя.
2. Способ по п. 1, отличающийся тем, что процесс проводят при охлаждении до 0-10°С.
Авторы
Даты
1968-07-23—Публикация
1967-03-31—Подача