Известен способ получения эф,иров тритио- и тетратиофосфорных кислот общей формулы, где R и R - алкилы, содержащие 1-5 атомов углерода; Y - атом кислорода или серы; М - один или несколько заместителей: галоиды; галоидзамещенные или незамещенные алкилы; нитро-, циано-, алкоксиили тиоалкилыные радикалы; -A-COOR, где А - алкил- или карбоксиалкилзамещенный или незамещенный метиленовый или этиленовый радикал; RI - имеет те же значения, что R R или
o(s) , .U z4II
ОН одинаковые или различные: ; атомы водорода, насыщенные или ненасыщенные органические радикалы с 1-5 атомами углерода, галоидзамещенные или незамещенные фенилы, Ro и Rs могут также образовывать с атомом азота гетероциклический радикал, который может содержать другой гетероатом, нанример кислород: п-1 или 2; Z - О, S, N НЛП Н. дложенному .способу галоидные е RGal, где R - группа -(сн,) т взаимодействию с тетраметилй солью двухзамещенного произофосфорной кислоты формулы
2(СНЛ
н
Процесс -проводят при температуре 50- 100°С в среде органического растворителя, например ацетона, хлороформа.
В том случае, «огда Ri имеет значение
/Ra
(СН2)
получаемые соединения целесообразно превращать в соли действием «а них кислоты или галоидного алкила. Пример 1.
(СНз8),Р-8-СН (COOCaHs),
il
.PV.
24,T.,l молЩ 5,5-диметилтритиофосфата тетраметиламмония растворяют в 100 мл хлороформа; в раствор вводят 23,9 г (0,1 моль) ВгСН(СООС2Н5)2. Сосуд герметически закрывают и нагревают 2 час на водяной бане 1при температуре 80°С.
После охлаждения содержимого колбы отфильтровывают количественно образовавшийся бромистый тетраметиламмоний. Фильтрат промывают 0,1 н. раствором бикарбоната натрия до слабощелочной реакции, а затем - водой до нейтральной реакции. Раствор хлороформа .после этого сущат «ад сульфатом
натрия. Фильтруют, выпаривают в вакууме хлороформ и полученный продукт очищают перегонкой в атмосфере азота.
При этом получают 25 г продукта, т. пл. 148-150°С/0,01 мм рт. ст.; по° 1,5415.
Полученный продукт .представляет собой бесцветную жидкость, растворимую в органических растворителях и нерастворимую в воде; ВЫХО.Д составляет 81% от теории.
Примеры 2-4. Олыты ведут, как описано в примере 1; реакцию проводят между 5,5-диметилтритиофосфатом тетраметиламмония и галоидным лроизводным в среде хлороформа; в табл. 1 приведены получаемые
соединения и их характеристики.
Таблица 1



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ТРИТИОФОСФАТОВ | 1969 |
|
SU245772A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ЦИКЛОГЕКСАНА | 1970 |
|
SU267512A1 |
| Способ получения галоидзамещенных диалкил-1-окси-2,2,2-трихлорэтилфосфонатов | 1977 |
|
SU707921A1 |
| Способ получения производных индолизина или их фармацевтически приемлемых солей | 1987 |
|
SU1528321A3 |
| Способ получения производных гетразепина | 1989 |
|
SU1738089A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ОКСАЗОЛИДИНА | 1971 |
|
SU312420A1 |
| Способ получения производных эритромицина или их солей | 1976 |
|
SU682134A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЧЕТВЕРТИЧНЫХ СОЛЕЙ ТЕНИЛФОСФОНИЯ | 1973 |
|
SU368753A1 |
| Способ получения производных бензодиоксола | 1973 |
|
SU468412A3 |
| 4-ЗАМЕЩЕННЫЕ АНТРАЦИКЛИНОНЫ И ГЛИКОЗИД АНТРАЦИКЛИНА | 1991 |
|
RU2024483C1 |

При м е р 5. СНзЙ)2-Р-5- 5На-е Шв течение 5 час .при температуре 90°С нагревают -омесь 24,7 г (0,1 моль) 5,8-ди1мет-ИчГ1тритиофосфата тетраметиламмония, 23,75 г (0,1 моль) С1-СНг-СО-NH-СбНзСЬ (2,4) и 75 мл хлороформа. После 15 мин «arpeiBaния начинается осаждение хлористого тетраметиламмония. Реакционной смеси дают охладиться и фильтруют для удаления хлоргидрата тетраметиламмония. Фильтрат промывают раство3035 40 ром бикарбоната натрия до слабощелочной реакции, а затем водой; .промывные воды экстрагируют хлороформом. Объединенные хлороформ.ные растворы сущат над сульфатом натрия, фильтруют, растворитель выпаривают при разрел ении, создаваемом водоструйным насосом, а затем 30 мин при 50°С под давлением 0,01 мм рт. ст. При этом получают 30 г вязкого остатка, который кристаллизуют. Выход составляет 80%. Продукт, перекристаллизованный из циклогексана, плавится при температуре 90°С. П р и м е р ы 6 и 7. Олыты ведут, как описано в примере 5, и получают соединения, приведенные в табл. 2.
Пример 8.
(СНзЙ)2-Р- - СНг - С-NH-СНз О,. О
При взаимодействии N-метилхлорацетамида с диметилтетратиофосфатом тетраметиламмония и лри вьшоляении опыта, как описано в примере 5, получают вязкий бесцветный остаток, кристаллизующийся при потираний стенок из смеси четыреххлористого углерода и петролейного эфира.
Продукт, перекристаллизовавный из петролейного эфира, плавится при температуре 38-39°С. Выход составляет 80%.
Таблица 2
Пример 9.
(СНзЙ) -Р -S -СНа -(Zy-Cl
tti О
Проводят реакцию между 11,5 г (0,05 моль) хлористого 2,4,5-трихлорбензила и 13 г (0,0525 моль) S, S-диметилтритиофосфата тетраметиламмония, растворенного в 50 мл хлороформа. Реакцию ведут в течение 4 час при температуре 80°С и заканчивают ее, как описано в примере 5. При этом получают 16 твердого остатка, который после перекристаллизации из петролейного эфира плавится ппи температуре 62°С.
Выход составляет 70%.
Таблица 3 Примеры 10-15. Опыты ведут, .как описано в примере 9; реакцию проводят между гало:ИД1ИЫми производными и тетраметиламмокиовыми солям,и. В табл. 3 приведены полученные соедипения. Пример 16. (СНзЙ)2-Р-; -СН2-СИ2-К-1СгНб)2 О В течение 6 час ири температуре окружающей (ореды пфемешивают смесь 24,7 гis (0,1 моль) S, S-диметилтритиофосфата тетраметиламмония, 14,8 г (0,11 моль) свежеприг-отовлениого ClCH2CH2N(C2Hg)2 и 50 мл
Пример
(СНз;)2-Р-;й-Сн.,-снз-к-(СгН,);
17
(СНзЙ) -СНа-еНг - 0
18
(, -p- i-CHj сыг-к-( )
19
(5Ы2-Ш-Л-(СаН5)2
Соон Ы Н
к раствору 11,5 г 5,5-ди1м етил-3-(2-д1иэт1Иламияоэтил)-тритиофосфата в 25 мл ацетона прибавляют по каплям при перемешиванил раствор 5 г (С4ООН)2 2Н2О в 30 мл ацетона до рН4.
Перемешивание продолжают вести еще 1/4 час, отфильтровывают образовавшуюся соль, промывают ее тремя оорциями безводного аде гона по 25 мл. Продукт сушат в вакууме над Р205. При этом получают 13,4 г
Таблица 4
Выход,
Формула
96
85
73,2
86,6
продукта, плавящегося при те.мпературе 123- 124°С, который после кристаллизации из ацетонитрила плавится при температуре 124°С. Выход составляет 87,5%.
Пример 21. Й1зй),,-СНа- -(С2Н5)2Вг
Сн,
11,5 г 3,5-диметил-5-(2-диэтиламинометил)тритиофосфата в 10 мл ацетона обрабатывают 25 мл 40%-ного (по весу) раствора бромистого метила в ацетоне. Соль начинает осаждаться по прошествии нескольких минут при .компатной температуре. Реакционную смесь выдерживают 3 суток при комнатной температуре, выделяют продукт фильтровахлорофо1рма. Хлористый тетраметиламмо ий удаляют фильтрованием. Хлороформ выпаривают при разрежении, создаваемом водоструйным насосом, а затем 30-минутным нагревапием при 40°С под давлением 0,01 мм рт. ст. Остаток обрабатывают 100 мл безводного эфира для осаждения тетраметиламмониевой соли, растворимой в растворе хлороформа, фильтруют, эфир выпаривают в вакууме и получают 23 г бесцветного остатка. Выход составляет 84,2%. Примеры 17-19. Проводят реакцию между галоидными производными и тетраметиламмониевыми солями; опыты ведут, как описано в примере 16, и получают следующие соединения, приведенные в табл. 4. нием, промывают его ацетоном и сушат в вакууме над PgOs. При этом получают 12,7 г продукта, который после перекристаллизации из смеси 15% изо-СзН7ОН и 85% ацетона цлавится цри тем-5 цературе 112°С. Выход составляет 82%.
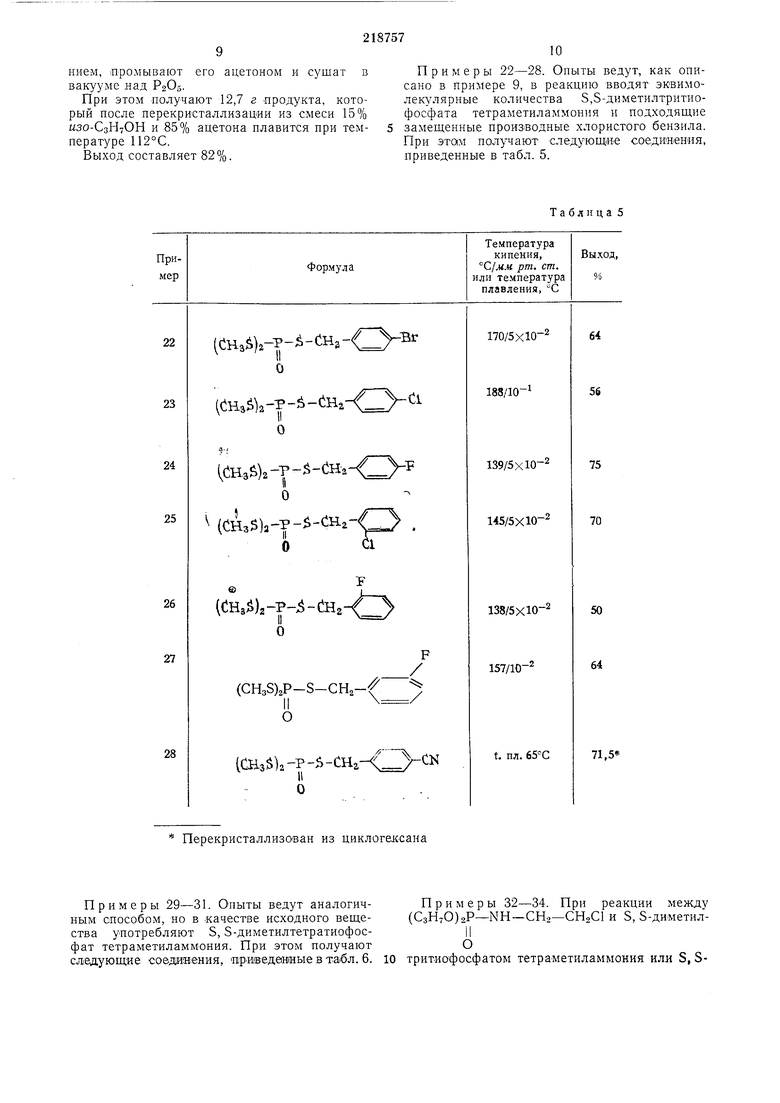
Перекристаллизосан из циклoreJi:caиa Примеры 29-31. Опыты ведут аналогичным способом, но в -качестве исходного вещества употребляют S, S-диметилтетратиофосфат тетраметиламмония. При этом получают
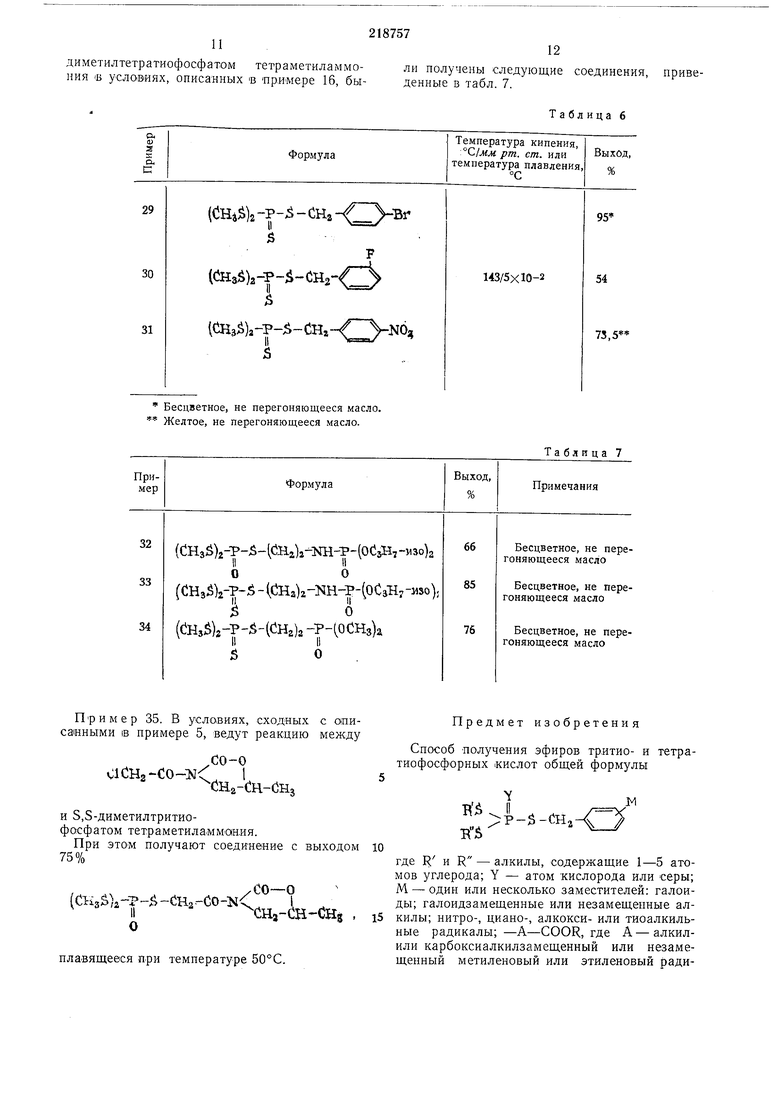
Таблица 5 Примеры 22-28. Опыты ведут, как описано в примере 9, в реакцию вводят эквимолекулярные количества 5,5-диметилтритиофосфата тетраметиламмония и подходящие замещенные производцые хлористого бензила, При этом получают следующие соединения, приведенные в табл. 5. Примеры 32-34. При реакции между (СзН70)2Р-Nn-СП,-СНаС и S, S-диметилОдиметилтетратиофосфатом тетраметиламмония (Б условиях, описанных в примере 16, бы Бесцветное, не перегоняющееся масло. Желтое, не перегоняющееся масло.
Пример 35. В условиях, сходных санными IB примере 5, ведут реакцию
СО-0
аСН2-со-Б 1
ОНа-СН-ОЫз
и 5,5-диметилтритиофосфатом тетраметила.ммаЕия.
При этом получают соединение с в 75%
/СО-О
(CH3S).-|--i te,-CO-X
Таблица 6
Таблица 7
Предмет изобретения
Способ получения эфиров тритио- и тетратиофосфорных (КИСЛОТ общей формулы
B;i
.-р-$-СНаЧ.
где и R - алкилы, содержащие 1-5 атомов углерода; Y - атом кислорода или серы; М - один или несколько заместителей: галоиды; галоидзамещенные или незамещенные алкилы; нитро-, циано-, алкокси- или тиоалкильные радикалы; -А-COOR, где А - алкилили карбоксиалкилзамещенный или незамещенный метиленовый или этиленовый радили получены следующие соединения, приведенные в табл. 7.
кал; Ri - имеет те же значения, что R и R или / 2/Ra -CH -CO-N/ ; -(СН,)У ; II /ORII /OR - (СН,)„ -P ( ; -(СН,)„ - Z- P где Ra и Rs - одинаковые или различные: атомы водорода, насыщенные или ненасыщенные органические радикалы с 1-5 атомами углерода, галоидзамещенные или незамещенные фенилы, или R2 и Rs могут также образовывать с атомом азота гетероциклический радикал, который может содержать другой гетероатом, например, кислород;
n - 1 или 2; Z - 0,S,N «ли H, отличающийся
тем, что соединение
1 Gul-CK2 ; ,/ нодвергают взаимодействию с тетра метиламмониевой солью двухзамещенного производного тиофосфорной кислоты формулы N(te. , -f при температуре 50-100°С в среде органического -растворителя, на пример ацетона.

Авторы
Даты
1968-01-01—Публикация