Изобретение относится к способу получения нового типа эфиров карбамидной кислоты, которые могут найти широкое применение в фармацевтической промышленности. Предлагается способ получения эфиров карбамидной кислоты, заключающийся в том, что производное пиразолбензимидазола общей формулы где Y - обозначает водород или алкильный радикал, А - водород, галоген, нитро-, или низший алкильный или алкоксильный радикалы, В - может быть одинаковым или различным с А, тип - обозначают 1 или 2, подвергают взаимодействию с производным угольной кислоты общей формулы R-0-С-Д арильный радикалы или гетероциклический радикал, Д - галоген, группа -ORi или -OCORa, II О Причем RI или Ra могут быть одинаковыми или различными и иметь указанные для R значения, а R и Д могут быть остаточными составными частями кольцевой системы гликокарбоната или бензкатехинкарбоната с последующим выделением или переэтерификацией целевого продукта известными приемами. Пример 1. В суспензию, состоящую из 39.83 (0,2моль) 2- |Пиразолил-1)-5-ами1Нобензимидазола и 100 см этанола, добавляют в течение 1 час, 40,5 г (0,25 моль) диэтилового эфира пироугольной кислоты. При образовании COg образуется сначала раствор, из которого выпадает позже реакционный продукт. На другой день к нему добавляют 150 с,из петролейного эфира, отсасывают, промывают петролейным эфиром и высушивают. Выход 49.9г соединения формулы C HjO-C-NH-T
Для анализа вторично осаждают колбу из кипящего эфира уксзсной кислоты (легкого бензина) и высушивают при температуре 110°С.
Вычислено, %: С 57,56; Н 4,83; N 25,82; О 11,80.
CiaHisN Oa (мол. вес 271,27).
Найдено, %: С 57,57; Н 5,08; N 25,35; О 12,45.
Пример 2. 53,2 г (0,25 лшль) 1-метил-2 пиразолил-(1)-5-аминобензимидазол растворяют при нагревании в 250 слгз этанола. Охлаждают снова до комнатной температуры и добавляют, размешивая, в течение 30 мин 50,6 г (0,3125 моль) диэтилового эфира пироугольной кислоты. Образуется густая каша, в которую добавляют остальные 50 смз этанола. Реакционную массу доводят до кипения, заканчивают реакцию обменного разложения.
После охлаждения до 0°С, реакционный продукт отсасывают и промывают этанолом при температуре около -20°С. Получают 62,5 г соединения формулы
C-N-Ы
C HsO-C-NH-r
-/ и
СНз
ст. пл. 164,5-165,5°С.
После перекристаллизации из этанола т. пл. 167--168С.
Вычислено, %: С 58,93; Н 5,30; N 24,55; О 11,22.
CiiHisNgOa (мол. вес 258,30).
Найдено, %: С 58,8; Н 5,3; N 24,7; О 11,2.
Пример 3. В смесь из 19,9 г (0,1 моль) 2- пиразолил-(1)-4-аминобензимидазола и 100 смя этанола добавляют, при температуре О-5°С, размешивая, 17,8 г (0,11 моль) диэтиленового эфира пироугольной кислоты и снимают охлаждение. На другой день разбавляют загустевшую реакционную смесь 50 см этанола, кипятят и оставляют остывать. Затем изолируют осевший реакционный продукт при температуре 0°С и высушивают при 110°С. Получают 20 г соединения формулы
О II C HjO-C-NH
С-К-N
с т. пл. 186-187°С.
Перекристаллизация из этанола не производит никакого изменения в точке плавления.
Вычислено, %: С 57,56; Н 4,83; N 25,82; О 11,80.
Пример 4. В суспензию, состоящую из 29,85 г (0,15 моль) 2- пиразолила-(1)-5-амикобензнмидазола и 60 см метанола, добавляют в течение 1 час, размешивая, 22,1 г
(0,165 моль) диметилового эфира пироугольной кислоты. В продолжение этого времени смесь становится сначала жиже, а затем снова очень густой. Для лучшего перемешивания добавляют еще 165 слгз метанола. На другой
день охлаждают до -20°С, отсасывают, промывают метанолом с температурой около -60°С и высушивают при температуре 110°С. Получают 33,8 г соединения формулы
C-N-N
kJ
ст. пл. 215-217°С.
В случае надобности соединение можно далее очишать посредством повторного растворения из 70-кратного количества хлорбензола.
Вычислено, %: С 56,02; Н 4,31; N 27,23; О 12,44.
СхгНцЫзО-р (мол. вес 257,25).
Найдено, :%: С 56,0; Н 4,5; N 27,0; О 12,6.
Пример 5. В суспензию, состоящую из 28,85 г (0,15 моль) 2- пиразолил-(1)-5-аминобензимидазола и 90 см н-бутанола, добавляют, размешивая, в течение 40 мин 40,9 г 88%ного ди-н-бутилэфира пироугольной кислоты (0,165 люль). Получают прозрачный раствор, который после затравливания кристаллом превращается в густую кашу. Добавляют еще 50 СЛ& м-бутанола. На другой день смесь отсасывают при температуре 0°С, промывают петролейным эфиром и высушивают при 110°С. Получают 35,5 г соединепия формулы
Н-СфН9-0 С-НК-г 6
ст. пл. 173,5--175°С.
Перекристаллизация из 10-кратного количества хлорбензола повышает т. пл. до 175,5- 176°С.
Вычислено, %: С 60,19; Н 5,72; N 23,40; О 10,69.
CigHiTNsOa (мол. вес 299,33).
Найдено, %: С 60,7; Н 6,1; N 22,8; О 10,7.
Пример 6. В суспензию, состоящую из 39,8 S (0,2 моль) 2- пиразолил-(1)-5-аминобензимидазола и 80 сжз н-пропанола, добавляют в течение 50 мин 47,5 г (0,25 моль) ди«-пропилэфира пироугольной кислоты. Получают прозрачный раствор, который после затравливания кристаллом, застывает в густую кашу. Последню о размешивают на другой день с 750 CMS легкого бензина, затем отсасывают, промывают легким бензином и высушивают при температуре llp°C. Получают 54,8 г соединения формулы
H-C H O-C-NH О
ст. пл. 171,5-172,5°С.
Продукт может быть вторично растворен в горячей смеси из н-пропанола (горячего легкого бензина); т. пл. остается однако неизменной.
Вычислено, %: С 58,93; Н 5,30; N 24,55; О 11,22.
CuHisNsOa (мол. вес 285,30)
Найдено, %: С 58,8; Н 5,5; W 24,4; О 11,6.
Пример 7. В суспензию, состоящую из 59,7 г (0,3 моль) 2- пиниразолил-(1)-5-аминобензимидазола и 300 слгз изопропанола, добавляют в течение 20 мин, размешивая, 62,7 г (0,33 моль диизопропилэфира пироугольной кислоты. Сначала получают прозрачный раствор, из которого постепенно выпадает желаемый продукт. На другой день после охлаждения на льду продукт изолируют и высушивают при температуре 110°С. Получают 57,9 г соединения формулы
Пример 9. Из 2- 4-метоксипиразолил-(1) 5-аминобензимидазола и диметилового эфира ннроугольной кислоты получают аналогично примеру 8 соединение формулы
(1ГК,,
С т. пл. 235-235,5°С.
Вычислено, %: С 54,25; Н 4,56; iN 24,38; О 16,71.
CisHiaNjOs (мол. вес 287,27).
Найдено, %: С 54,1; Н 4,7; N 24,4; О 16,8.
Пример 10. В суспензию, состоящую из 22,7 г (0,1 моль} ,5-диметилпиразолил-(1)5-аминобеизимидазола и 100 еж метанола, добавляют в течение 15 мин 14,74 г (0,11 моль диметилового эфира пироугольной кислоты. Исходный материал переходит в раствор. На другой день его сгущают в вакууме и в заключение выпаривают при температуре бани 40°С. Как остаток, получают стекловидную пену, которую растворяют в 100 см теплого толуола. Из раствора выпадает при охлаждении желаемый продукт формулы
N
С Н О-С-НН II О
,C-N-N
й- и
ст. пл. 180,5-181,5°С.
Вычислено, %: С 58,93; Н 5,30; N 24,55; О 11,22.
CwHisNsOa (мол. вес 285,30).
Найдено, %: С 58,9; Н 5,4; N 24,3; О 11,7.
Пример 8. В суспензию, состоящую из 45,8 г (0,2 моль} 2- 4-метоксипиразолил-(1)-5аминобензимидазола и 200 сж-з этанола, добавляют, размещивая, 35,64 г (0,22 моль} диэтилэфира пироугольной кислоты. Сначала исходный продукт растворяют, и затем выкристаллизовывают реакционный продукт. На другой день его отделяют при температуре 0° и оставляют высохнуть. Получают 56,8 г соединения формулы
С jH, О - С - %.
о и,/OCHj
ст. пл. 209,5-210,5°С.
После перекристаллизации из этанола т. нл. 210211 5°С
Вычислено, %: С 55,80; Н 5,02; N 23,25О 15,93.
Его отсасЕэшают при 0°, промывают петролейным эфиром и высущивают. Получают 27,1 г с т. пл. 185-186,5°С и снова растворяют в толуоле. Толуол удаляют путем растворения в щестикратном количестве горячего ацетонитрила и в течение короткого времени нагревают до кипения. При этом выпадает свободная от растворителя субстанция. Ее отсасывают в холодном состоянии, промывают эфиром и высушивают при температуре 110°С.
Получают 17,6 г с т. пл. 186-186,5°С.
Вычислено, %: С 58,93; Н 5,30; N 24,55; О 11,22.
CuHisNjOa (мол. вес 185,30).
Найдено, %: С 58,9; Н 5,3; N 24,4; О 11,3.
Пример И. В суспензию из 22,7 г (0,1 моль) ,5-диметилпиразолил-(1)-5-аминобензимидазола в 100 слз этанола добавляют 17,82 г (0,11 моль) диэтилового эфира пироугольной кислоты, причем исходный материал постепенно растворяется. На другой день образуется кристаллическая каща. После охлаждения до -20°С ее отсасывают и промывают нетролейиым эфиром. Получают соединение формулы
C,H,0-C-1Sl j кристаллами этанола. Последний удаляют постепенным нагреванием до 110°С до постоянства веса. Препарат плавится при 175- 175 5°С Вычислено, %: С 60,19; Н 5,72; N 23,40; О 10,69. CnHnNsOa {мол. вес 299,33). Найдено, %: С 60,0; Н 5,7; N 23,3; О 10,9. Пример 12. В 22,7 г (0,1 моль) ,5-диметилпирозолил-(1)-5-аминобензимидазола в 100 сжз ызо-пропанола добавляют 20,9 г (0,11 моль} диизопропилэфира пироугольной кислоты. Постепенно образуется раствор, из которого выпадает позже желаемое соединениеiCHjJaCH-O-C-N-T С кристаллами изопропанола. Их отсасывают, промывают петролейным эфиром и высушивают (29,5 г). Для удаления кристаллов растворителя растворяют в возможно меньшем количестве кипящего ацетонитрила, кипятят короткое время, причем выделяется свободное or растворителя соединение, охлаждают, изолируют при температуре -20°С и высушивают при 110°С, Т- пл. лежит тогда при 178,5- 179°С. Вычислено, %: С 61,32; Н 6,11; N 22,35; О 10,21. CieHigNsOa (мол. вес 313,35). Найдено, %: С 61,4; Н 6,2; N 22,4; О 10,5. Пример 13. В хорошо размешанную смесь из 99,5 г (0,5 моль) 2- пиразолил-(1)-5аминобензимидазола и 250 см. пиридина добавляют при температуре О-5°С в течение 2,5 час 47,8 сжз (0,5 моль} этилового эфира хлоромуравьиной кислоты. На другой день отгоняют в вакууме 155 слгз пиридина. Полученную как осадок кашу размешивают с 3 л воды, причем желаемый продукт выделяется полностью. Отсасывают, промывают водой и высушивают сначала на воздухе, потом при 110°С. Получают 123 г с т. пл. 177,5-179°С. Перекристаллизацией из 8-кратного количества пропионитрила получают 115 г чистого соединения с т. пл. 180-180,5°С. Во всех своих свойствах оно вполне идентично продукту согласно примеру 1. Пример 14. В смесь, состоящую из 49,75 г (0,25 моль 2- пиразолил-(1)-5-аминобензимидазола и 125 сжз пиридина, добавляют при температуре О-5°С в течение 2 час, интенсивно размешивая, 34,6 г (0,25 моль} р-метоксиэтилэфира хлоромуравьиной кислоты. На другой день отгоняют в вакууме 45 слг- пиридина. Остается почти не размешиваемая каша. Добавляют 120 сл/з воды, причем образуется эмульсия. Последнюю размешивают с 3 л воды, и по прошествии некоторого времени отделяют соедин.ние формулы CHaOCHjGHa-O-C-N О Соединение отсасывают, промывают водой и высушивают, вес 57,8 г. Сырой продукт размешивают в течение 1 час с 120 смз ацетонитрила при температуре 70°С, добавляют к этому еще 50 см ацетонитрила, отсасывают при 0°С, промывают ледяным ацетонитрилом и оставляют высыхать. Продукт (49,0 г с т. пл. 156-158,5°С может быть перекрнсталлизован из ацетонитрила, точка плавления, однако, не повышается. Вычислено, %: С 55,80; Н 5,02; N 23,25; О 15,93. CuHisNgOs (мол. вес 301,30); Найдено, %: С 55,9; Н 5,2; N 23,2; О 16,3. Пример 15. В смесь из 49,75 г (0,25 моль) 2- пиразолил-(1)-5-аминобензимидазола и 125 смз пиридина добавляют при ледяном охлаждении и размешивании в течение 2 час 30,6 г (0,25 моль) изопропилэфира хлоромуравьиной кислоты. На другой день отгоняют в вакууме при 40°С (температура бани) 80 сжз пиридина. Оставшуюся массу размешивают с 3 уг воды, причем она затвердевает. Ее отсасывают, промывают водой и высушивают. Сырой продукт (67,9 г) перекристаллизовывают из пропионитрила; он плавится затем при 205-206°С. Соединение представляет собой более высоко плавящуюся модификацию продукта согласно примеру 7. Пример 16. В 49,75 г (0,25 Л(0.ль) 2- пиразолил-(1)-5-аминобензимидазола в 125 с.и пиридина добавляют при ледяном охлаждении и размешивании 35,75 г (0,25 моль р-хлорэтилэфира хлоромуравьиной кислоты. На другой день отдестиллируют из реакционной смеси при 40°С (температура бани) 45 смз пиридина. Полученную как осадок массу размещивают с 3 л воды, причем она постепенно кристаллизуется, затем ее отсасывают, промывают водой и высущивают. Получают 77 г сырого соединения формулы a-CH.,rH,-()-C-N Для очищения массу растворяют в 150 см теплого диметилформамида и осаждают, размешивая, с 1,5 л ацетонитрила. Продукт отсасывают, промывают эфиром и высушивают при температуре . Получают 55 г с т. пл. 189-189,5°С. Вычислено, %: С 51,10; Н 3,93; С1 11,61; О 10,48; N 22,90.
Найдено, %: С 51,1; Н 4,3; С1 11,4; О 10,40; N 22,7.
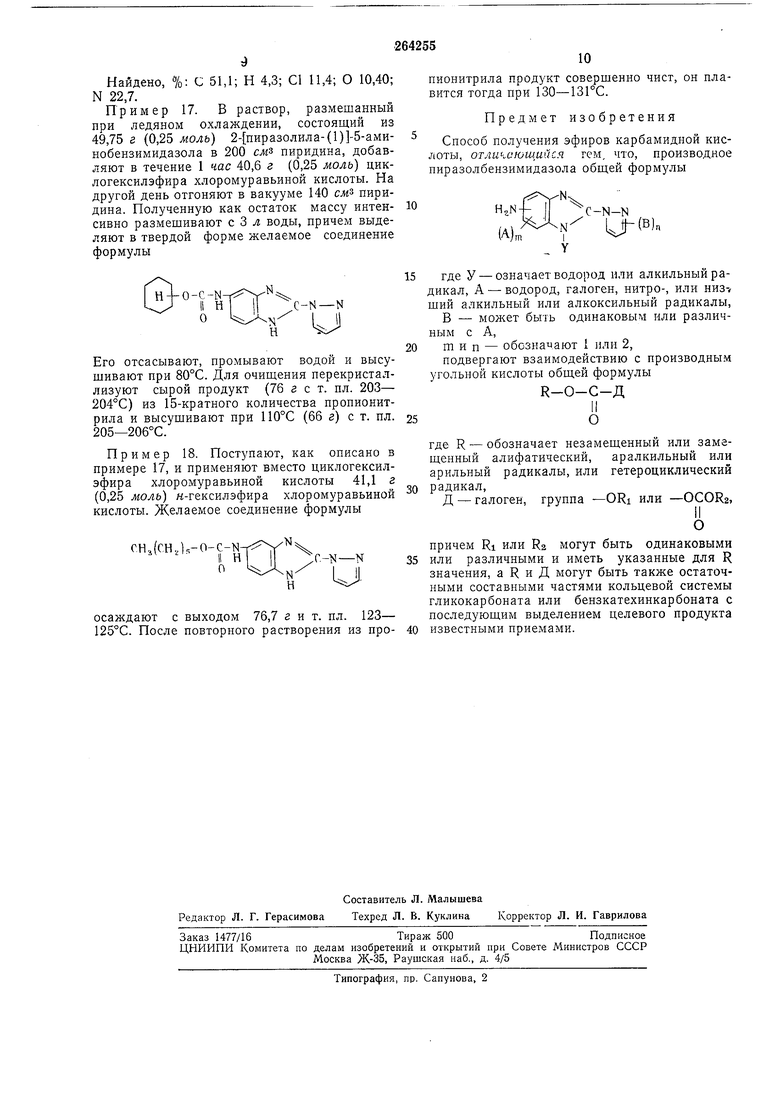
Пример 17. В раствор, размешанный при ледяном охлаждении, состоящий из 49,75 г (0,25 моль) 2- пиразолила-(1)-5-аминобензимидазола в 200 слз пиридина, добавляют в течение 1 час 40,6 г (0,25 моль) циклогексилэфира хлоромуравьнной кислоты. На другой день отгоняют в вакууме 140 см пиридина. Полученную как остаток массу интенсивно размешивают с 3 л воды, причем выделяют в твердой форме желаемое соединение формулы
H4-0-C-N- J 11 Н I I
C-N-N
о Н
Его отсасывают, промывают водой и высушивают при 80°С. Для очищения иерекристаллизуют сырой продукт (76 г с т. нл. 203- 204°С) из 15-кратного количества пропионитрила и высушивают при 110°С (66 г) с т. пл. 205-206°С.
Пример 18. Поступают, как описано в примере 17, и применяют вместо циклогексилэфира хлоромуравьиной кислоты 41,1 г (0,25 моль) н-гексилэфира хлоромуравьиной кислоты. Желаемое соединение формулы
CH,(CH.J,-0-C-N-r; V 4
1 Н r-N-N
Ч.Х I Н осаждают с выходом 76,7 гит. пл. 123- 125С. После повторного растворения из пропионитрила продукт совершенно чист, он плавится тогда при 130-13ГС.
Предмет изобретения
Способ получения эфиров карбамидной кислоты, oтлu -aющuйcя гем, что, производное пиразолбензимидазола общей формулы
10
C-N-N ijh(B)n
где У - означает водород или алкильный радикал, А - водород, галоген, нитро-, или низ-, ший алкильный или алкоксильный радикалы,
В - может быть одинаковым или различным с А,
тип - обознач.ают 1 или 2,
подвергают взаимодействию с производным угольной кислоты общей формулы
R-0-С-Д
II О
где R - обозначает незамещенный или замещенный алифатический, аралкильный или арильный радикалы, или гетероциклический радикал,
Д - галоген, группа -ORi или -OCORa,
II О
причем RI или Ra могут быть одинаковыми или различными и иметь указанные для R значения, а R и Д могут быть также остаточными составными частями кольцевой системы гликокарбоната или бензкатехинкарбоната с последующим выделением целевого продукта известными приемами.



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,1Л-ТРИХЛОРЭТАНА | 1972 |
|
SU353412A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2-АМИНО- 5-НИТРОТИАЗОЛА | 1972 |
|
SU354658A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАМИНОСОЕДИНЕНИЙ | 1973 |
|
SU399109A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ5,П-ДИГИДРО-6Н-ПИРИДО-[2,3-Ь]-[1,4]-БЕНЗО-ДИАЗЕПИН-6-ОНА | 1972 |
|
SU331554A1 |
| ВПТБ10Й €51Д;Г.ТГ;!Г?5Т?ЯШ145ИСП511 | 1973 |
|
SU374825A1 |
| СПОСОБ ПОЛУЧЕНИЯ ОПТИЧЕСКИ АКТИВНЫХ | 1969 |
|
SU242777A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПИПЕРАЗИНА | 1973 |
|
SU363248A1 |
| СПОСОБ ПОЛУЧЕНИЯ АРИЛСУЛЬФОНИЛМОЧЕВИН, СОДЕРЖАЩИХ ГЕТЕРОЦИКЛИЧЕСКИЕ АЦИЛАМИННЫЕГРУППЫ | 1972 |
|
SU359817A1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛОВЫХ ЭФИРОВ АМИДОТИОНОФОСФОРНОЙ КИСЛОТЫ | 1971 |
|
SU321006A1 |
| СПОСОБ ПОЛУЧЕНИЯ ы-ЦИАНАЛКИЛКАРБАМИЛ- БЕНЗИМИДАЗОЛОВ12 | 1973 |
|
SU365887A1 |


Авторы
Даты
1970-01-01—Публикация