Изобретение относится к способу получения не описаиных в литературе производных 1,3диазетидина, которые могут найти применение в качестве вулканизирующих агентов, а также в синтезе физиологически активн з1х веществ.
Предлагается способ получения 2,4-диамино-2,4-бис(амиптио)-1,3- бис{арилсульфонил)1,3-диазетидинов, заключающийся в том, что соли щелочных металлов аренсульфамидов подвергают взаимодействию с трихлорметапсульфепилхлоридрм в воде или четыреххлористом углероде при охлаи дении от -1,5 до 3°С предпочтительно и молярном соотношении компонентов 2:1. Полученный 2,4-дихлор-2,4 - бис (хлортио)-1,3 - бис(арилсульфонил)-1,3-диазетидин обрабатывают аминами в органическом растворителе при 20-37°С с последующим выделепием целевых продуктов известными нриемами.
Пример 1. Синтез 2,4-дихлор-2,4-бис(хлортио)-1,3-бис(бензолсульфопил)-1,3 - диазетидина.
В реактор на 1 л, снабженный механической мешалкой, термометром и канельной воронкой, загружают 20 г (0,5 г-моль) едкого натра, 500 мл воды и 78,6 г (0,5 г-моль) бензолсульфамида. Реакционную массу при перемешивании подогревают па водяной бапе до полного растворения бензолсульфамида, затем охлаждают до -1,5°С. К охлажденной реакцпогпюй массе нрн интенсивном перемепшвании по каплям в теченне 20 инн нрнбав ляют 50,16 г (29,5 мл; 0,27 г-моль) трихлорметансульфенилхлорпда (ТХМСХ) при указанной темнературе. После этого реакц1по продолжают вести при -1,5°С п перемешиваннн до исчезновепня 1целочной среды (I час).
Полученный осадок отфильтровывают на воропке Бюхнера днаметром 12 см, промывают 50 мл воды п отжимают досуха. Затем промывают 50 мл петролейного эфира для удалеппя следов ненрореагировавшето ТХМСХ. После сушки осадка в течение 6 час при 30-40°С и атмосферном давлении получают бесцветпую кристаллическую смесь 2,4дпхлор-2,4-бис(хлортио)-1,3 - бис(бепзолсульфоннл)-1.3-дпазетнднна (I) п бепзолсульфампда.
Выделяют продукт (I) из смеси одним из двух .методов:
перекрнсталлизацией из н-гептана;
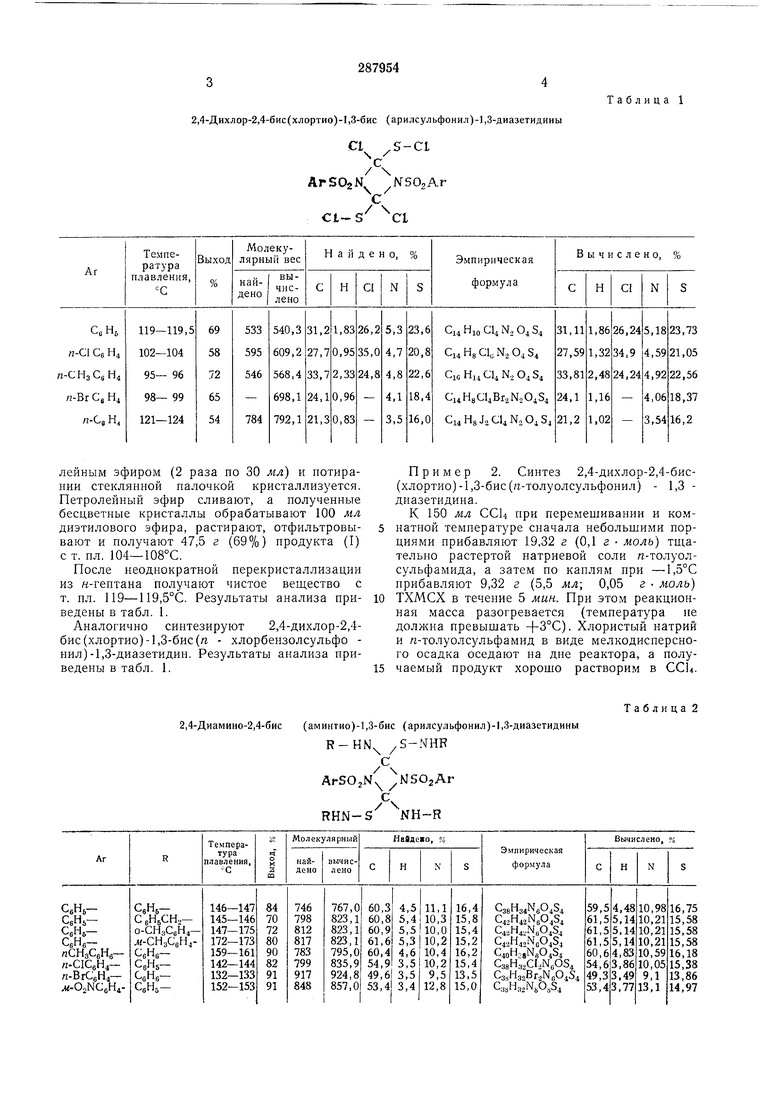
обработкой смесп CCLi (2 раза но 200 мл) при пагреватпп до 60°С для полпого растворения нродукта (I), с последуюнхпм охлаждепием и отфильтровыванпем бензолсульфамида в количестве 39 г (99%). Фильтраты сливают в колбу и отгоняют ecu на кипящей водяиой бане. После отгопки СС14 в колбе остается масло, которое при обработке петро2,4-Дихлор-2,4-бис(хлортио)-1,3-бис (арилсульфонил)-1,3-диазетидины
ArSOaN КЗОгАг
ct-s ci
Таблица 1
С1 /S-CI
)

| название | год | авторы | номер документа |
|---|---|---|---|
| ПАТЕНТИО-ТЕКВГ'Е^КАПБИБЛИОТЕКА | 1971 |
|
SU301330A1 |
| СПОСОБ ПОЛУЧЕНИЯ АРЕНСУЛЬФО-2,4-ДИНИТРОАНИЛИДОВ | 1967 |
|
SU192803A1 |
| СПОСОБ ПОЛУЧЕНИЯ АРЕНСУЛЬФОНИЛ-(ДИНИТРОАРИЛАМИДОВ) | 1971 |
|
SU292971A1 |
| СПОСОБ ПОЛУЧЕНИЯ N-(БEHЗOKCAЗOЛ-2-CУЛЬФEHИЛ)--N,N^-БИC-(APИЛCУЛЬФOHИЛ)-БEHЗOKCAЗOЛ-2- | 1973 |
|
SU384823A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 5,7-ДИХЛОР-6-ОКСИИНДОЛА | 1972 |
|
SU425907A1 |
| СПОСОБ ПОЛУЧЕНИЯ НАТРИЕВОЙ СОЛИ 5-ЭТИЛ-5- | 1969 |
|
SU238551A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АРЕНСУЛЬФОНИЛ- 2,2-ДИМЕТИЛЭТИЛЕНИМИДОВ | 1965 |
|
SU176306A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АРЕНСУЛЬФОНИЛ-2-АРИЛ- ФОРМАМИДИНОВ | 1966 |
|
SU187777A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,4-БИС-(МОНОАЛКИЛАМИДО)-2,4,6,6- -ТЕТРАКИС(ДИМЕТИЛАМИДО)ЦИКЛОТРИФОСФАЗЕНОВ | 1967 |
|
SU202137A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АРИЛСУЛЬФОНИЛ- 2-ЦИАНЭТИЛЕНИМИДОВ | 1968 |
|
SU209453A1 |

лейным эфиром (2 раза по 30 мл) и потираний стеклянной палочкой кристаллизуется. Петролейный эфир сливают, а полученные бесцветные кристаллы обрабатывают 100 мл диэтилового эфира, растирают, отфильтровывают и получают 47,5 г (69%) продукта (I) ст. нл. 104-108°С.
После неоднократной перекристаллизации из н-гептана получают чистое вещество с т. пл. 119-119,5°С. Результаты анализа приведены в табл. 1.
Аналогично синтезируют 2,4-дихлор-2,4бис(хлортио)-1,3-бис(п - хлорбензолсульфо нил)-1,3-диазетидин. Результаты анализа приведены в табл. 1.
(аминтио)-1,3-бис (арилсульфонил)-1,3-диазетидины
R-HN /S-NHH ArSOjN МВОгАг RHN-S NH-R
Пример 2. Синтез 2,4-дихлор-2,4-бис(хлортио)-1,3-бис(«-толуолсульфонил) - 1,3 диазетидина.
К 150 мл ecu при перемешивании и комнатной температуре сначала небольшими порциями прибавляют 19,32 г (0,1 г моль) тщательно растертой натриевой соли п-толуолсульфамида, а затем по каплям при -1,5°С прибавляют 9,32 г (5,5 мл; 0,05 г моль)
ТХМСХ в течение 5 мин. При этом реакционная масса разогревается (температура не должна превышать +3°С). Хлористый натрий и л-толуолсульфамид в виде мелкодисперсного осадка оседают на дне реактора, а получаемый продукт хорошо растворим в CCU.
Таблица 2
С
С
я Ef
s E; vo
; S
Реакцию при постоянном перемешивании и - 1,5°С заканчивают после исчезновения щелочной среды (5-6 час). Осадок отфильтровывают и получают 8,32 г (97%) п-толуолсульфамида и 5,8 г (99,5%) NaCl. Фильтрат переносят в фарфоровую чашку и оставляют под тягой для упаривания на воздухе. После упаривания СС14 остается маслообразный продукт, который нри обработке петролейным эфиром (2 раза по 10 мл) п потираннн стеклянной палочкой кристаллизуется в виде бесцветных кристаллов. Вес полученного продукта 10,3 г (72,5 %), т. нл. 95-96°С после перекристаллизации из н-гексана.
По аналогичной методике получают и ДРУ гие соединения. Их формулы, выходы, температуры плавления и результаты анализов приведены в табл. 1.
Пример 3. Синтез 2,4-дифениламиио-2,4бис(фениламинтио) - 1,3 - бис(бензолсульфонил) -1,3-диазетидина.
В грушевидную колбочку емкостью 100 мл помещают 30 мл бензола и 1,7 г (0,00315 г-моль 2,4-дихлор-2,4-бис(хлортио)1,3-бнс (бензолсульфонил) -1,3-диазетидина. К
и 25 раствору прибавляют при встряхивании 2,35 г (2,29 мл; 0,0252 г-моль свел енерегнанного анилина. Реакция экзотермична. Скорость прибавления анилина регулируют так, чтобы не допустить сильного разогревания реакционной смеси (температура не должна превышать 37°С).
После прибавления всего количества анилина реакционную смесь, охладившуюся до комнатной температуры, фильтруют. Конец реакции определяют по исчезновению активного хлора (иодкрахмальная бумажка не синеет). Оставшийся иа фильтре нерастворимый в бензоле солянокислый анилин (1,6 г, 98,4%) нромывают 10 мл бензола. Из фильтрата путем высаждения (петролейный эфир или гексан) получают 2,03 г (84%) 2,4-дифениламино-2,4-бис (фениламинтио) -1,3- бис (бензолсульфонил)-1,3-диазетидина; т. пл. 146- 147°С после перекристаллизации из этанола.
45
По аналогичной методпке получают целый ряд2,4-диамипо-2,4-бис(аминтио) -1,3-бис(арилсульфонил)-1,3-диазетидинов, приведенных в табл. 2.
В табл. 3 приведены характерные полосы
50 поглощения И1 -спектров 2,4-ди.хлор-2,4-бис (хлорти)-1,3 - бис(арилсульфоннл)-1,3-дназетидинов и других синтезированных эталонных соединений в соноставлении с литератур5 55 нымн данными, см.
Предмет изобретения
и S X
Способ получеипя 2,4-диамино-2,4-бис (аминтио)-1,3 -бис(арилсульфонил)-1,3-диазе 60 тидинов, отличающийся тем, что трихлормеWтансульфенилхлорид подвергают взаимодействию с солями щелочных металлов аренсульфамидов в воде или четыреххлористом углероде при охлаждении и молярном соотно шении компонентов 2 : 1 с последующей обработкой полученного 2,4-дихлор-2,4-бис(хлортио)-1,3 - бис(арилсульфонил)-1,3-диазетиди8на аминами в органическом растворителе и выделением целевого продукта известными приемами.

Даты
1970-01-01—Публикация