Предлагается способ получения новых алкиловых эфиров алкилзамещенных резорциловых кислот, которые могут найти применение в парфюмерии.
Обнаружено, что некоторые из этих соединений обладают приятным ароматом, напоминающим запах природных экстрактов дубового мха «мусс-де-шен.
Полученные алкилзамещенные (в ядро) резорциловые кислоты и сложные эфиры на их основе можно представить следующей общей формулой
OR,
в которой каждый из заместителей Ri и R2 представляет собой алкильный радикал, содержащий от 1 до 5 атомов углерода, причем по крайней мере один из радикалов Ri или R2 содержит два и более атомов углерода, а R представляет собой атом водорода или низщий алкильный радикал, содержащий от 1 до 5 атомов углерода, предпочтительно от 1 до 3 атомов углерода. К числу заявляемых соединений
этого типа, общая формула которых представлена выще, относятся следующие соединения; метил-3-метил-6-изопропилрезорцилат, метил-3-изопропил-6-метилрезорцилат, метил-3,6-диэтилрезорцилат,
метил-З-метил-6-н-бутилрезорцилат, метил-3,6-ди-н-пропилрезорцилат, метил-3,6-ди-изобутилрезорцилат, метил-3,6-ди-н-бутилрезорцилат, этил-3-к-пропил-6-метилрезорцилат,
3,6-ди-изопропилрезорциловая кислота, метнл-3-н-метил-6-метилрезорцилат, метил-3-метил-6-метилрезорцилат. Соединения, отвечающие формуле, могут быть получены при использовании известных закономерностей путем взаимодействия моноили диалкилзамещенных (в ядро) дигидрорезорцилатов (т. е. сложных эфиров соответствующих дигидрорезорциловых кислот) с окислителем, содержащим хлор. Этот метод довольно прост, удобен и выгоден, дает высокий выход продуктов и не сопровождается нежелательными побочными реакциями.
Соответствующие моно- или диалкилзамещенные (в ядро) гидроалкилрезорциловые кислоты и их сложные эфиры, пригодные в качестве исходных веществ для осуществления упомянутой реакции, можно представить с помощью следующих общих структурных формул:в которых каждый из символов Ri, Rz и Rs обозначает атом водорода или низший алкильный радикал, содержаш,ий в своем составе or 1 до 5 атомов углерода, включая метильный, этильный, пропильный, бутильный, изонропильный и амильный радикалы, причем по крайней мере один из заместителей Hi или R2 непременно представляет собой такой низший алкильный радикал. В качестве исходных веществ могут быть использованы также смеси подобных изомеров. Конкретный выбор соогветствуюш,его исходного соединения можег быть сделан в зависимости от того, какой конечный продукт желательно получить. Выбрапный в качестве исходного веш,ества дигидрорезорцилат должен быть по возможности чистьш; это условие является необходимым с точки зрения предотвращения нежелательных побочных реакций и облегчения выделения и очистки конечного продукта реакции окислительной дегидрогенизации. В качестве окислителя, содержащего хлор, можно использовать молекулярный хлор или любое соединение, которое в условиях реакции снособно генерировать атомарный хлор, например хлорноватистую кислоту или нитрозилхлорид. Лучше всего использовать в качестве упомянутого окислителя свободный хлор. Выход желаемых нродуктов, который получается при осуществлении упомянутой реакции по методу, заявляемому в соответствии с настоящим изобретением, во многом зависит от степени контактного взаимодействия указанных реагентов. Так, если время контактирования окислителя с дигидрорезорциловой кислотой или ее сложным эфиром окажется слишком незначительным, выход соответствующего продукта заметно падает. В реакционной смеси остается большое количество исходных веществ, которые необходимо по возмолшости полностью удалить, чтобы выделить желаемый продукт реакции. Если же для более тесного контактного взаимодействия упомянутых реагентов использовать энергичное перемешивание или другие методы эффективной турбулизации реакционной смеси (т. е. стараться максимально увеличить поверхность контактирования реагентов), реакцию можно провести с высокой степенью конверсии. При этом уменьшается вермя, необходимое для контактирования и увеличивается выход желаемого продукта. При использовании в качестве окислительного хлорного материала хлорноватистой кислоты применяется двухфазная водно-неводная реакционная система, которая состоит из двух не смешивающихся между собой фаз - водной тактирования (т. е. степень поверхностного взаимодействия) между двумя этими фазами является важнейшим фактором, от которого зависит и которым определяется выход конечного продукта. Степень контактирования этих фаз можно изменять и регулировать в желаемых пределах в зависимости от того, какой способ перемешивания или встряхивания реакционной системы применяется для этой цели, Реакцию между днгидрорезорциловыми кислотами или их эфирами и окислительным хлорным материалом желательно проводить в среде инертного растворителя, хорошо растворяющего исходный дигидрорезорцилат, поскольку при температуре порядка 20-30 С, которая является наиболее предпочтительной для проведения реакции, большинство дигидрорезорцилатов находится в твердом состоянии. Растворитель, таким образом, способствует гомогенизации реакционной смеси и позволяет эффективно влиять на контактное взаимодействие упомянутых реагентов. Наиболее подходяшими для этой цели инертными в условиях реакции растворителями являются такие нереакционноспособные галогенированные углеводороды, как хлороформ и тетрахлорэтан. При выборе условий проведения реакции (включая температуру и давление) необходимо учитывать время осуществления реакции, химическую природу используемых реагентов и вид продукта, который желательно получить. Как правило, реакцию целесообразно проводить при атмосферном давлении, хотя можно использовать и повышенное. Оптимальная для нроведения реакции температура примерно ог 15 до 50°С, причем наиболее предпочтительна температура от 20 до 30°С. Допускаются также и некоторые отклонения от указанного температурного интервала. Продолжительность реакции зависит от того, при какой температуре она проводится и под каким абсолютным избыточным давлением находится при этом реакционная смесь. На продолжительность реакции могут также оказывать влияние химическая природа реагирующих веществ, способ перемешивания реакционной системы, стенень и продолжительность контактирования реагентов, желаемый выход продукта реакции и степень ее конверсии. Как установили, в большинстве случаев желательно проводить реакцию в течение 1-10 час. Сокращение времени реакции ниже указанного предела отрицательно влияет на выход конечного продукта, а увелнчение продолжительности реакции не дает никаких преимуществ. Упомянутую реакцию удобно проводить путем растворения или суспендирования исходной дигидрорезорциловой кислоты или ее сложного эфира в инертном органическом растзорителе, нанример в хлороформе. В результате образуется двухфазная суспензия твердого вещества в его насыщенном растворе. Окислительный хлорный материал, например газообразный хлор, вводится в реакционную
реакционную массу, которую при этом энергично перемешивают или взбалтывают с целью достижения наибольшей степени контактирования реагентов. Введение окислительного хлорного материала в реакционную смесь прекращается в тот момент, когда хлор перестает поглощаться и реакционная масса становится прозрачной. После этого производится удаление органического растворителя из реакционной среды, отделение непрореагировавщих исходных веществ от продукта реакции и, наконец, извлечение и очистка желаемого продукта реакции. Все эти операции выполняются с помощью обычных, наиболее удобных в конкретной ситуации методов, включая перегонку, селективную (избирательную) экстракцию и тому подобное.
Пример 1. Получение метил-3,6-диметилрезорцилата.
В 5-литровую реакционную колбу, снабженную мещалкой, обратным холодильником, термометром и барботером для ввода газа, помещают 450 г метил 3,6-диметилдигидрорезорцилата, суспендированного в 2,5 л хЛороформа. Затем при интенсивном перемещивании в реакционную смесь через барботер пропускают газообразный хлор (при атмосферном давлении и комнатной температуре), который пробулькивает через реакционную массу и частично поглощается ею. Пропускание газообразного хлора через реакционную смесь продолжают до тех пор, пока хлор не перестает поглощаться реакционным раствором, который к этому времени становится прозрачным. В течение всего времени пропускания газообразного хлора реакционную смесь в колбе энергично перемещивают. Перемещивание продолжают для облегчения удаления из него реакционной массы хлористого водорода. Когда выделение хлористого водорода практически прекращается, из реакционной массы отгоняют хлороформ. В колбе после отгонки растворителя остается твердый продукт весом 476,3 .. Это твердое кристаллическое вещество смещивают с диэтиловым эфиром, и полученную смесь переносят в делительную экстракционную воронку для удаления непрореагировавшего исходного вещества водным раствором бикарбоната натрия. Эфирный слой промывают после этого 10%-ным водным раствором гидроокиси натрия. Полученную таким образом водную фазу подкисляют соляной кислотой и охлаждают до 0°С. После этого к охлажденной водной фазе прибавляют еще некоторое количество соляной кислоты до рН 2. Осадок, выпадающий из водного раствора в процессе его подкисления, отфильтровывают, дважды промывают на фильтре водой и затем сушат до постоянного веса. Высущенный кристаллический продукт весит 224,4 г. Анализ полученного продукта с помощью инфракрасной спектроскопии, ЯМР-спектроскопии и масс-спектрометрии показал, что он представляет собой желаемый метил-3,6-диметилрезорцнлат. Полученный таким образом продукт
плавится при температуре от 30,8 до 13б,6°С, имеет приятный запах, напоминающий запах экстракта дубового мха (экстракта «мусс-дещен). Выход метил-3,6-диметилрезорцилата
составляет 50,4%, а степень конверсии в расчете на непрореагировавщий исходный продукт 75,0%.
Пример 2. Получение метил-3-изопропил6-метилрезорцилата.
В 2-литровую круглодонную колбу, оборудованную мешалкой, термометром, барботером и обратным холодильником, загружают 211 г метил-3-изопропил-6-метил-дигидрорезорцилата и 1000 мл хлороформа. Затем через
реакционную смесь при атмосферном давлении и комнатной температуре пропускают газообразный хлор до тех пор, пока он не перестанет растворяться в реакционной массе. После этого реакционный раствор перемешивают еще некоторое время, а затем упаривают с помощью испарителя для удаления из раствора хлороформа. В результате упаривания получают вязкое масло, которое закристаллизовывается при стоянии. Твердое кристаллическое вещество растворяют в диэтиловом эфире, и полученный эфирный раствор промывают в делительной воронке насыщенным водным раствором бикарбоната натрия до прекращения выделения углекислого газа.
Затем эфирный раствор экстрагируют 10%ным водным раствором гидроокиси натрия при температуре порядка 50°С, и экстракт отфильтровывают в вакууме с целью удаления следов серного эфира, щелочной экстракт нейтрализуют концентрированной соляной кислотой (при температуре 5°С) до рН, равного 2. При этом выпадает в осадок вязкая смолистая масса, которая кристаллизуется после непродолжительного стояния при температуре 0°С. Это твердое вещество растворяют в метаноле, обесцвечивают активированным углем и перекристаллизовывают из смеси метанол-вода. Полученное твердое кристаллическое вещество высушивают до постоянного веса. Вес продукта (метилового эфира 3-изопропил-6-метилрезорциловой кислоты) 36,2 г, т. пл. от 125,6 до 135,8°С.
Аналогично получены все остальные перечисленные выще представители соединений,
отвечающих формуле.
Предмет изобретения
1. Способ получения алкиловых эфиров алкилзамещенных в ядро резорциловых кислот, общей формулы
b-i
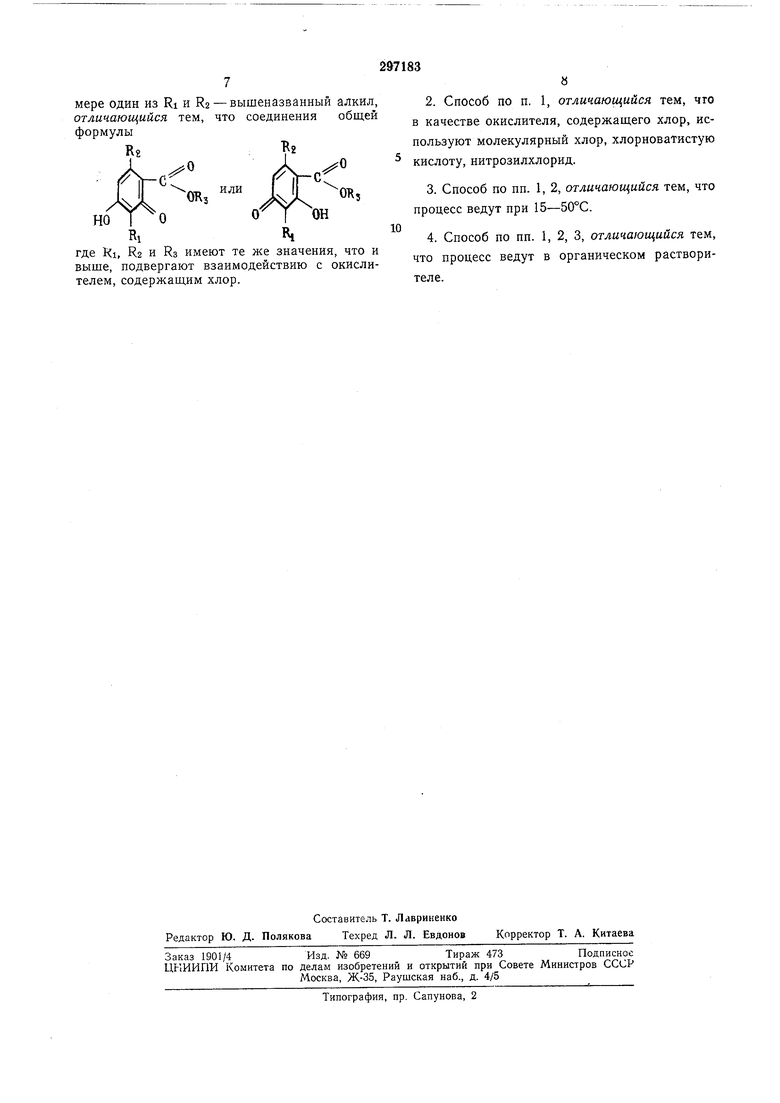
мере один из Ri и Кз - вышеназванный алкил, отличающийся тем, что соединения общей формулы
2
ИЛИ
где Ki, R2 и Rs имеют те же значения, что и выше, подвергают взаимодействию с окислителем, содержашим хлор.
2.Способ по п. 1, отличающийся тем, что в качестве окислителя, содержащего хлор, используют молекулярный хлор, хлорноватистую кислоту, нитрозилхлорид.
3.Способ по пп. 1, 2, отличающийся тем, что процесс ведут при 15-50°С.
4.Способ по пп. 1, 2, 3, отличающийся тем, что процесс ведут в органическом растворителе.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ЬЗАМЕЩЕННОГО 5-НИТРО-2-ИМИДАЗОЛА | 1973 |
|
SU385446A1 |
| СПОСОБ ПОЛУЧЕНИЯ 6-МЕТИЛЕНТЕТРАЦИКЛИНА | 1972 |
|
SU341225A1 |
| СПОСОБ ПОЛУЧЕНИЯ САЛИЦИЛАНИЛИДОВ | 1971 |
|
SU313352A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭНАНТИОМЕРОВдяс-1,2-эпоксипропилФосФОновой кислотыили ЕЕ СОЛЕЙ | 1971 |
|
SU293356A1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНОГО ЭФИРА ДЕЗАЦЕТОКСИЦЕФАЛОСПОРИНА | 1972 |
|
SU352464A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ КУМЕРМИЦИНОВ | 1972 |
|
SU342339A1 |
| СПОСОБ ПОЛУЧЕНИЯ (ДЯС-1,2-ЭПОКСИПРОПИЛ)- ФОСФОНОВОЙ кислоты или ЕЕ ПРОИЗВОДНЫХ | 1971 |
|
SU293357A1 |
| СПОСОБ ПОЛУЧЕНИЯЕИБЛг;СТ1::М(дяс-1,2-эпоксипропил)ФОСФОНовой кислотыили | 1971 |
|
SU294341A1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕНЗАМИДОВ | 1972 |
|
SU340159A1 |
| СПОСОБ ПОЛУЧЕНИЯ Д>&/С-1,2-Э110КСИГП>&ОПИ^1ФОСФОНОВОИ кислоты или ЕЕ ПРОИЗВОДНЫХ | 1971 |
|
SU315360A1 |


Авторы
Даты
1971-01-01—Публикация