СПОСОБ ПОЛУЧЕНИЯ БИС-(4-ГИДРОКСИ-3,5-ДИАЛКИЛБЕНЗИЛ)-ОВЫХ ЭФИРОВ КАРБОНОВОЙ КИСЛОТЫ
12
Изобретение относится к способу получения бис- (4-гидрокси-3,5-диалКИлбензил) -овых эфиров карбоновой кислоты, которые могут найти применение в качестве стабилизаторов полимеров против действия кислорода, света и тепла.
Предлагаемый способ получения бис- (4гидрокси- 3,5 - диалкилбензил) - овых эфиров карбоновой кислоты общей формулы
CHjHa(
CH,Hfli
где Hal - галоид,
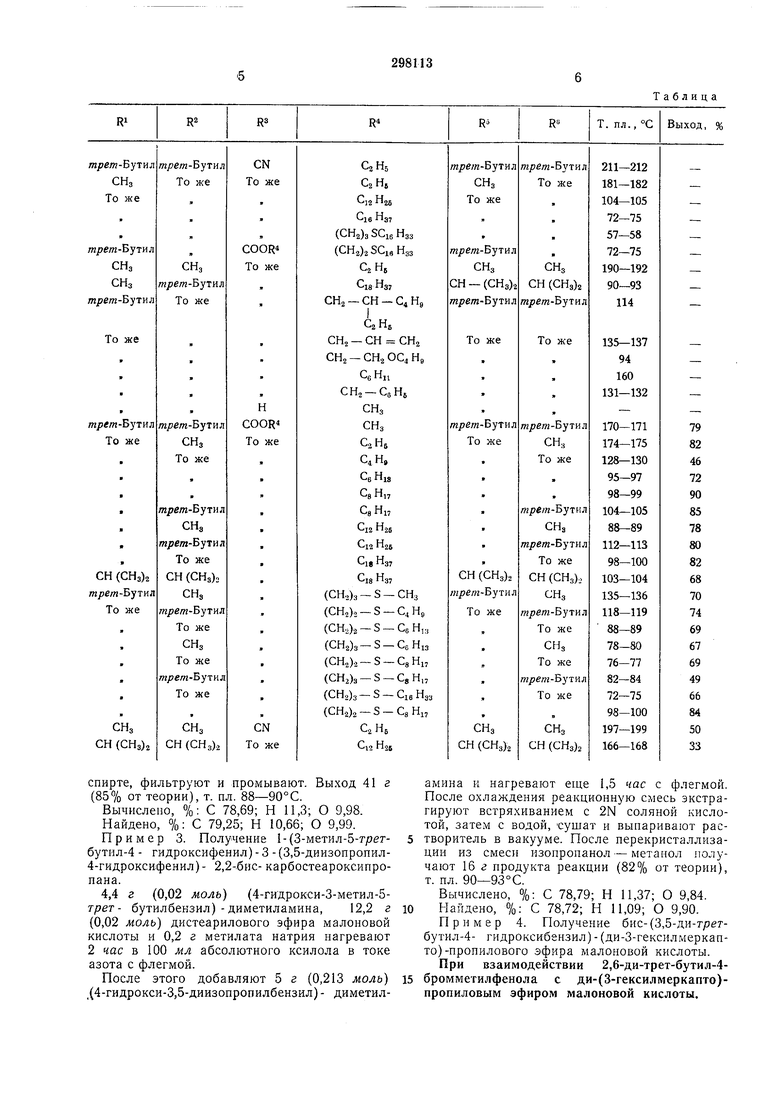
в присутствии щелочного металла или одинаковых или различных оснований Манниха 10 общих формул c-coffsT I где R, R2, R и R - одинаковые или различные GI-Сб-алкильные группы с прямой или разветвленной цепью; R3 - водород, CN, COOR4; R4 - алкил, прямой или разветвленный, циклический, насыщенный или ненасыщенный, тиоэфирная, эфирная или аралкильная группа с 1-20 атомами углерода, заключается во взаимодействии двух молей одинаковых или различных бензилгалогенидов формул ч НО(R - низщий алкил предпочтительно) в присутствии каталитических количеств оснований щелочных или щелочноземельных металлов, желательно их алкоголятов, с одним молем эфира карбоновой кислоты общей формулыR I CH,-COOR другими подходящими растворителями могут .быть общеизвестные углеводороды, гликолевый эфир и другие высококипящие эфиры. Кроме того, в качестве растворителей могут применяться спирты типа НЮН. Реакцию проводят при нагревапии, главным образом до температуры кипения реакционной массы. Получение исходных бенз-илгалогенидов представляет определенные трудности, и выход продуктов взаимодействия бензилгалогенидоБ с эфирами карбоновой кислоты составляет около 50%. Используемые основания Манниха, которые, как известно, легко полу iin-
i-HO- -CHj-CH-COOR NHRj
Р2
f чаются из фенолов, формальдегида и вторичных аминов (в частности диметиламина), напротив, дают с эфирами карбоновой кислоты практически количественно продукт реакции, так чтоэтот способ особенно экономичен. При получении несимметричных бис-продуктов с ярко выралсенной специфической активностью, когда используют основания Маиниха, сначала реагирует лишь 1 моль основания Манниха с 1 моль эфира карбоновой кислоты, образуя промежуточное соединение по следующей схеме:
которое затем реагирует со вторым молем основания Манниха по схеме
к
в
„... ,:. ., .. ..
CHj- СД.-СООЛ ч. но CHjNRj-
.
р,/ f
уС-СООВ NHB,
Обе реакции могут бьпь проведены в одном и том же реакционном сосуде.
При получении симметричных бис-нродуктов 2 моль основания Манниха нагревают с 1 моль эфира карбоновой кислоты (малонового, циануксуснокислого) в присутствии 1-20 г алкоголята щелочного или щелочноземельного металла в 1 л толуола, в токе азота в течение 1,5-4 час с флегмой и после охлаждения выделяют из реакционного раствора полученные продукты реакции, используя известные методы. Целесообразно сначала удалить катализатор, в частности посредством нейтрализации разбавленной кислотой и экстракции водой при встряхивании, после чего реакционный раствор высущить, отогнать растворитель в вакууме и очистить остаток, например перекристаллизацией. Выход составляет около 80-99% от теоретического.
Данную реакцию, т. е. «С-алкилирование фенольного основания Манниха до -получения дизамещенных эфиров малоновой или циануксусной кислоты, невозможно было предвидеть. По известным данным следовало ожидать, что фенольные основания Манниха дают гладкое «С-алкнлирование лишь в случае возможного взаимодействия, в частности с эфиром малоновой кислоты, если исходить из аммониевых солей енольных оснований Манниха, получение которых представляет значительную трудность.
Реакция между 2 моль фенольных оснований Манниха и 1 моль эфира малоновой или циануксусной кислоты до сих пор не была о.писана в литературе.
Бис-(4-гидрокси-3,5 -диалкилбензил)-эфирные соединения монокарбоновой кислоты общей формулы I, где , получают омылением и декарбоксилированием соответствующих эфиров циануксусной или двухосновной малоновой кислоты.
Пример 1. Получение бис-(4-гидрокси3,5-ди - т/зег-бутил-4-гидроксибензил)-этилового эфира циануксусной кислоты.
263,4 г (1 моль) (4-гидрокси-3,5-ди-тр 1Гбутилбензил)-диметиламина, 51 г (0,45 моль) этилового эфира циануксусной кислоты, 3 г зтилата магния и 5 г этилата натрия нагревают в 1 л абсолютного спирта в течение 1,5 час с флегмой, охлаждают, осажденный продукт реакции отфильтровывают. После экстракции встряхиванием с 96%-ным этиловым спиртом продукт реакции однократно перекристаллизовывают из 1,5 л ацетона. Выход 2аЗ г (99% от теории), т. пл. 212-213 С. Найдено, %: С 76,3; П 9,13. Вычислено, %: С 76,3; Н 9,35.
Пример 2. Получение бис-(4-гидрокси-3метил-5 - г/ует -бутилбензил)- дистеарилового
эфира малоновой кислоты.
2/,6 г (0,125 моль) {4-гидрокси-3-метил-5трет - бутилбензил)-диметиламина, 30,5 г (0,05 моль) дистеарилового эфира малоновой кислоты и 0,5 г метилата натрия нагревают
2,5 час в 100 мл абсолютного толуола в токе азота с флегмой, после охлаждения разбавляют метиленхлоридом, экстрагируют встряхиванием с 2N соляной кислотой и водой, сушат над сульфатом натрия и досуха выпариТаблица


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ФЕНИЛГИДРАЗОНА | 1970 |
|
SU268296A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИСИЛАЗАНОВ | 1972 |
|
SU328593A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИСИЛАЗАНОВ | 1971 |
|
SU294355A1 |
| Способ получения диэтилового эфира 4-гидрокси-3,5-ди-трет-бутилбензил-N-ацетиламиномалоновой кислоты | 1988 |
|
SU1558897A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИПЕРАЗИНОФЕНОЛОВ | 2010 |
|
RU2454408C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННЫХ ПОЛИЭФИРОВ | 1973 |
|
SU407452A1 |
| СПОСОБ ПОЛУЧЕНИЯ АНИЛИДОВ ДИАЦИЛОКСИБЕНЗОЙНОИКИСЛОТЫ | 1972 |
|
SU346857A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ5,П-ДИГИДРО-6Н-ПИРИДО-[2,3-Ь]-[1,4]-БЕНЗО-ДИАЗЕПИН-6-ОНА | 1972 |
|
SU331554A1 |
| ОТВЕРЖДАЕМАЯ ЭПОКСИДНАЯ КОМПОЗИЦИЯ | 1970 |
|
SU413680A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ХИНОЛИНКАРБОНОСЫХ КИСЛОТ | 1973 |
|
SU399121A1 |

спирте, фильтруют и промывают. Выход 41 г (85% от теории), т. пл. 88-90°С.
Вычислено, %: С 78,69; Н 11,3; О 9,98.
Найдено, %: С 79,25; Н 10,66; О 9,99.
Пример 3. Получение 1 - (3-метил-5-грегбутил-4 - гидроксифенил) - 3 - (3,5-диизопро,пил4-гидроксифенил)- 2,2-бис- карбостеароксипропана.
4,4 г (0,02 моль) (4-гидрокси-3-метил-5трет- бутилбензил) - диметиламина, 12,2 г (0,02 моль} дистеарилового эфира малоновой кислоты и 0,2 г метилата натрия нагревают 2 час в 100 мл абсолютного ксилола в токе азота с флегмой.
амина и нагревают еще 1,5 час с флегмой. После охлаждения реакционную смесь экстрагируют встряхиванием с 2N соляной кислотой, затем с водой, сушат и выпаривают растворитель в вакууме. После перекристаллизации из смеси изопропанол-метанол получают 16 г продукта реакции (82% от теории), т. пл. 90-93°С.
Вычислено, %: С 78,79; Н 11,37; О 9,84. Найдено, %: С 78,72; Н 11,09; О 9,90.
Пример 4. Получение бис-(3,5-ди-трегбутил-4- гидроксибензил) - (ди-3-гексилмеркапто)-Пропилового эфира малоновой кислоты.
Авторы
Даты
1971-01-01—Публикация