Изобретение касается способа получения новых соединений - замещенных в цепи полиметингидантоцианиновых красителей - производных 1-циклогексилимидазолинона-4, которые применяются в качестве оптических сенсибилизаторов галогенидосеребряных эмульсий.
Известен способ получения незамещенных в цепи полиметингидантоцианиновых красителей взаимодействие1 1 четвертичных солеи 2-имидазолинона с ацетанилиновинильнымп или ацетанилинобутадиенильными производными. Сведения о получении замещенных в цепи красителей отсутствуют.
Предлагаемый способ получения замеще} ных в цепи полиметннгидантоцианиновых красителей общего строения
где Y и Y -S; Se; О; -СН СН-; С- --(СНз)2; R, R, R и R - углеводородный остаток; или 1; или 2 при /п 0,1 или 2 при я 1; R -углеводородный
остаток при А и В - атом водорода или галогена, углеводородный остаток, алкоксиили бензогруппа; X - кислотный остаток, заключается в том, что мероцианиновые красители общего строения 1 () -N-CsH« С-СНз N X где Y, А, R, R, R, п, X имеют указанные значения, конденсируют с четвертичными солями гетероциклических оснований общего строения €H)irZ где В, Y, R, R, ш и X имеют указанные значения; Z - группа атомов, отщепляющихся при конденсации, например -SCHs; -ОСНз; -N-СеНб, I сосн, в органическом растворителе в присутствии алифатического амина с выделением целевых продуктов известными приемами. Реакцию проводят при обычной температуре или при умеренном нагревании (до 110°С). Красители предлагаемым способом получают с достаточно высокими выходами (50-90%). Пример 1. Получение 3-метил-3-этил-1циклогексил - 4-кето - этилбензтиазолинилиден-2 -(р - метилбутенилиден)имидазолинотиамонометинцианинперхлората. Смесь 0,1 2 метилперхлората 1-циклогексил2-метил-5 - 3- этилбензтиазолинилиден -2-(рметилбутенилиден)имидазолинона-4 и U,l г этил-я -толуолсульфоната 2-метилмеркаптобензтиазола в 2 мл пиридина нагревают при 95°С 2 мин, добавляют 2 капли триэтиламина. Реакционную смесь нагревают при 95°С 3 час, охлаждают и краситель осаждают эфиром. Эфир сливают, краситель закристаллизовывают при затирании в воде. Кристаллы отфильтровывают, промывают большим количеством воды, смесью слирта и эфира (1:3), эфиром. Выход продукта 0,08 г (58,8%); темно-синие пластинки (из этилового спирта), т. пл. 185- 186°С. Найдено, %: N 8,08; 8,28. Сз4Нз9Н452ОбС1 Вычислено, %: N8,20. Максимум поглощения при 656 км (в эти10ВОМ спирте). Пример 2. Получение 3-метил-3-этил-1циклогексил - 4 - кето-5- 3 - этилбензтиазолинилиден-2 - (р- этилбутенилиден)имидазолинотиакарбоцианинперхлората. Смесь 0,09 г метилперхлората 1-циклогексил-2-метил -5 - 3 - этилбензтиазолинилиден-2(р-этилбутенилиден)имидазолинона-4 и 0,06 г этилметилсульфата 2-(р-метилмеркаптовинил) бензтиазола в 3 мл пиридина нагревают 20 мин при 95-105°С, охлаждают и краситель осаждают водой. Выделившиеся кристаллы отфильтровывают, промывают большим количеством воды, смесью спирта и эфира (1:3) и эфиром. Выход 0,06 г (50%); зеленые мелкие кристаллы (из метилового спирта), т. пл. 196-197°С. Найдено, %: N 7,75; 7,06. C37H43O5N4S2C1 Вычислено, %: N 7,75. Максимум поглощения при 760 нм (в метиловом спирте). Пример 3. Получение 3-метил-3-этил-5метокси-1 -циклогексил - 4-кето-5- 3 -этилбензтиазолинилиден-2 - (|3-метилбутенилиден)имидазолинотиакарбоциапинйодкда. Смесь 0,1 г йодэтилата 1-циклогексил-2-метил-5- 3- этилбензтиазолинилиден-2- (|3-метилбутенилиден)имидазолинона-4 и 0,1 г зтилл-толуолсульфоната 5-метокси-2-(р-ацетанилиновинил) бензтиазола в 2 мл уксусного ангидрида нагревают при 150°С 1-2 мин и добавляют 0,2 мл триэтиламина. Реакционную смесь выдерживают при обычной температуре в течение 30 мин. Выделивщиеся кристаллы отфильтровывают, промывают водой, смесью спирта и эфира (1:4) и эфиром. Выход 0,1 г (65,6%), зеленые пластинки (после однократной промывки кипящим метиловым спиртом), т. нл. 244-245°С. Найдено, %: N 7,25; 7,23. Сз7Н4зМ4О2521 Вычислено, %: N 7,31. Максимум поглощения при 760 нм (в метиловом спирте). Пример 4. Получение 3-метил-3-этил-1циклогексил-4-кето-5- 3 - этил-5 - метоксибензселеназолинилиден (р-этилбутенилиден) имидазолинотиакарбоцианинперхлората. Смесь 0,12 г метилперхлората 1-циклогексил-2-метил-5- 3-этил-5 - метоксибензселеназолинилиден -2- (р-этилбутенилиден)имидазолииона-4 и 0,1 г йодэтилата 2-(р-ацетанилиновинил) бензтиазола и 2 мл уксусного ангидрида кипятят в теченле 1-2 мин и добавляют 0,2 мл триэтиламина. Реакционную смесь кипятят 5 мин, охлаждают, и краситель осаждают водой. Выделившиеся кристаллы отфильтровывают, промывают большим количеством воды, смесью спирта и эфира (1:3) и эфиром. Выход 0,16 г (100%), зеленые пластинки (после однократной промывки кипящим этиловым спиртом), т. пл. 193-195°С. Найдено, %: N 6,97; 6,89. Сз8Н45ОбМ455еС1 Вычислено, %: N 7,00. Максимум поглощения при 770 нм (в этилово.м спирте).
линилиден этилиден)имидазолинотиамезометилдикарбоцианинперхлората.
Смесь 0,1 г метилперхлората 1-циклогексил2-метил-5- (3- этилбензтиазолинилиден - 2-этилиден)имидазолинона-4 и 0,08 г этилметилсульфата 2-(б- метилмеркапто-у-метилбутадиенил)-5,6-диметилбензтиазола в 4 мл пиридина нагревают при 100°С в течение 2 мин и добавляют 4 капли тризтиламина. Реакционную смесь нагревают в течение 25 мин при 100°С, охлаждают и краситель осаждают водой. Выделившиеся кристаллы отфильтровывают, промывают большим количеством воды, смесью спирта и эфира (1:3) и эфиром. Выход 0,12 г (75%), зеленые пластинки (после однократной промывки кипящим метиловым спиртом), т. пл. 253-254° С.
Найдено, %: N7,44; 7,42.
C38H4505N4S2C1
Вычислено, %: N 7,60.
Максимум поглощения при 760 нм (в метиловом спирте).
Пример 6. Получение 3-метил-3-этил-1циклогексил -4-кето-5-( этилбензселеназолинилиден-2- этилиден) имидазолинотиамезоэтилдикарбоцианинперхлората.
Смесь 0,12 г метилперхлората 1-циклогексил-2-метил-5-.(3- этилбензселеназолинилиден2-этилиден)имидазолинона-4 и 0,08 г этилметилсульфата 2- (б-метилмеркапто-у-этилбутадиенил)бензтиазола в 4 мл пиридина нагревают 2 мин при 90-95°С и добавляют 4 капли триэтиламина. Реакционную смесь нагревают 20 мин при 95°С, охлаждают и краситель осаждают водой.
Выделившиеся кристаллы отфильтровывают, промывают большим количеством воды, смесью спирта и эфира (1:3) и эфиром. Выход 0,12 2 (78,9%), зеленые пластинки, т. пл. 221 °С (из метилового спирта).
Найдено, %: N 7,24; 6,88.
Сз7Н4з05К455еС1
Вычислено, %: N 7,28.
Максимум поглощения при 750 ял; (в метиловом спирте).
Пример 7. Получение 3-метил-1 -этил-1 циклогексил- 4-кето-5- ( этилбензтиазолинилиден-2 - этилиден) имидазолинохиномезоэтилдикарбоцианинперхлората.
Смесь 0,12 г метилперхлората 1-циклогексил-2-л1етил - 5 - (3-этилбензтиазолинилиден-2этилиден)имидазолинона-4 и 0,12 г этилметилсульфата 2- (б-метилмеркапто-у-этилбутадиенил)хинолина в 6 мл пиридина нагревают 2 мин при 100°С и добавляют 6 капель триэтиламина. Реакционную смесь нагревают в течение 25 мин при 100°С, охлаждают и краситель осаждают водой. Выделившиеся кристаллы отфильтровывают, промывают большим количеством воды, смесью спирта и эфира (1:3) и эфиром. Выход 0,12 г (66,), темно-зеленые с бронзовым отливом пластинки (после однократной промывки кипящим
метиловыл спиртом), т. пл. 258-259°С. Найдено, %: N 8,00; 8,25.
СзоН4505К43С1
Вычислено, %: N 7,81.
Максимум поглощения при 780 нм (в .метиловом спирте).
Пример 8. Получение 3-метил-3-этил-1п,иклогексил-4-кето - 5 - (Г ,3, триметилиндоли:1нлиден - зтилиден) имидазолинотиамезометилдикарбоцианинперхлората.
Смесь 0,1 г метилперхлората 1-циклогексил2-метил -5-(Г,3,3- триметилиндолинилиден-2этилиден)имидазолинона-4 и 0,08 г этилметилсульфата 2-б-метилмеркапто-у-метилбутадиеН11л)бензтиазола ъ 4 мл пиридина нагревают
в течение 2 мин при 100°С и добавляют 4 капли триэтиламима. Реакционную смесь нагревают 20 мин при 95-100°С, охлал дают и краситель осаждают водой. Выделившиеся кристаллы отфильтровывают, промывают воДой, смесью спирта и эфира (1:7) и эфиром. Выход 0,12 г (85,7%), темно-зеленые с бронзовым отливом пластинки (из метилового спирта), т. пл. 199-200°С. Найдено, %: N 7.69; 7,58.
C38H45O5N4SC1
Вычислено, %: N 7,94.
Максимум поглощения при 740 нм (в метиловом спирте).
Предмет изобретения
Способ получения замещенны.к в цепи полиметингидантоцианиновых красителей общего строения


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ сенсибилизации галогенсеребряных фотографических эмульсий | 1975 |
|
SU545959A1 |
| Способ получения полиметиновых красителей (7-алкоксиродакарбоцианинов) | 1950 |
|
SU93725A1 |
| СПОСОБ ПОЛУЧЕНИЯ 7-АЛКИЛ-, АРАЛКИЛ- И ДИАЛКИЛАМИНОРОДАКАРБОЦИАНИНОВ | 1956 |
|
SU102811A1 |
| СПОСОБ ПОЛУЧЕНИЯ р-АЛКИЛ(АРИЛ)ЗАМЕЩЕННЫХ | 1969 |
|
SU241588A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИКАРБОЦИАНИНОВБ1Х ИЛИ ТЕТРАМЕТИНМЕРОЦИАНИНОВЫХ КРАСИТЕЛЕЙ | 1968 |
|
SU213575A1 |
| Способ получения имидамероцианиноцианиновых красителей | 1982 |
|
SU1076433A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИМЕТИНМЕРОЦИАНИНОВЫХКРАСИТЕЛЕЙ | 1968 |
|
SU210658A1 |
| Способ получения тетра- и гексаметингемициановых красителей | 1956 |
|
SU107123A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИМЕРОЦИАНИНОВ, ПРОИЗВОДНЬ!Х 3-МОНО- ИЛИ 3-ДИАЦИЛАМИНОРОДАНИНОВ | 1967 |
|
SU192017A1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРАМЕТИНГЕМИЦИАНИНОВЫХ КРАСИТЕЛЕЙ, ЗАМЕЩЕННЫХ В ПОЛИМЕТИНОВОИ ЦЕПИ | 1967 |
|
SU195316A1 |

R i-CH(СН С) N-Qi,,
с-()ш- сн4,
R. X
fytл
C,H,,
.-
)
X
пп
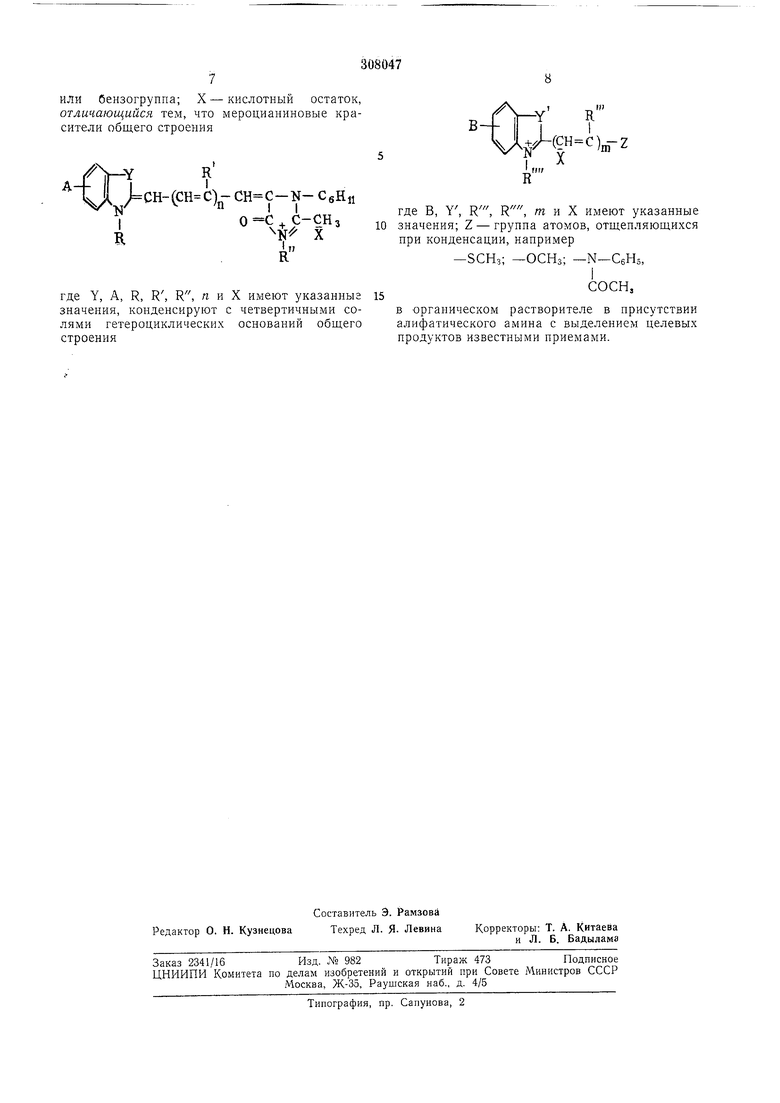
ИЛИ бензогруппа; X - кислотный остаток, отличающийся тем, что мероцианиновые красители общего строения
)-СН С-К-СбНй
С-СНз N X
R где Y, А, R, R, R, л и X имеют указанные15 значения, конденсируют с четвертичными солями гетероциклических оснований общего строения
308047
где В, Y, R, R, m и X имеют указанные 10 значения; Z - группа атомов, отщепляющихся при конденсации, например
-ЗСНз; -ОСНз; -N-CeHs, СОСН, в органическом растворителе в присутствии алифатического амина с выделением целевых продуктов известными приемами.
Даты
1971-01-01—Публикация