Изобретение относится к способу получения новых аналого-в простагландина EI (nPEi). nrEi имеет следующее строение:
н он
где прерывистая линия связи с кольцом циклопентана указывает заместителей в а-конфигурации, т. е. под плоскостью циклопентанового кольца. Толстые сплошные линии связи с циклопентановым кольцом указывают заместителей в р-конфигурации, т. е. над плоскостью циклопентанового кольца.
nPEi является производным простаповой кислоты, которая имеет следующее строение и нумерацию атомов:
соон
Химическое название нростановой кислоты 7-(2р -октил)циклонент - 1а - ил гептановая кислота.
Соединения формулы II, но с боковой ценью, оканчивающейся карбоксилом, связанной с циклопентановым кольцом в |3-конфигурации, называются 8- зо-простановыми кислотами и имеют следующую формулу:
10
COOR
15
Химическое название «зо-простановой кислоты 7- (2р - октил)цикло-1р - ил гептановая кислота.
ГЬрюстаглалдии Ej и его аналоги представляются следующей формулой
Mzri-COOR,
25
л. -4
НО ОН
в которой RI алкил с 1-8 атомами углерода, циклоалкил с 3-10 атомами углерода, аралкил с 7-12 атомами углерода, фенил, фенил, замещенный 1-3 атомами хлора, или алкилом с 1-4 атомами углерода, или этил, замещенный в р-положении 3 атомами хлора, 2 или 3 атомами брома или 1, 2, 3 атомами йода;
Ra - водород или алкил с 1-8 атомами углерода,-замещенный 1-3 атомами фтора;
Нз и R4 - водород или алкил с 1-4 атома1У1И углерода;
СпН2п-алкилен с 1-8 атомами углерода, замещенный 1-2 атомами фтора;
-- указывает характер ирисоединения группы - CnH2n COORi с кольцом в а- или |3-ко;нфигурации.
Формула IV представляет ПГЕь когда Ri, Rs, R4 являются водородами, Ra пентилом, СпН2п гекс а метилен ом, связь-СпН2п-COORi, с циклопентановым кольцом в «-конфигурации и конфигурация гидроксила в боковой цепи S.
В формуле IV к алкилам с 1-4 атомами углерода относятся метил, этил, пропил, бутил и их изомерные формы. Примерами алкила с 1-8 атомами углерода являются приведенные выше, а также пентил, гексил, гептил, октил и их изомерные формы.- К циклоалкилам с 3-10 атомами углерода, включающим алкилзамещенный циклоалкил, относятся циклопропил, 2,2-диметилциклоиропил, 2,3-диэтилциклоиропил, 2-бутилциклопрОПИЛ, циклобутил, 2-метилциклобутил, 3-пропилциклобутил, 2,3,4-триэтилциклобутил, циклопентил, -2,2 - диметилциклопентил, 3 -пентилциклопентил, 3-г/9ег-бутилц-иклопентил, циклогексил, 4-трег-бутилциклогексил, 3 - изопропилциклогексил, 2,2-диметилциклогексил, циклогептил, -циклооктил, циклононил, и циклодецил.
В качестве аралкила с 7-12 атомами углерода могут быть применены бензил, фенетил, 1-фенетилэтил, 2-фенилпропил, 4-фенилбутил, З-фен-илбутил, 2-(1-нафтилзтил), и 1-(2-нафтилметил).
Примерами фенила, замещенного 1-3 атомами хлора или адкил ом,-с .L-4/атомами углерода являются Я-5 лбрфёнил;./и-хлорфенил, о-хлорфенил, 2,4-дихлорфенил, 2,4,6-трихлорфенил, п-толил, иг-толил, о-толил, и-этилфенил, п-грег-бутилфенил, 2,5-диметилфе;нил, 4-хлор-2-метилфенил и 2,4-дихлор-З-метилфенил.
К алкилену с атомами угл-ерода относятся метилен, этилен, триметилен, тетраметилен, пентаметилен, гексаметилен, гептаметилен, октаметилен и их изомерные формы с боковой целью.-- Примерами алкилена с 1-8 атомами углерода, замещенного 1-3 атомами фтора, являются 2-фто-рэтий, 2-фторбутил, .торбутил, б-фторшентнл, 4-фтор-4-метилпе:нтил, З-фторизогептил78-ф1:ороктил, 3,4-дифторбутпл, 4,4дифторпентил и 5,5,5-трифторпентил.
Алкилен с 1-8 атомами углерода, замещенный 1 или 2 атомами фтора, имеет формулы:
-CHaCHF-, -СНгСРг-, -СНзСНаСНРСНа-, -СНгСНзСНгСРг-,
-СНгСНСНаСНР-,
-СНгСНаСНгСНРСНР-,
-СН2СН2СН2СН2СН2СНР-,
СН2СН2СН2СН2СН2СР2,
-СН2СН2СН2СР2СН2СН2СН2-, -СН2СН2СН2СН2СН2СН2СН2СР2
Полученные аналоги простагландина EI являются новыми физиологически активными веществами, которые по сравнению с известными естественным простагландиеом EI обладают более ценными свойствами.
Соединение формулы IV получают путем взаимодействия соединения общей формулы
/V
CnH2rrCOORt
..Н
- -С(080г115)4 (оЗОгЯбЖг з
в экзоконфигурации относительно группы -С {OS02R5)R4-C(OS02R5)R2R3
где R2, Ra, R4 Ri CnH2n имеют вышеуказанные значения,
Rs - ал-кил с 1-5 атомами углерода, с водой при температуре О-60°С. В случае значения , процесс ведут в присутствии инертного органического растворителя, растворимого в воде, например ацетона.
Пример 1. Метиловый эфир dl-простагландина EI и метиловый эфир dl-15-изo|пpoстагландина Ej.
|СпНгп СооЯт н
-C(OH)R4-C(OH)R2R3 И
А. Раствор 509 мг более полярного изомера (а-боковая цепь, R7 CH3) и 9 мл пиридина охлаждают до 0°С и обрабатывают 1,3 мл хлорангидрида метансульфокислоты. Через 1 час выдержки при 0°С ледяную баню удаляют и смесь перемешивают еще 1 час. Затем снова охлаждают до 0°С, добавляют лед и экстрагируют хлористым метиленом. Экстракт промывают холодной разбавленной соляной кислотой, сушат и упаривают. Этот остаток неочищенного димера дает одно пятно TLC и показывает УФ поглощение при 1740, 1350, 1175 и 910 сж и основные пики ио-на в масс-спектре при 332 (М-2СНз5ОзН), 301 (332-32) и 330 (332-32). Остаток очень нестоек при обычной очистке хромато-графией. Остаток растворяют в 27 мл ацетона и разбавляют 13,5 мл воды. Полученный раствор выдерживают при 25°С б час. Смесь концентрируют под вакуумом, экстрагируют хлористьш метиленом, эк1стракт . промывают, высушивают и упаривают. Хроматография на 50 г силикагеля и элюировани-е все большими концентрациями этилацетата в Скеллизольве-В дает следующие материалы: А-75 мг неизвестных, м-енее полярных продуктов; В-389 мг смеси двух мономезилатов гликоля; С-27 мг (5,3%) К-изомера метилового эфира ё/-15-изопростагландина EI и D-35 мг (6,7%) кристаллического метилового эфира dl-простагландина Е (изомер S).
Фракция В двух мономезилатов характеризуется следующим: ясные ионы в масс-спектре при 350 (М-СНзЗОзН); 332 (350-18), 301 (323-31), 300 (332-32), 319 (350-31), 318 (350-32). ИФ-поглощение нри , 1745, 1340, 1170 и 920 CM-i и в НМР-спектре один протон в виде широкого мультиплета 5,0-4,66, 3 -протон синглет при 3,76 (СНз), один протон в виде дублета дублетов 3,416 ,5 и 3,5 ops 3- протон сииглет при 3,16 (S-СНз) и водород 6-эндоциклоПропила в ввде мультиплета 0,85-0,56.
Фракция метилового эфира dl-15-изонроста.нгландина EI имеет ИФ и НМР-опектры одинаковые с опти чески активным метиловым эфиром 15(R)-nrEj. Масс-спектр показывает молекулярный ио« 368 и другие ясные ионы при 350, 332, 297 единиц массы.
Фракция D была перекристаллнзована из смеси эфир - Скеллизольв-В, т. пл. 55-57°С. НМР и ИФ-спектры и JLC одинаковы с таковыми для метилового эфира природного ПГЕь Масс-спектр показывает пики при 368, 350, 332 и 297 масс единиц и поглощение в УФ-области при 278 ммк (е-26000) после добавления небольшого количества 50%- НОГО водного раствора КОН к образцу в метаноле.
Вычислено для С21НзбО5%: С 68,44; И 9,85.
Найдено, %: С 68,07; Н 9,92.
B.Менее полярный эритроизомер структуры VI (а-бо;ковая цепь, Н7 СНз), обработанный как указано выше, дает 5% метилового эфира dl-nPEi и такое же количество его 15-Э(пимера.
C.Более -полярный треоизомер структуры VI («-боковая цепь, Н7 СНз) дает 5% метилового эфира dl-nPEi и 5,5% его 15-эпимёра.
D.Аналогичным образом, как описано выше, смесь моном-езилатов, полученная в результате указанных реакций сольволиза, превращается в бисмезилаты и сольволизируется, давая с 5%-.ным выходом метиловый эфир. dl-nrEi и такое же количество его 15-эпимера.
Пример 2. dl-Праста.гландин Е.
К высушенному образцу 329 мг кислотного гликоля («-боковая цепь, R7 H), состоящему из более полярного эритро- и треоизомеров добавляют 20 мл хлористого метилена, 3,3 мл трихлорэтанола, 1,8 мл пиридина и затем 0,33 г дицнклогексилкарбодиимида. После перемешивания в течение 2 часов при 25°С
всю реакционную смесь заливают в колонку
со 100 г силикагеля. Элюирование 2 л 25-
75%-ной смеси этилацетат-Скелли-В дает
300 мг желаемого р,р,р-трихлорэтилового эфира, 6-экзо-(Г,2 - дигидроксигептил)-2а-(6 карбоксигексил) - бицикло (3,1,0)-гекса«-3-о«а
(VI, сс-боковая цепь), немного загрязненного
кристаллической дициклогексилмочевиной.
Этот материал имеет 2-протонный сияглет при
4,76 для протонов трихлорэтилгруппы и в остальном аналогичен соответствующему метиловому эфиру формулы VI, а-боковая цепь, .
300 мг полученного трихлорэтилового эфира
гликоля в 7,5 мл пиридина обрабатывают при 0°С под азотом 0,8 мл хлорангидрида метансульфокислоты. После 5 мин выдержки при 0°С реакционной массе дают нагреться до комнатной температуры и перемешивают
2 час. Затем снова охлаждают льдом и добавляют 5 мл воды. После перемешивания в течение 5 мин. при 0°С добавляют этилацетат и дважды промывают водой, дважды 1 н. соляной кислотой, затем бикарбонатом натрия
и упаривают. Остаток 348 кг, согласно хроматографии в тонком слое, состоит главным образом из материала менее полярного чем исходный гликоль.
К остатку приливают 8 мл ацетона и 2 жл
воды и выдерживают при 5°С под азотом,в течение 68 час. Затеем вносят воду, ацетон удаляют под вакуумом и продукты экстрагируют этилацетатом. Экстракт промывают бикарбонатом, насыщенным раствором соли, сушат над сульфатом натрия и упаривают, вес очищенного остатка 315 Л1г. Хроматография на 50 г силикагеля и элюирование 1 л 25100% смеси этилацетат-Скелли-В и затем 5%-ной смесью метанол - этилацетат дает
четыре пика.
Фракции № 9-15 и № 17-26 состоят из мономезилатов. ИФ-спектры их очень сходны, ОН (3500 CM-i); С О (1745 см-i); 1340,
1170, 920, 800, 720 сж-1.
Фракция № 32-40 на TLC несколько быстрее, чем метиловый эфир 15-изоПГЕ и состоит из его соответствующего трихлорэтилового эфира.
Фракция № 43-47 (12 мг), движется на TLC немного быстрее, чем метиловый эфир nrEi и показывает в НМР-спектре два олефиновых протона при 5,656; два протона трихлорэтиловой эфирной группы в виде синглета при 4,766 и в остальном совпадает с трихлорэтиловЫм эфиром ПГЕ.
Аналогичным о,бразом 200 мг менее полярных эритро-треогликолей структуры VI (а-боковая цепь, ), превращают в трихлорэтиловые эфиры, бимезилаты и сольволизируют. Получают 8,5 мг трихлорэтилового эфира dl-nPEi, идентичного вышеописанному.
Фракцию № 43-47 (12 мг) растворяют в 1 мл 90%-ной уксусной кислоты и перемещиTLC не покажет отсутствие эфира. Добавляют этилацетат и раствор декантируют в разделительную, воронку, и промывают несколько раз водой, затем насыщениым раствором соли, сушат «ад сульфатом натрия и упаривают. Остаток хроматог.рафируют на 3 г силикагеля, элюируя 50, 75, 100%-ной смесью этилацетат-Окелли-В и 5%-:ной смесью метанолэтнлацетат.
Фракция № 7-9 большей частью кристаллическая, движется на TLC, как ПГЕь и после перекристаллизации из смеси этилацетат-Скелли-В плавится при 113,5-115°С, вес 3,4. мг. Точка плавления смеси с природным ПГЕ (т. пл. 114-115) 109-104°С.
Кривая рассеяния оптического вращения не показывает оптической активности между 475 и 230 ммк (0,001°) и масс-спектр идентичен со спектром природного nPEi в двух системах.
Выделенные мономезилатиые фракции предыдущего опыта (205 мг) ремезилируют и сольволизируют как указано выше и фракции трихлорзтилового эфира dl-nPEi ( мг гидролизируют цинком с уксусной кислотой. Получают еще 2 мг dl-HrEi, т. пл. 113- 115°С, общий выход чистого dl-nrE 5,4 мг или 1,6% от всей гликолевой кислоты.
Пример 3. 8-Изопростагла.ндин ЕЬ К 1,2 г 6-экзо-(Г-г «с-гептенил)-2р-(6 -карбоксигексил) -бицикло(3.1.0)-гексан-3-она под азотом добавляют холодный раствор (0°С) 325 мг бикарбоната натрия и 0,1 мл 90%-ной перекиси водорода в 25 мл 98%-ной муравьиной кислоты. Посл-е получасового перемешивания при 0°С ледяную баию удаляют и перемешивают еще 1,5 час, муравьиную кислоту удаляют под вакуумом и .приливают25 лм беезола, который также удаляют под вакуумом. Остаток экстрагируют этилацетатом, экстракт промывают водой и насыщенным раствором соли, сущат сульфатом натрия и упаривают.
К остатку приливают 45 мл метанола и 15 мл .насыщенного водного раствора бикарбоната натрия. Смесь перемешивают при 25°С 2 час, концентрируют в вакууме для удаления метанола и подкисляют до рН 2-3, Продукты экстрагируют этилацетато-м, экстракт промывают водой, сушат и у1паривак)т. Остается 1,38 г смеси эпимерных кислот гликоля VI, (р-боковая цепь, ). Их этерифицируют в 140 мл хлористого метилена с 23 м.л трихлорэтанола, 12,6 мл пиридина и 2,31 г дициклогексилкарбадиимида при 25°С в течение 2 час. Остаток растворяют в бензоле, фильтруют для удаления дициклогексилмо-чевины и хроматографируют на 150 г силикагеля.
Элюирование 20 100%-ным этилацет-атом (в Скеллизольве-В) дает большие пики, соответствующие эпимерным гликолям структуры vn
n zn-cooR-T
/о,
CR -СКеЕз
(р-боковая цепь, К7 СН2СС1з). Менее полярный (700 мг} показывает одно пятно, TLC (силикагель, 50% этилацетатциклогексан), более полярный (800 мг показывает два очень близких пятна в той же системе. Величины R( этих трихлорэтиловых эфиров аналогичяые, IHO 1не;око1ЛЬко больше чем R{ соответствующих указанных выше метиловых эфиров.
К 667 м.г менее полярного гликоля формулы VI (р-боковая цепь, К7 СН2СС1з) добавляют 16,5 мл пиридина и затем при 0°С 1,67 МА хлорангидрида метансульфокислрты.
Смесь перемешивают 10 мин при 0°С и 1 - час
после удаления ледяной бани. Затем снова
охлаждают до 0°С, приливают 15 мл воды и смесь экстрагируют этилацетатом. Экстракт промывают несколько раз холодной разбавленной соляной кислотой, водным раствором бикарбоната натрия, сушат и упаривают.
Неочищенный бисмезилат перемещивают в течение ночи с 53 мл ацетона и 26 мл воды при 25°С под азотом. Затем концентрируют в вакууме, экстрагируют этилацетатом, экстракт промывают, сущат и упаривают. Остаток
хроматографируют на 75 г силикагеля и
элюируют увеличивающимися количествами
этилацетата, растворенного в Скеллизольве-В.
После двух главных пиков материала 276
и 103 мг, неперегруппированпых мономезилатов гликоля, алюируют 34 мг трихлорэтилового эфира 8-изопростагландина ЕЬ показывав щего два олефиновых протона между 5,0 и 6,06 (Hi3 -при 5,286, и 9,5 cps и Нн при 5,76, J 15 и 7 cps); два протона трихлорэтиловой группы в виде синглета 4,86; два карбинольных протона в виде мультиплета между 3,9 и 4,56. За этим следует 12 мг. трихлорэтилового эфира простагландина Ei, НМР-С;пектр которого идентичен спектру, полученному выще.
34 мг трихлорэтилового эфира 8-изопрОстагландина Ei растворяют в 1 мл 90%-ной уксусной кислоты и перемешивают со 100 мг цинковой пыли 2 час, затем разбавляют этилацетатом, промывают несколько раз водой, сушат и упаривают. Остаток хроматографируют на 5 г Силикар-СС4 (Маллинкродт, промытый кислотой силикагель) и элюируют 50-100%-.ным этилацетатом и Скеллизольвом-В.
Фракции по TLC подвижности, соответствующие 8-изопростагландину EI в системе А (15 мг) объединяют и кристаллизуют из смеси этилацетат-Скелл«80льВ-В, т. пл. 101
Материал не показывает оптического вращения между 475 и 230 ммк и НМР и маос-опектры идентичны спектрам «природного изомера.
Вычислено для С2оНз405%: С 67,7; Н 9,67.
Найдено, %: С 67,56; Н 9,60.
Предмет изобретения
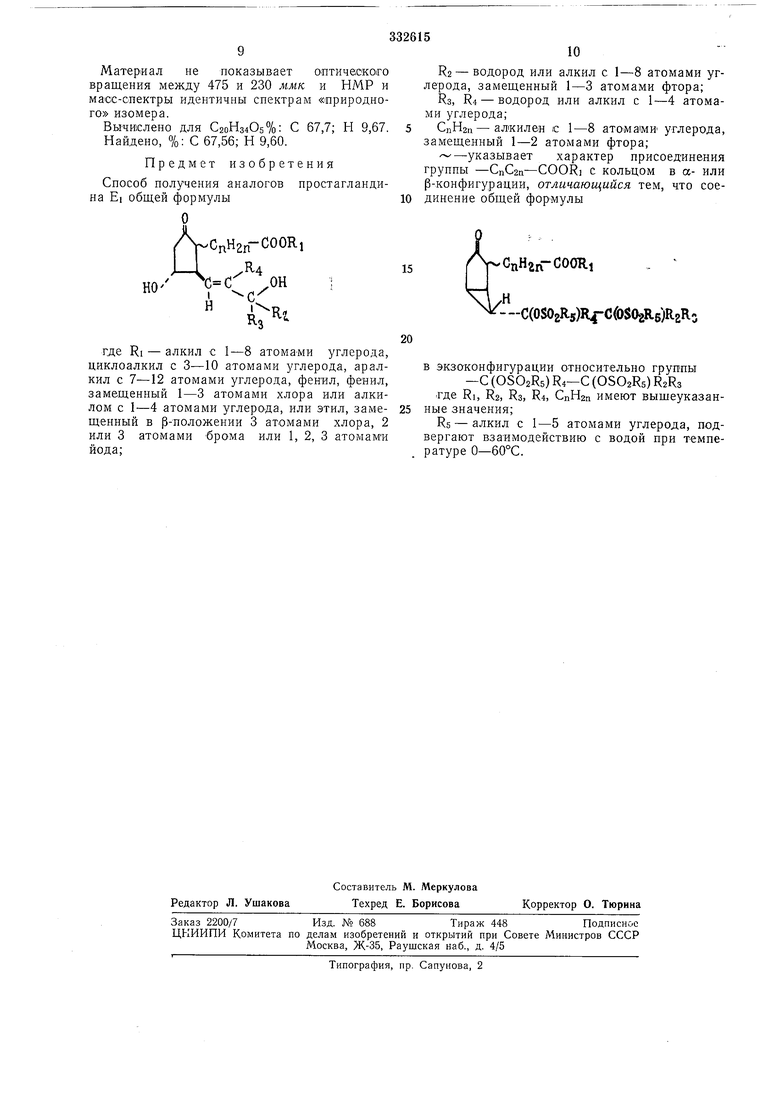
Способ получения аналогов простагландина EI общей формулы
НО
где RI - алкил с 1-8 атома-ми углерода, циклоалкил с 3-10 атомами углерода, аралкил с 7-12 атомами углерода, фенил, фенил, замещенный 1-3 атомами хлора или алкилом с 1-4 атомами углерода, или этил, замещенный в р-положении 3 атомами хлора, 2 или 3 атомами брома или 1, 2, 3 атомами йода;
R2 - водород или алкил с 1-8 атомами углерода, замещенный 1-3 атомами фтора;
Ra, R4 - водород или алкил с 1-4 атомами углерода;
СпН2п-алкилен с 1-8 атомами углерода, замещенный 1-2 атомами фтора;
-указывает характер присоединения группы -СпС2п-COOR с кольцом в а- или р-конфигурации, отличающийся тем, что соединение общей формулы
СпНггх сооя1
15
-C(OS02R5)R4-C i S02R5)RER:
20
в экзоконфигурации относительно группы -С (OSOaRs) R4-С (OSOzRs) R2R3
где RI, R2, Rs, R4, СпНзп имеют вышеуказанные значения;
Rs - алкил с 1-5 атомами углерода, подвергают взаимодействию с водой при температуре О-60°С.



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АНАЛОГОВ ПРОСТАГЛАНДИНА Ф, | 1971 |
|
SU307562A1 |
| ВСЕСОЮЗНАЯ I;^|Т1-ЕГг^"^-"'Т^-^'Т'''': а?^.мл i 4,si i 1?ы ;!,.'i(i.j .i-.-iif::-^- | 1972 |
|
SU331539A1 |
| СПОСОБ ПОЛУЧЕНИЯ АНАЛОГОВ ПРОСТАГЛАНДИНА А | 1972 |
|
SU327669A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ПРОСТАГЛАНДИНОВ А | 1973 |
|
SU399108A1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНОГО ЭФИРА ДЕЗАЦЕТОКСИЦЕФАЛОСПОРИНА | 1972 |
|
SU352464A1 |
| СПОСОБ ПОЛУЧЕНИЯ НОВЫХ АНАЛОГОВ ПРОСТАГЛАНДИНА Fs | 1972 |
|
SU359805A1 |
| СССРОпубликовано 28.XI 1.1972. Бюллетень N° 5за 1973Дата опубликования описания 30.VIII.1973УДК 547.6iS9.6.07(C.S8.8) | 1973 |
|
SU365067A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ Дз- ИЛИ Д^-ФЕНИЛ- ЦИКЛОГЕКСЕНОВЫХ КИСЛОТ | 1970 |
|
SU269807A1 |
| СПОСОБ ПОЛУЧЕНИЯ ОПТИЧЕСКИ АКТИВНЫХИЛИ РАЦЕМИЧЕСКИХ КИСЛОТ ИЛИ ИХ ЭФИРОВ15-АЛКИЛ-ПРОСТАГЛАНДИНОВ F | 1971 |
|
SU416939A3 |
| СПОСОБ ПОЛУЧЕНИЯ3- | 1972 |
|
SU340173A1 |


Авторы
Даты
1972-01-01—Публикация