Изобретение относится к получению новых замещенных 2-азабициклоалканов.
Использование известной реакции замещения водорода на тиоэфирную группу позволило получить новые соединения, обладающие высокой гербицидной активностью.
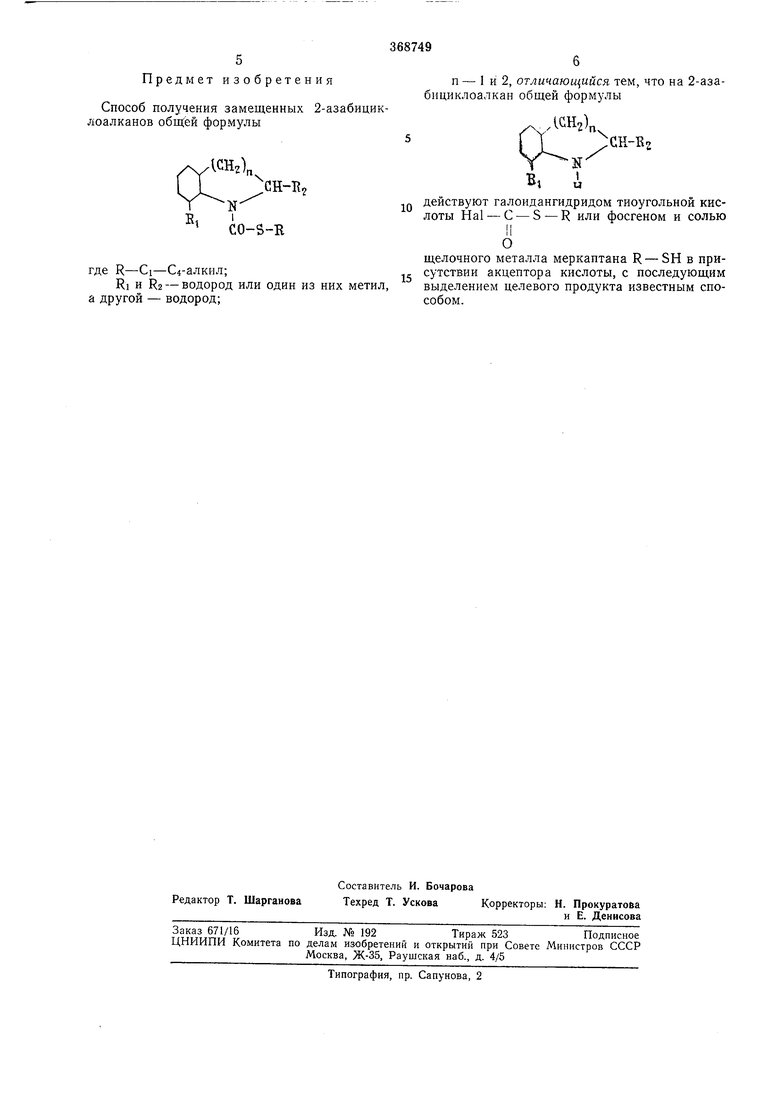
Предлагаемый способ получения замещенных 2-азабициклоалканов общей формулы
1СН,)„
сс
,
CO-S-R
где R - Ci-С4-алкил;
RI и Нг - водород или один из них метил, а другой - водород;
п - 1 и 2,
заключается в том, что на 2-азабициклоалкан общей формулы
сн,)„
СН-Вг
NI Н
действуют галоидангидридом тиоугольной кислоты Hal-С-S-R или фосгеном и солью
6
щелочного металла меркаптана R - SH в присутствии акцептора кислоты, с последующим выделением целевого продукта известным способом. Если в качестве акцептора кислоты применяют органические основания, например
третичные амины, то целесообразно вести процесс в среде органического растворителя. При использовании неорганических оснований пригодны вода и водные смеси органических растворителей, смешивающихся с водой. Кроме
того, акцептором кислоты может служить избыток 2-азабициклоалкана.
Пример 1. К раствору 45 г транс-д,екагидрохинолина в 200 мл петролейного эфира
приливают по стенке колбы раствор 13 г гидроокиси натрия в 100 .лгл воды. К этой смеси, сильно перемещивая и охлаждая ее (10- 15°С), прибавляют по каплям 40,5 г этилового эфира хлортиомуравьиной кислоты. По окончании реакции смесь перемещивают 30 мин, разделяют фазы, промывают органическую фазу до нейтральной реакции, высущивают и отгоняют петролейный эфир в вакууме. Остаток дистиллируют в вакууме и получают 65 г
1-(этнлтиокарбонил) - гранс-декагидрохинолина, бесцветное масло; / о i 5315; т. кип. ПО- 116°СуО,01 лш.
Пример 2. При обработке раствора 45 г транс-декагидрохинолина в 200 мл петролейного эфира и раствора 13 г гидроокиси натрия в 100 мл воды 32 г фосгена при постоянном перемешивании и охлаждении до -5-0°С получают после отделения органической фазы транс - декагидрохинолин - N - карбоксихлорид. Этот промежуточный продукт обрабатывают в петролейном эфире водным раствором 27 г этилмеркаптида натрия и получают 61 г бесцветного масла. Константы продукта такие же, как у продукта, приведенного в примере 1.
Пример 3. В раствор 13,9 г транс-д,екагидрохинолина и 4 г гидроокиси натрия в 200 мл 50%-него водного этанола при постоянном перемешивании и температуре О-5°С вводят 6,1 г сероокиси углерода. Через 0,5 час после окончания реакции прибавляют по каплям 11 г этилбромида и перемешивают 5 час при 25°С. Удаляют этанол в вакууме и обрабатывают остаток метиленхлоридом. После разделения смеси получают 15 г коричневатого масла, как в примере 1.
Пример 4. К раствору 16,7 г i uc-декагидрохинолина в 200 мл петролейного эфира приливают по стенке колбы раствор 4,8 г гидроокиси натрия в 50 мл воды. При сильном перемешивании и охлаждении до 5-10°С прибавляют по каплям 16,6 г S-изопропилового эфира хлортиомуравьиной кислоты. По окончании реакции перемешивают еще 8 час при комнатной температуре, разделяют фазы, промывают органическую фазу до нейтральной реакции, высушивают и выпаривают петролейный эфир в вакууме. Масло дистиллируют в высоком вакууме и получают 20 г 1-(изопропилтиокарбонил) -4{ыс-декагидрохинолина, бесцветное масло т. кип. 102-107°С/0,05 мм.
Пример 5. К раствору 109 г декагидрохинальдина в 750 мл бензола после добавления 72 г триэтиламина при 5-10°С прикапывают 88 г S-этилового эфира хлортиомуравьиной кислоты. Перемешивают 5 час при комнатной температуре, отсасывают хлоргидрат триэтиламина, промывают осадок бензолом и выпаривают фильтрат в вакууме. Желтоватое масло дистиллируют в вакууме и получают 115 г 1-(этилтиокарбонил) - 2 - метилдекагидрохинолин, бесцветное масло, т. кип. 108-120°С/ /0,02 мм.
Пример 6. При взаимодействии растворов 15 г декагидрохинальдина в 200 мл эфира и 4 2 гидроокиси натрия в 50 мл воды с 10 г фосгена при перемешивании и охлаждении до -5-0°С получают эфирный раствор 1-хлоркарбонил-2-метилдекагидрохинолина, который перемешивают с водным раствором 8,4 г этилмеркаптида натрия при комнатной температуре. После разделения получают 16 г почти
бесцветного масла, т. кип. 108-120°С/0,02 мм.
Пример 7. Постоянно перемешивая, при
температуре О-5°С в раствор 15 г декагидрохинальдина и 4 г гидроокиси натрия в
200 мм 50%-него водного этанола вводят 6,5 г сероокиси углерода.
Через 1 час подогревают до 20-25°С и добавляют 13,7 г н-бутилбромида. Перемешивают 10 час при комнатной температуре, удаляют этанол в вакууме. Образовавшееся масло после обработки метиленхлоридом и удаления растворителя дистиллируют в вакууме. Получают 14 г 1-(н-бутилтиокарбонил)-2-метилдекагидрохинолина, бесцветное масло, т. кип.
125-127°С/0,01 мм.
Пример 8. К раствору 12,2 г 8-метилдекагидрохинолина в 150 мл диэтилового эфира добавляют при перемешивании раствор 3,2 г
гидроокиси натрия в 50 м-л воды, охлаждают до О-5°С, добавляют по каплям при сильном перемешивании 11,1 г S-изопропилового эфира хлортиомуравьиной кислоты. Перемешав 12 час при комнатной температуре, разделяют
фазы, промывают эфирную фазу до нейтральной реакции, выпаривают эфир в вакууме и получают коричневатое масло, которое дистиллируют в вакууме. Получают 15 г 1-(изопропилтиокарбонил) - 8-метилдекагидрохинолина,
бесцветное масло, т. кип. 104-10б°С/0,01 мм.
Пример 9. К раствору 80 г октагидроиндола в 1500 мл бензола при перемешивании и охлаждении льдом добавляют по каплям 65 г
триэтиламина, затем 79 г S-этнлового эфира хлортиомуравьиной кислоты. По окончании реакции перемешивают 8 час при комнатной температуре, отсасывают хлоргидрат триэтиламина, промывают осадок бензолом и выпаривают бензольный раствор в вакууме. Масло дистиллируют в вакууме и получают 100 г 1-(этилтиокарбонил)-октагидроиндола, т. кип. 98-10 ГС/0,1 мм.
Пример 10. Постоянно перемешивая и охлаждая до , смесь растворов 12,5 г октагидроиндола в 200 мл эфира и 4 г гидроокиси натрия в 100 мл воды обрабатывают 10 г фосгена. Выделенный октагидроиндол-Nкарбоксихлорид обрабатывают в эфире водным раствором 8,5 г этилмеркаптида натрия. Получают 14 г бесцветного масла, аналогичного маслу, полученному в примере 9.
Пример 11. В раствор 13,9 г 2-метилоктагидроиндола и 4 г гидроокиси натрия в 200 мл 50%-ного водного этанола при постоянном перемешивании и температуре О-5°С вводят 6,5 г сероокиси углерода. Перемешивают 30 мин при 15-20°С и добавляют 12,5 г н-пропилбромида. Перемешивают 15 час, удаляют этанол в вакууме и прибавляют к образовавшемуся маслу метиленхлорид. Растворитель отгоняют в вакууме и получают 15 г 1-(н-пропилтиокарбонил) - 2 - метилоктагидроиндола, бесцветное масло, т. кип. 102-104°С/0,005 мм. 5 Предметизобретения Способ получения замещенных 2-азабициклоалканов общей формулы tcvn ЛГ I 1 . JJI CO-S-R где R-Ci-С4-алкил; RI и R2 - водород или один из них метил, а другой - водород; 6 n - 1и2, отличающийся тем, что на 2-азабнциклоалкан общей формулы . (СН) :сн-Ег 1 1 Действуют галоидангидридом тиоугольной кислоты Hal - С - S - R или фосгеном и солью 11 щелочного металла меркаптана R - SH в присутствии акцептора кислоты, с последующим выделением целевого продукта известным способом.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 2-АЗАБИЦИКЛОАЛКАНОВ | 1972 |
|
SU357727A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПИРРОЛА ИЛИ | 1973 |
|
SU368748A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ п- | 1973 |
|
SU382285A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 0-АНИЛИНО- ФЕНИЛЭТИЛОВЫХ СПИРТОВ | 1973 |
|
SU381217A1 |
| СПОСОБ ПОЛУЧЕНИЯ АМИДОВ АРИЛОКСИАЛКАНОВЫХ ИЛИ АРИЛТИОАЛКАНОВЫХ КИСЛОТ12 | 1973 |
|
SU385440A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛОВЫХ ЭФИРОВ НЕНАСЫЩЕННЫХ КИСЛОТ | 1968 |
|
SU207827A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКАЛОИДОВ | 1973 |
|
SU372813A1 |
| В П Т Б | 1973 |
|
SU393825A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ЦИКЛОГЕПТЕНА | 1973 |
|
SU383288A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАЛКИЛАМИНОЭТИЛОВЫХ ЭФИРОВ | 1968 |
|
SU218756A1 |


Авторы
Даты
1973-01-01—Публикация