Изобретение относится к синтезу новых эфиров хлоралкилтиолфосфорной кислоты общей (юр мулы { П ОЛч cfcH-0-pC VRg R, Кз R4 О где RI, R2, Rs, R4 - водород, алкил, галоидалкил; или 1; R5 н RG - алкил, галоидалкил, циклоалкил, незамещенный или замещенный галоидом, нитро- ИЛ.И ме.ркалтогруппой, фенил; Y - кислород или сера, Y г О, если Re - алкил пли циклоалкил, которые могут найти нримененпе в качестве физиологически активных веществ. Общеизвестно получение разнообразных эфиров фосфорной кислоты взаимодействием галоидангидридов фосфорной кислоты со спиртами, меркаптанами и феноламп. Однако для синтеза вышеназванных соедпнен1ий указанный .спо-соб «е применяют. Предлагаемый способ состоит в том, что хлорангидрид хлоралкилтиолфосфорной кислоты подвергают взаимодействию со спиртом, пли меркаптаном, или тиофенолом, или фенолом. Процесс лучше вести при температуре 20-100°С в среде органического растворителя, папример бензола. Пример 1. К суспензии 160 г (1 моль 4-нитрофенолнатрия в 200 мл ацетонитрнла по каплям добавляют 223 г (1 моль) хлорангидрида диэфира 0- 3-хлорпропил-(2)-5-метилтполфосфорной кислоты и смесь нагревают в течение 12 час с обратным холодильником. Затем реакционную смесь охлаждают, выливают в ледяную воду, экстрагируют бензолом, органическую фазу промывают насыщенным раствором бикарбоната натрия и сушат. После отгонки бензола нри нониженном давлении в виде маслянистого вещества остается 204 с (63%) эфира 0- :1-хларфенИЛ-(2)-5-метил-4(4-пптрофенил) -тиолфосфорной кислоты. Вычислено, %: Р 9,5; N 4,3. CioHisClNOsPS. Найдено, %: Р 9,2; N 4,1. Мол. вес 326,5. Пример 2. Суспендируют 175 г (1 моль) З-метил-4-метилмеркаптофенолнатрия в 600 л/л ацетопитрила и ло каплям добавляют к получепной суспензии 223 г (1 моль) хлорангидрида эфира 0- 3-хлорПроп.ил-(2)-5-метилт«олфосфорной кислоты. Затем смесь 3 час нагревают до кипения, охлаждают, выливают в ледяную воду и экстрагируют бензолом. Органическую фазу отделяют, промывают ее насыщенным раствором бикарбоната натрия, бензольный раствор С)шат и бензол отгоняют под пониженным давлением. Остается 200 г (59%) эфира 0- 3-хлорпропил-(2)-5-метил-0-(3-метил-4-метилмеркапто) -тиофосфорной кислоты в виде вязкого масла.
Вычислено, %: Р 9,1; S 18,8.
CisHieCIOaPS.
Найдено, %: Р 8,7; S 19,0.
Мол. вес. 340,5.
Пример 3. Реагирует 175 г (1 моль З-метил-4-метил-меркантофенолнатрия и 209 г (1 моль) хлорангидрида диэфира 0-{2-хлорэтил-5-метилтиолфосфорной кислоты, как в примере 1. Получают 220 г (67%) эфира 0-(2хлорэтил) -S-метил-О- (3 - метил-4 - метилмер капто)-тиолфосфорной кислоты с т. кип. 128- 13,0°С/1 мм рт. ст.
Пример 4. Аналогично примеру 2 получают по реакции 160 г (1 моль) 4-нитрофенолнатрия и 209 г хлорангидрида диэфира (1 моль 0-(2-хлорэтил)-5-метилтиолфосфорной кислоты 160 г (51%) эфира 0-(2-хлорэтил) -S-метил-О- (4-нитрофенил) -тиолфосфорной кислоты.
Вычислено, %: N 4,5; S 10,3. CgHiiClNOsPS. Найдено, %: N 4,8; S 9,6. Мол. вес 311,5.
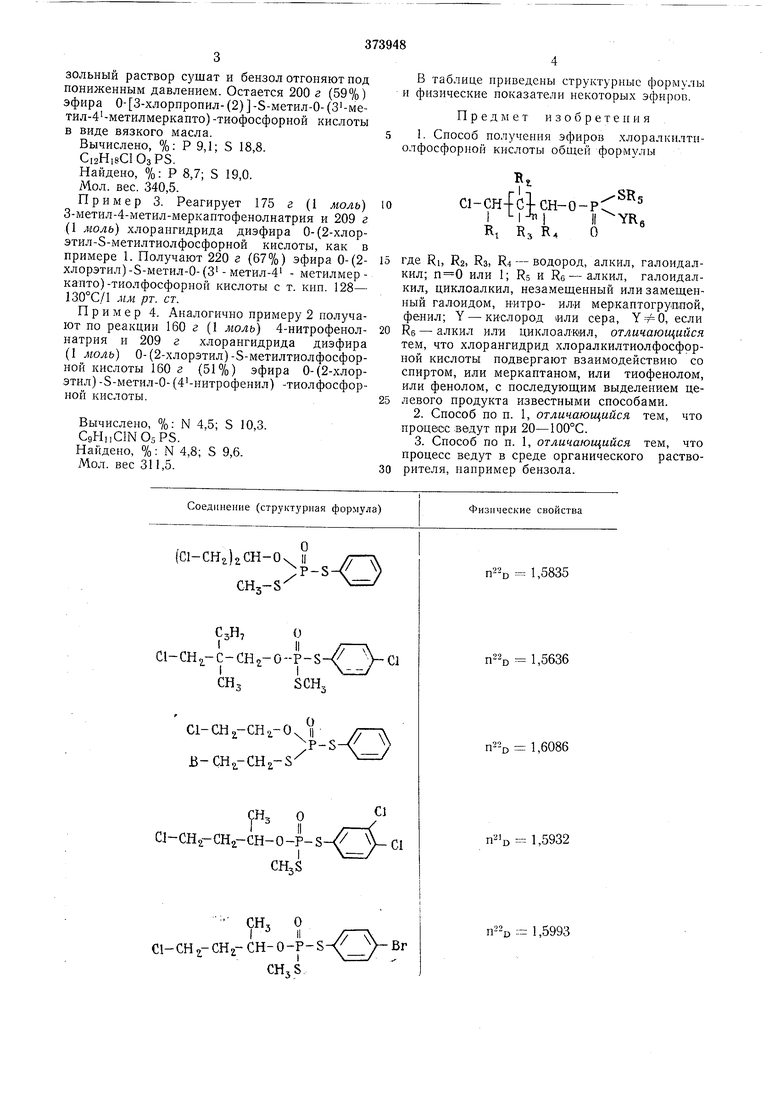
Соединение (структзрная формула)
В таблице приведены структурные формулы и физические показатели некоторых эфиров.
Предмет изобретения
1. Способ получения эфиров хлоралкилтполфосфорной кислоты общей формулы
-SR.
Cl-CH-fc -CH-0-pC
I 4-bi|II YR,
RI RS Кч
О
где Ri, R2, Нз, R4 - водород, алкил, галоидалкил; или 1; Rs и Re - алкил, галоидалкил, циклоалкил, незамещенный или замещенный галоидом, НИтро- или меркаптогруплой, фенил; Y - кислород «ли сера, , если
Re - алкил или циклоалкил, отличающийся тем, что хлорангидрид хлоралкилтиолфосфорной кислоты подвергают взаимодействию со спиртом, или меркаптаном, или тиофенолом, или фенолом, с последующим выделением целевого продукта известными способами.
2.Способ по п. 1, отличающийся тем, что процесс ведут при 20-100°С.
3.Способ по п. 1, отличающийся тем, что процесс ведут в среде органического растворителя, например бензола.
Физические свойства
(Cl-CH j CH-O
P-S
GHj-S
1,5835
СзБ,О
III //
CH,-C-CH2-0--P-S- /
II
СНзSCH
0
CH.,-CHi-0
il
P-S
CH2,-CH2-S
- 1,5636
y
n-- D 1,6086
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВНОЗАМЕЩЕННЫХ АЛКИЛОВЫХ ЭФИРОВ ТИОЛКАРБАМИНОВОЙ КИСЛОТЫ | 1971 |
|
SU419025A3 |
| Способ получения -тиопропионами-дОВ или иХ КиСлОТНО-АддиТиВНыХСОлЕй | 1978 |
|
SU803859A3 |
| СПОСОБ ПОЛУЧЕНИЯ АМИНОКЕТОНОВ | 1974 |
|
SU440826A1 |
| Способ получения -замещенных эфиров или тиоэфиров -хлорметилкарбаминовых кислот | 1972 |
|
SU443510A1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОСФОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ | 1974 |
|
SU440843A1 |
| ГЕРБИЦИДНЬШ СОСТАВ | 1972 |
|
SU354627A1 |
| СНОСОВ ПОЛУЧЕНИЯ сложных ЭФИРОВ ЦИКЛОНРОНАНКЛРБОНОВОЙ КИСЛОТЫ | 1973 |
|
SU372810A1 |
| Способ получения производных нафтиридина или их стереоизомеров или их солей | 1977 |
|
SU655314A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ КЕТОТИОЛФОСФИПОВЫХКИСЛОТ | 1970 |
|
SU284988A1 |
| Способ получения бензиламинооксазолинов или их солей или их оптических изомеров | 1975 |
|
SU578880A3 |

СНз 0
ci-cH -CH-.-cH-o-p-s- / Vci
0
H,
СН,-СНг-СН-0-Р-5Ч
п21о - 1,5932
п2-о :- 1,5993
7 V
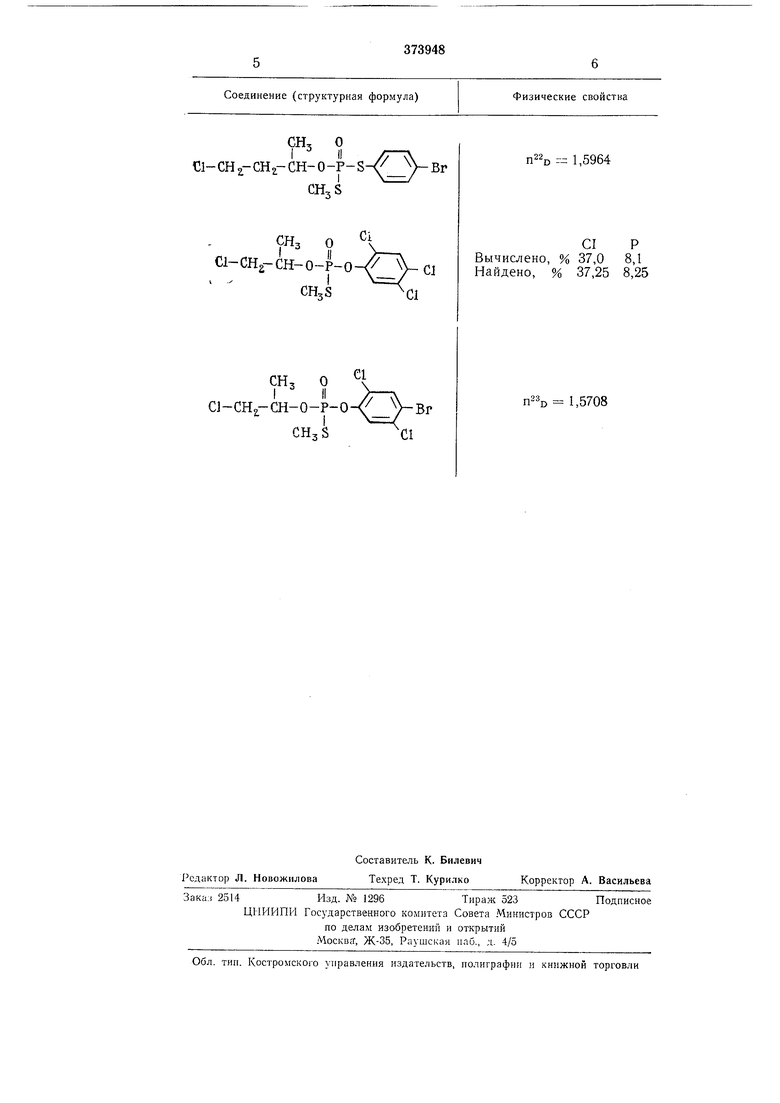
Соединение (структурная формула)
сн, о
Cl-CHo-CH,-CH-0-F-S-( V-Br
Физические свойства
П22о г 1,5964
СНз о Cl-CH -CH-0-P-O
CHgS
CI Р
Вычислено, % 37,0 8,1 Найдено, % 37,25 8,25
сн.
о
Cl-Cm-CH-O-P-O-//
CH,s
1,5708
Вг
Cl
Авторы
Даты
1973-01-01—Публикация