1
Изобретение относится к области получения новых гетероциклических соединений, которые могут найти применение в фармацевтической промышленности.
Использование известной реакции алкилирования привело к получению дигидро-3-(1-замещенный - 4-окси-4-пиперидил)-2 (ЗН)-фуранона, обладающего его высокой биологической активностью.
Предлагается снособ получения дигидро-3(1-замещеннь Й-4-окси-4-пиперидил) -2 (ЗН) -фуоанона обпдей формулы (1)
НО
К-СНг-СЯг
(I)
где RI-водород или низщий алкил;
Rg - водород, фтор, хлор, бром, низшая алкил-, алкокси- или алкилтиогруппа, циано-, м-амино, р-амипо- или трифторметилгруппа или остаток - NHCORa,
где R3 - низшая алкилгруппа,
или их солей.
Способ заключается
в том, что соединения общей формулы (II)
НО
М
(В
Q
где RI имеет указанное значение, конденсируют с соед1П ен)ем общей формулы (III)
Х-СНг-СН2-
где R2 имеет указанные значения;
X - кислотный остаток реакционноспособпого сложного эфира. Процесс ведут в среде инертного растворителя в присутствии связывающего кислоту агента.
В качестве инертного растворителя можно хпотреблять, например, ароматические углеводороды (бензол, толуол или ксилол), ди (низщий) алкиламиды низших алифатических монокарбоновых кислот (диметилформамид) или хлорированные алифатические углеводороды (хлороформ или тетрахлорметан). Как связывающие кислоту средства можно использовать, например, карбонаты щелочного металла (карбонаты калия или натрия), третичные амины (триэтиламин или пиридин) или избыток соединений формулы (II). В соединениях формулы (III), где X обозначает, например, кислоты, например алкилсульфонилокси- или арилсульфонилокси-остагок, предпочтителен бром. С целью ускорения реакции можно нагревать реакционную смесь и/или перемешивать ее. Предпочтительнее проводить реакцию при 30-100°С и перемещизании.
Пример 1. Дигидро-3-(4-гидрокси-1-фенэтил-4-пиперидил) -2 (ЗН) -фурапон.
К суспензии 18,5 г дигидро-3-(4-гидрокси-4пиперидил)-2(ЗН)-фуранона и 15,3 г карбоната калия в 50 мл диметилформамида капают при перемещивании раствор 18,5 г фенэтилбромида в 10 ..кл диметилформамида при 50С. Реакционную смесь перемешивают в течение 3 час При 50°С, после остывания наливают ее в 400 мл воды, экстрагируют хлороформо.м, промывают экстракты хлороформа водой, сущат над сульфатом магния и выпаривают растворитель. Из кристаллического остатка получают после двукратной .перекристаллизации из ацетона названное в заголовке соединение с т. пл. 106-108°С. Точка плавлепия гидрохлорида (из этанола) 206-207°С. Аналогично примеру 1 можно получать также следующие соединения формулы (I):
3- (1 -п-хлорфенэтил-4-гидрокси-4-пиперидил) дигидро-2(ЗН)-фуранон с т. пл. ИЗ-114°С;
3- (1 -я-бромфенэтил-4-гидрокси-4-пиперидил) дитидро-2(ЗН)-фуранон с т. пл. 115-117°С;
дигидро-3 - (4-гидрокси-4-пиперидил-1-«-толилэтил)-2(ЗН)-фуранон с т. пл. 106-107 С;
дигидро-3-(4-гидрокси-1-л-метоксифенэтил-4пиперидил)-2(ЗН)-фуранон с т. пл. 117-119°С.
Пример 6. 3-(1-о-хлорфенэтил-4-гидрокси4-пиперидил) -дигидро-2 (ЗН) -фуранон.
К суспензии 18,5 г дигидро-3-(4-гидрокси-4пиперидил)-2(ЗН)-фуранона « 16,5 г карбоната калия в 100 мл диметилформамида прибавляют по каплям раствор 21,9 г о-хлорфенэтилбромИда в 50 М.Л диметилформамида, перемешивая в течение 90 мин при 60°С. Затем дают реакциопной смеси реагировать еще в течение 90 мин при той же температуре, и после этого наливают ее в 800 мл 5%-ного раствора карбоната калия, к которому прибавлено 200 г льда. Экстрагируют несколько раз хлороформом, сушат экстракты над сульфатом магния и выпаривают растворитель при пониженном давлении. Перекристаллизовывают оставшийся медленно кристаллизующийся остаток из бензола - петролейного эфира. Т. пл. 92-94°С.
Аналогично примеру 6 можно получать также следующие соединения формулы (I):
3-(1-л1-хлорфенэтил-4-гидрокси-4-пипер.идил)дигидро-2(ЗН)-фураНОн с т. пл. 76-78°С;
3-(1-п-аминофенэтил-4 - гидрокси-4-пиперидил) - дигидро - 2(ЗН) - фуранон с т. пл. 145-146°С.
Пример 9. Дигидро-3- (4-|ГИДрокси-1-о-метоксифенэтил-4-пиперидил) -2 (ЗН) -фуранон.
К суспензии 16,5 г дигидро-3-(4-Г|ИДрокси-3пиперидил)-2(ЗН)-фуранона и 14,8 г карбоната калия в 165 мл диметилформамида прибавляют по каплям раствор 19,1 г о-метоксифенэтилбромида в 50 мл диметилформамида, перемешивая при 60°С. Дают реакционной смеси реагировать еще в течение 3 час при 60°С и затем наливают ее в 500 мл 5%-ного раствора карбоната калия, который содержит примерно 500 г льда. Экстрагируют метиленхлоридом, сущат экстракты над сульфатом магния и при пониженном давлении выпаривают растворитель. С целью удаления оставшегося еще диметилформамида сущат остаток в течение 1 час при 80°С при разрежении водоструйным насосом и Перекристаллизовывают остаток два раза из бензола. Т. пл. 98-99°С. Аналогично примеру 9 можно получать также следующие соединения формулы (I): дигидро-3-(4-гидрокси-1-л-метоксифенэтил-4пиперидил) - 2(ЗН) - фуранон с т. пл. 98,5-99,5т.
дигидро-3 - (4-гидрокси-4-.пиперидил-1-о-толил-этил)-2(ЗН)-фуранон с т. пл. тидробромида 193-194°С;
дигидро-3-(4-гидрокси - 4-пипepидил-l-лl-тoлил-этил)-2(ЗH)-фypaнoн с т. пл. 103-104X1 3-(1-я-фторфенэтил - 4 - гидрокси-4-пиперидил)-дигидро-2 (ЗН)-фуранон с т. пл. 92-93°С; 3-(1-ж-фторфенэтил-4-гидрокси - 4 - пиперидил)-дитидро-2(ЗН)-фуранон с т. пл. гидрохлорида 205-206°С;
3-(1 - о - фторфенэтил-4-гидрокси-4-пиперидил) - дигидро - 2(ЗН) - фуранон с т. пл. 123-124°С;
3-(1-.и-трифторметилфенэтил - 4 - гидрокси-4пиперидил)-дигидро-2 (ЗН)-фуранон с т. пл. гидрохлорида 165-167°С;
3-(1-о-трифторметилфенэтил-4 - гидрокси-4пиперидил)-дигидро-2(ЗН)-фуранон с т. пл. гидрохлорида 215-216°С;
3-(1-о - цианофепэтил-4-гидрокси-4-пиперидил)-дигидро-2 (ЗН)-фуранон с т. пл. гидрохлорида 207,5-208,5°С (с разложением); дигидро-3 - (4-гидрокси-1-фенэтил-4-пиперидил) - 5 - метил - 2(ЗН) - фуранон с т. пл. 129-130°С;
3- (1 -п-ацетамидофенэтил-4-гидрокси-4-пиперидил) - дигидро - 2(ЗН) - фураноп с т. пл. 193-195°С.
Пример 21. Гидрохлорид дигидро-3-(4гидрокси-4-пиперидил) - 5-метил-2(ЗН)-фуранона.
А. Гидрохларид 3-(1-бензил-4-гидрокси-4-пиперидил) -5-метил-дигидро-2 (ЗН) -фуранона.
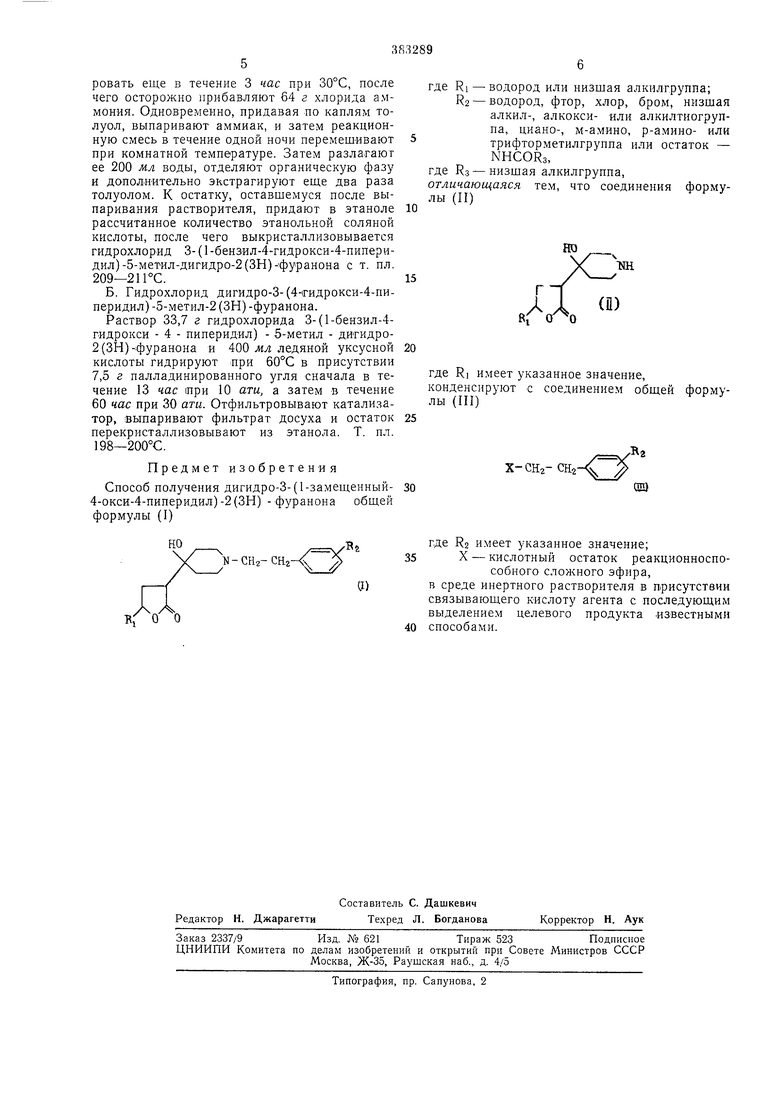
К суспензии амида лития в жидком аммиаке (изготовленной из 5,6 г лития в 1000 мл жидкого аммиака) прибавляют по каплям смесь 37,8 г 1-бензил-4-пиперидона и 70 г -валеролактона. Реакционной смеси дают реагировать еще в течение 3 час при 30°С, после чего осторожно прибавляют 64 г хлорида аммония. Одновременно, придавая по каплям толуол, выпаривают аммиак, и затем реакционную смесь в течение одной ночи перемешивают 5 при комнатной температуре. Затем разлагают ее 200 мл воды, отделяют органическую фазу и дополнительно экстрагируют еще два раза толуолом. К остатку, оставшемуся после выпаривания растворителя, придают в этаноле 10 рассчитанное количество этанольной соляной кислоты, после чего выкристаллизовывается гидрохлорид 3-(1-бензил-4-гидрокси-4-пиперидил)-5-метил-дигидро-2(ЗН)-фуранона с т. пл. 209-211°С. Б. Гидрохлорид дигидро-3-(4-1Гидрокси-4-пиперидил) -5-метил-2 (ЗН) -фуранона. Раствор 33,7 г гидрохлорида 3-(1-бензил-4гидрокси - 4 - пиперидил) - 5-метил - дитидро2 (ЗН)-фуранона и 400 жл ледяной уксусной кислоты гидрируют лри 60°С в присутствии 7,5 г палладинированного угля сначала в течение 13 час (при 10 ати, а затем в течение 60 час при 30 ати. Отфильтровывают катализатор, выпаривают фильтрат досуха и остаток 25 перекристаллизовывают из этанола. Т. пл. 198-200°С. Предмет изобретения Способ получения дигидро-3-(1-замещенный- 30 4-окси-4-пиперидил)-2(ЗН) -фуранона общей формулы (I) / Ц-СНг-Саг-- J вЛоЛ гд гд от лы гд ко л RI - водород или низщая алкилгруппа; R2 - водород, фтор, хлор, бром, низшая алкил-, алкокси- или алкилтиогруппа, циано-, м-амино, р-амино- или трифторметилгруппа или остаток - NHCORa, Rs - низшая алкилгруппа, чающаяся тем, что соединения формуII) Л Rf ( RI имеет указанное значение, енсируют с соединением общей формуIII) R2 имеет указанное значение; X - кислотный остаток реакционноспособного сложного эфира, в среде инертного растворителя в присутствии связывающего кислоту агента с последующим выделением целевого продукта .известными способами.



Авторы
Даты
1973-01-01—Публикация