1
Изобретение относится к способу получения алкилтетрагидробензилиденцикланонов, которые могут |быть использованы в парфюмерной промышленности.
На основе известной реакции конденсации Дильса-Альдера получен ряд соединений, не описанных в литературе,
Предлагаемый способ получения алкилтетрагидробензилиденцикланонов заключается в том, что кетоны алидиклического ряда подЁергйют взаимодейс1вию с алкилтетрагидробензальДегидамй при нагревании, предпочтительно при температуре 60°G, в присутствия Щелочных катализаторов, например водного раствора едкого калия, с последующим выделением целевого продукта известными приемами,
В литературе отсутствуют какиЁ-либо данные о душистых веществах, представляющих собой производные feтpaгиДpoбeнзилиДeнцик ланонов, в Частнос№ йлкилпроизводных.
Указанные соединения обладают душистыми свойствами и легко могут быть получены .на основе сопряженных диолефиновых углеводородов и карбонильных соединений алифатического и цикланового рядов, большими ресурсами которых располагает нефтехимическая промышленность. Так в качестве исходных продуктов для этой цели могут быть использованы пипериленовая фракция, являюаяся отходом нефтехимического производста и не находящая до сих пор никакого применения.
Общая методика проведения реакции.
Реакцию конденсации алкилтетрагидробенальдегидов с алициклическими кетонами
проводят Б круглодонной трехгорлой колбе,
снабженной механической мещалкой, капельной воронкой и термометром.
Реакцию проводят в присутствии 20%-него водного раствора едкого кади в количестве от реагирующей смеси при температуре 60°С и продолжительности реакций 3 час в избытке циклического кетона.
По окончании опыта продукты реакЦйь нейтрализуют 40%-ной серной кислотой, эК сТрагируют эфиром, сушат .над хлор.истым кальцием и подвергают атмосферной разгонке с отгонкой эфира, и затем вакуумной - с разделением компонентов реакционной смеси и выделением целевых продуктов реакции, алкилтетрагидробензилиденцикланонов (но вых соединений с приятным запахом). Пример 1. Взято в реакцию, г (моль): 4-метил-Д -тетрагидробензальдегида12,4(0,1)
циклопентанола42(0,5)
КОН (20%-ный водный раствор)15
Получено 9,05 г (47,3% от теоретического) 4-метил-А тетрагидробензилиденциклопентанона-2 с т. кип. 165-166°С (15 лж рт. ст.), df 1,0157, п 2° 1,5242.
Найдено MRp 57,3. Вычислено MRo 56,9. Пример 2. Взято в реакцию, г (моль): 4-метил-Д -тетрагидробензальдегида12,4(0,1)
циклогексапона49(0,5)
КОН (20%-ный водный
раствор)15
Получено 12,3 г (60,3% от теоретического) 4-метил-Д - тетрагидробензилиденциклогексанона-2 - т. кип. 170-171 °С (15 мм рт. ст.), df 1,0013, 2о 1,5216.
Найдено MRi, 62,09. Вычислено MRu 61,6.
Пример 3. Взято в реакцию, г (моль): 4-метил-Д -тетрагидробензальдегида12,4(0,1)
метилциклогексанонов56(0,5)
КОН (20%-ный водный
раствор)15
Получено 7,0 г (32,1% от теоретического метилтетрагидробензилиденметилциклогекса нонов с т. кип. 180-185°С (20 мм рт. ст.) df 0,9844, «201,5148.
Найдено MRo 66,7. Вычислено M,RD 66,17. В качестве исходных кетонов могут быть использованы и другие кетоны ал.ициклического ряда, а для получения исходных аддуктов - любые сопряженные диеновые углеводороды алифатического ряда и а, р-ненасыЩенные альдегиды.
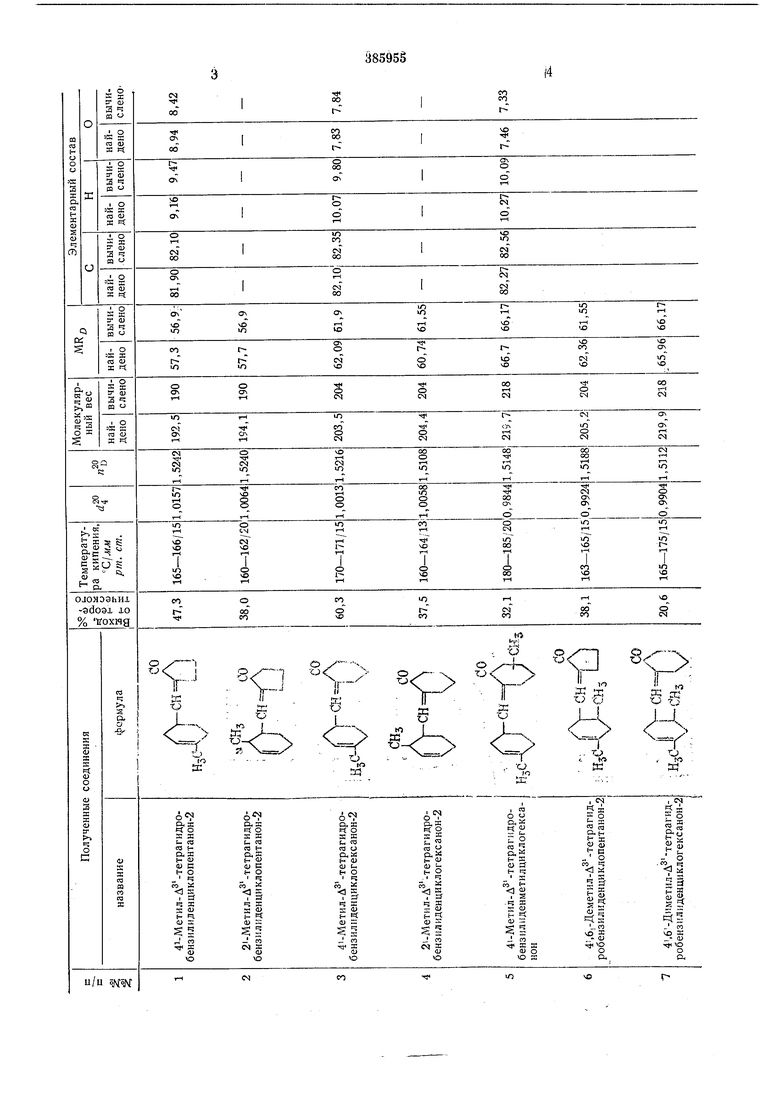
Полученные соединения и их физико-химические свойства приведены в таблице.
Методом газожидкостной хроматографии показано, что во всех случаях целевой продукт реакции состоит из смеси двух .изомеров, соответствующих продуктам взаимодействия алициклического кетона по указанной выше схеме с двумя изомерами исходного алкилтетрагидробензальдегида с различным взаимным
положением алкильной (в частности, метильной) и карбонильной группы в молекуле, образующихся при конденсации сопряженных диеновых углеводородов с непредельными альдегидами.
Хроматограммы продуктов конденсации 4-метилтетрагидробензальдегидов с циклопентаноном и с циклогексаноном, сняты при 200°С на колонке длиной 3 м, диаметром 6 мм с использованием в качестве неподвижной
фазы силиконового масла и в качестве газоносителя гелия.
Предмет изобретения
1. Способ получения алкилтетрагидробензилиденцикланонов, отличающийся тем, что кетоны алициклического ряда подвергают взаимодействию с алкилтетрагидробензальдегидами при нагревании в присутствии щелочных катализаторов, например водного раствора едкого калия, с последующим выделением целевого продукта известными приемами.
2. Способ по п. 1, отличающийся тем, что процесс ведут при 60°С.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОПЕНИЛИДЕН- ИЛИ КРОТОНИЛИДЕНСОДЕРЖАЩИХ АЛИЦИКЛИЧЕСКИХКЕТОНОВ | 1971 |
|
SU308003A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКЕНИЛЦИКЛАНОНОВ | 1971 |
|
SU304249A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛТЕТРАГИДРОБЕНЗИЛИДЕНОКСИМЕЗИТИЛОВ | 1971 |
|
SU296759A1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРДИЕНОВЫХ КЕТОНОВ | 1973 |
|
SU395356A1 |
| СПОСОБ ПОЛУЧЕНИЯ а.гДИЗАМЕЩЕННЫХ а-КАРБЭТОКСИ-б-ОКСИ-у- | 1972 |
|
SU332083A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛ- И АРАЛКИЛЗАМЕЩЕННЫХАЛЬДЕГИДОВ | 1972 |
|
SU352873A1 |
| СПОСОБ ПОЛУЧЕНИЯ КРЕМНИЙОРГАНИЧЕСКИХ БИЦИКЛИЧЕСКИХ МОНОМЕРОВ | 1971 |
|
SU311919A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1-ОКСО-1-ХЛОР•^.__ФОСФОЛЕНА | 1969 |
|
SU250140A1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТАКРИЛОВЫХ ЭФИРОВ МНОГОАТОМНЫХ АМИНОСПИРТОВ | 1967 |
|
SU193479A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОИДЗАМЕЩЕННЫХ- -а-МЕТИЛСТИРОЛОВ | 1968 |
|
SU218879A1 |


Авторы
Даты
1973-01-01—Публикация