Изобретение относится к способу получения новых стероидных соединений, обладающих ценными фармакологическими свойствами. Известен способ получения эстра-1,3,5(10)триенов, замещенных в 17а-положении, заклю- 5 чающийся в том, что на соответствующие замещенные в 17 положении винилом стероиды действуют дигалокарбеном. Однако известный способ не является универсальным и не нозволяет получить целый 10 ряд новых стероидных соединений. Предлагаемый способ получения замещенных стероидов формулы I :ЬЛ--сн с сн, где RI - алкил с 1-3 атомами углерода; R-t - атом водорода, окси или алканоил- 25 окси с 2-4 атомами углерода; ьца А и В и имеет слеения:RcO
Rc,0
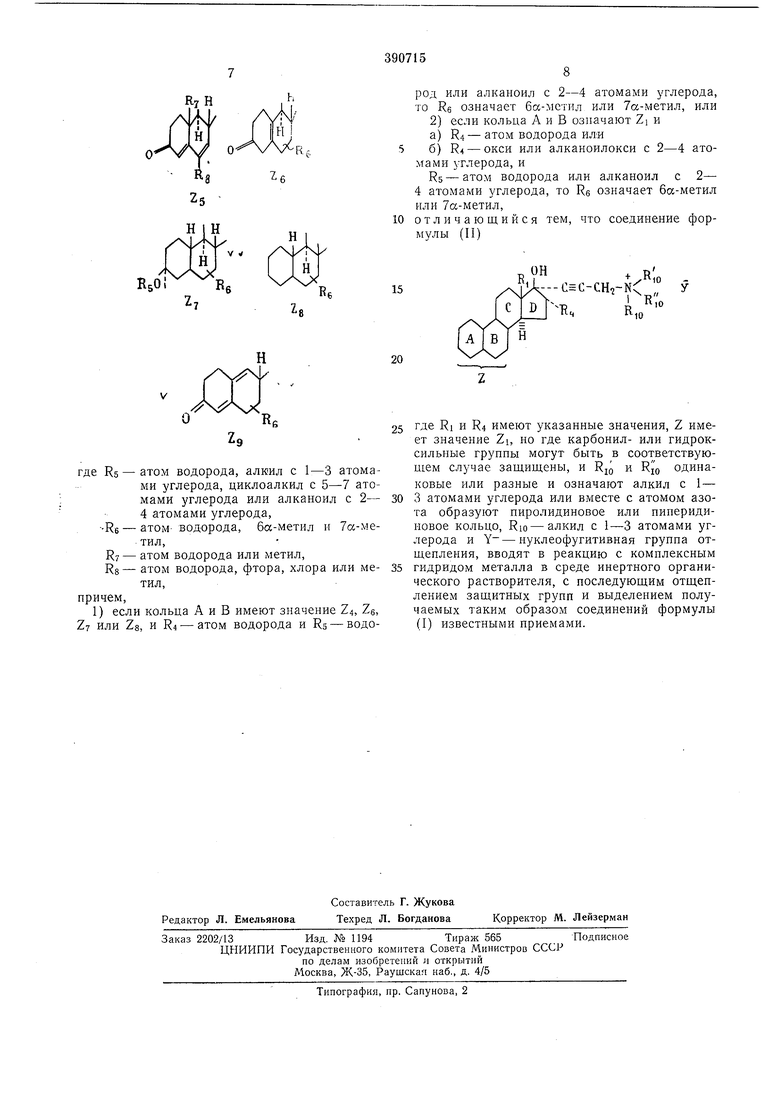
RS - атом водорода, алкил с 1-3 атомами Зглерода, циклоалкил с 5-7 атомами углерода или алканоил с 2-4 атомами углерода;
Rfi - атом водорода, 6а-метил и 7а-метил;
Нт - атом водорода или метил;
Rs-атом водорода, фтора, хлора или метил, причем,
1)если кольца А и В имеют значение Z4, Zs, Z или Zs и R4 - атом водорода и Rs - водород или алканоил с 2-4 атомами углерода, то Re - означает бес-метил или 7а-метил, или
2)если кольца А и В означают Zi и
а)R4 - атом водорода или
б)R4 - окси или алканоилокси с 2-4 атомами углерода, и Rs-атом водорода или алканоил с 2-4 атомами углерода, то Re - означает бсх-метил или 7а-метил, заключается в том, что соединение формулы II
т ОН т.
Л--с с-сн,-кс: I R.O
10
где RI и R4 - имеют указанные значения,
Z - имеет значение Zi, но где карбонил- или гидроксильные группы могут быть в соответствующем случае защищены и RJQ и Rjg одинаковые или разные и означают алкил с 1- 3 атомами углерода или вместе с атомом азота образуют пиролидиновое или пиперидииовое кольцо, где
RIO - алкил с 1-3 атомами углерода, Y - нуклеофугитивная группа отщепления, вводят в реакцию с комплексным гидридом металла в среде инертного органического растворителя с последующим отщеплением защитных групп и выделением получаемых таким образом соединений формулы I известными приема1 1и.
Комплексный гидрид .металла может представлять собой, например литийалюминийгидрид. Реакцию можно проводить примерно при температуре -80°, -f-80°C, причем в качестве инертного растворителя можно использовать простой диэтиловый эфир или тетрагидрофуран. Нуклеофугитивная группа Y может быть, например ионом хлора, брома, йода, метансульфоната или я-толуолсульфоната.
Реакцию проводят преимущественно в присутствии Си+-ионов и малых количеств слабой кислоты, например уксусной, при температуре 10°-80°С, в основном при 50°-70°С. Пример 1. 17а-Пропадиенил-3-метоксиэстра-1,3,5-(10)-триен-17р-ол.
Смесь 15,8 г 17а-этинил-3-метоксиэстра1,3,5(10)-триен-17||3-ола, 15,0 мл диметиламипометанола, 500 мг хлорида меди (I), 8,5 мл ледяной уксусной кислоты и 125 мл диоксана
в течение 5 час выдерживают при 70°С. Затем
добавляют ледяную воду, устанавливают
рН 10 и затем экстрагируют простым эфиром.
Остается пена.
Смесь 10,0 г указанного продукта, 290 мл
ацетона и 87 мл метилйодида 24 часа выдерживают при 0°С.
Получаемый продукт выпадает в виде кристаллов; его отфильтровывают. Во взвесь 3,00 г полученного выше продукта в 65 мл
безводного тетрагидрофурана при -75°С добавляют 11,25 мл 0,525 молярного раствора литийалюминийгидридтетрагидрофурана. После двухчасового перемещивания получают (при - 10°С) прозрачный раствор, который выдерживают ночь при комнатной температуре, затем охлаждают до 0°С, добавляют насыщенный водный раствор хлористого аммония и экстрагируют простым эфиром. При этом с количественным выходом получают кристаллический продукт.
Пример 2. При описанных в примере 1 условиях и с использованием следующих исходных веществ:
а)17а-этинил-3-метоксиэстра - 1,3,5(10)6,8пентаеп-17|3-ол,
б)17а-этинил-3-метокси-7а-метилэстра-1,3,5 (10)-триеп-17|3-ол,
в)17а-этинил-16а-окси-3-метоксиэстра -1,3,5 (10)-триеп-17р-ол,
получают:
а)17сс-пропандиенил - 3 - метоксиэстра-1,3,5 (10) -7-тетраен-17 Р-ОЛ,
б)17а-пропадиенил-3-метокси-7а - метилэстра-1,3,5(10)-триен-17р-ол,
в) 17а-пропадиенил-16а-окси-3 - метоксиэстра-1,3,5(10)-триен-17р-ол, которые дальще употребляют в виде их метилйодидов.
Пример 3. 7а-метил-17а-пропадиенил-3метоксиэстра-2,5(10)-диен-17р-ол.
В смесь реактива Гриньяра, состоящую из 1,50 г магния, 4,68 г этилбромида и 70 мл тетрагидрофурана по каплям добавляют 5,3 г диметиламинопропина, растворенного в 10 мл тетрагидрофурана. По окончании образования
этана добавляют раствор 1,716 г 3-метоксиэстра-2,5(10)-диен-17-она в 30 мл тетрагидрофурана по каплям при постоянной температуре О-5°С; реакцию проводят 4 часа при 20- 25°С. После добавления 100 мл 2 н. раствора едкого натра смесь концентрируют при температуре не выше 30°С до общего объема 100 мл в вакууме. Концентрат экстрагируют простым эфиром (5x25 мм), причем в целях облегчения фазоотделения используют центрифугу. Путем упаривания высушенных растворов (эфирных) и отсасывания имеющегося избытка диметиламинопропина получают целевой продукт.
Полученный продукт (2,1 г) растворяют в 30 мл ацетона. После добавления 3,5 г метилйодида смесь выдерживают 18 час при 8°С. Выкристаллизовывается 7а-метил-17а(3-диметиламино-1-пропинил) -3 - метоксиэстра - 2,5 (10)-диен-17а,р-ол-метилйодид. Его отфильтровывают и промывают безводным простым эфиром.
Во взвесь 2,6 г полученного выще продукта в 50 мл тетрагидрофурана при -75°С добавляют 9,3 мл 0,525 молярного раствора литийалюминийгидрида - тетрагидрофурана. Температуру смеси доводят до -10°С и перемешивают до получения прозрачного раствора ( мин) и затем еще 12 час держат при комнатной температуре. Затем добавляют 100 мл водного 2 н. раствора едкого натра, после чего смесь концентрируют в вакууме до общего объема 100 мл; раствор гидроокиси натрия содержит 50 мл ди-третичного бутилкрезола. После экстрагирования 5X20 мл простого эфира, фазоотделения путем центрифуги, высушивания эфирных растворов над карбонатом калия и выпаривания получают 7аметил-17а-пропадиенил - 3 - метоксиэстра-2,5 (10)-диеп-17р-ол.
Пример 4. 7а-метил-17а-пропадиенилэстра-5(10)-ен-17р-ол-3-он.
2,1 г 7сс-метил-17а-пропадиенил-3-метоксиэстра-2,5(10)-диен-17р-ола, полученного в примере 3, растворяют в смеси, состоящей из 20 мл ледяной уксусной кислоты и 2 мл воды. Через 2 часа добавляют 200 мл воды и экстрагируют продукт этилацетатом (5Х XIО мл). После испарения этилацетатных экстрактов получают 7а-метил-17а-пропадиенилэстра-5(10)-ен-17|3-ол-3-он в виде кристаллического твердого веш:ества.
Пример 5. 7а-метил-17а-пропадиенилэстра-4-ен-17|р-ол-3-он.
5,6 г 7а-метил-17а-пропадиенил-3-метоксиэстра-2,5-(10)-диен-17р-ола, полученного согласно примеру 3, растворяют в смеси, состоящей из 50 мл метанола и 1,5 мл 11 н. водной соляной кислоты и 30 мин выдерживают при ЯО°С. После разбавления 100 мл воды продукт экстрагируют хлористым метиленом (5Х Х15 мм). После упаривания высушенных растворов хлористого метилена и последующей перекристаллизации остатка из циклогексана получают чистый 7а-метил-17а-пропадиенилэстра-4-ен-17р-ол-3-он.
Пример 6. По способу получения, описанному в примерах 3 и 5, получают при использовании следующих исходных продуктов:
а) 3-этилендиокси-6а-метиландроста-5-ен-17он
б)З-этилендиоксиэстра-5 (10) ,9 (11) -диен-17он
в)3-этилендиокси-6-фторандроста-4,6 - диен17-он
г)3-этилендиокси-6-хлорандроста-4,6 - диен17-он
д)3-этилендиокси-6-метиландроста-4,6-диен17-он
следующие соединения:
а)6а-метил-17а-пронадиениландроста-4-ен17Р-ОЛ-3-ОН
б)17а.-пропадиенилэстра-4,9(10)-диен - 17рол-З-он, в виде некристаллического продукта
с ультрафиолетовым спектром в этаноле ,5 ммк, ,100; с ЯМР-спектром с отдельной линией спектра при 5,7 ррт и 1,08 ррт, а также ИФ-спектром в 3590 сми 1950 см-.
в) 6-фтор-17а-нропадиениландроста-4,6-диен17р-ол-3-он.
г)6-хлор-17а-пропадиениландроста-4,6-диен17Р-ОЛ-3-ОН.
д)6-метил-17а-пропадиениландроста-4,6-диен-17р-ол-3-он.
Предмет изобретения
Способ получения замещенных стероидов формулы (I)
р ОН
Mr-СН С СН7
где RI - алкил с 1-3 атомами углерода;
R4 - атом водорода, окси или алканоилокси с 2-4 атомами углерода; Z - означает кольца А и В и имеет следующие значения
Кб ВбО
ПсО
RT Н
KsO R
где Rs - атом водорода, алкил с 1-3 атомами углерода, циклоалкил с 5-7 атомами углерода или алканоил с 2- 4 атомами углерода, -Re - атом- водорода, 6а-метил и 7а-метил,
Rr - атом водорода или метил, Rs- атом водорода, фтора, хлора или метил, причем,
1) если кольца А и В имеют значение Z4, Zg, 2.1 или Ze, и R4 - атом водорода и Rs - водород или алканоил с 2-4 атомами углерода, то Re означает 6а-метил или 7а-метил, или 2) если кольца А и В означают Ъ и
а)R4 - атом водорода или
б)R4 - ОКОЙ или алканоилокси с 2-4 атомами углерода, и
Rs-атом водорода или алканоил с 2- 4 атомами углерода, то Re означает бк-метил или 7а-метил,
отличающийся тем, что соединение формулы (II)
R
CH,-N :
R 10
где RI и R4 имеют указанные значения, Z имеет значение Zi, но где карбоиил- или гидроксильные груииы могут быть в соответствующем случае защищены, и RJQ и RIQ одинаковые или разные и означают алкил с 1-
3 атомами углерода или вместе с атомом азота образуют пиролидиновое или иииеридииовое кольцо, Rio- алкил с 1-3 атомами углерода и Y - иуклеофугитивиая групиа отщепления, вводят в реакцию с комплексным
гидридом металла в среде инертного органического растворителя, с последующим отщеилением защитных груип и выделением получаемых таким образом соединений формулы (I) известными приемами.


| название | год | авторы | номер документа |
|---|---|---|---|
| ТМ. Кл. С 07с 169/08УДК 547.689.6.07(088.8) | 1973 |
|
SU379088A1 |
| ^А1ЕЙТИ04ЕХНй-1?иКАШБ^^^ПЛИОТЕКА I | 1973 |
|
SU376938A1 |
| ВПТ БгНПП •! <'i'i.''''''tpT{ ФциМ i';!''''ii.-5 '' | 1973 |
|
SU390714A1 |
| Способ получения 9 - метилстероидов | 1971 |
|
SU493962A3 |
| Способ получения 9 -метилстероидов | 1971 |
|
SU488405A3 |
| Способ получения производных 11 -метилстероидов | 1971 |
|
SU474978A3 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИМОВ 3-КЕТО-17а ПРОИАДИЕНИЛ СТЕРОИДОВ | 1971 |
|
SU433673A3 |
| Способ получения 17 -пропадиенил3-кетостероидов | 1971 |
|
SU495837A3 |
| Способ получения 3-кетостероидов | 1971 |
|
SU451239A3 |
| СПОСОБ ПОЛУЧЕНИЯ 1?а-АЛКА-1',3'-ДИИНИЛ-17р-ОКСИ-(17|3- -АЛКОКСИ)-СТЕРОИДНЫХ СОЕДИНЕНИЙ | 1969 |
|
SU248567A1 |


Авторы
Даты
1973-01-01—Публикация