1
предлагается способ Получения новых соединений ряда дигидролизергиновой или дигидроизолизергиновой кислоты, обладающих фармакологической активностью.
Известен способ получения 1-алкил(арил) дигидролизергиновой кислоты путем каталитической гидрогенизации 9,10-пептида лизергиновой кислоты с последующими алкилировакием в положение 1 и гидролизом. Однако исходным веществом для этой реакции является применяемый для терапевтических целей препарат.
Целью изобретения является разработка нового метода получения дигидролизергиновой, дигидроизолизергиновой кислоты и их нроизЁодных непосредственно из лизергиновой или изолизергиновой кислоты.
Предлагаемый способ получения производных дигидролизергиновой или дигидроизолизергиновой кислоты общей формулы
N-CH,
4rN
где RI - водород, метил; R2 - неразветвленная или разветвленная алкиламинная группа, замещенная, по крайней мере, двумя гидроксильными группами, или аралкиламинная группа, замещенная одной ГИДрОКСИЛЬНОЙ группой, или ГруННа ОД}ЮЙ
из приведенных ниже формул
СН ОНNH
10
I11
-NH-CH-CH2-CH2--CH2-NH-C-NH-NO
СНг-СН ОН
КН-СВз-СН7-СН7-К
СН-г-СН ОН -к-сн2-сщов.
-NH-CH -CH-z-CHi-N
-кГ
:N-cuo-cH-cH. он
СНоОН -NH-CH-СЩТ
N
СН-зОН
N07
-NH-CH-CH ОБ
CHjOH -NH-CH-CH
И в ТОМ случае, когда необходимое для алкилирования основание добавляют после, а не исиользуют то, которое образовалось в реакционной массе. Целевой продукт выделяют в виде основания или переводят в соль известпым способом. Соль получают взаимодействием с пригодной для терапевтических целей органической или неорганической кислотой.
Пример 1. Получение дигидролизергиповой кислоты.
3 г металлического иатрия растворяют в 300 мл жидкого аммиака и 2 мл этанола. После растворения натрия добавляют 2,68 г лизергиновой кислоты при минус 30 - минус 40°С. Реакциоппую смесь перемещивают ири этой температуре в течение 3 час, затем к ней прикапывают 20 мл абсолютированного этилового спирта. Аммиак испаряют и сухой остаток растворяют в 30 мл воды, рН раствора поддерживают с помощью уксусной кислоты 7-9 ири охлаждении. Дигидролизергииовую кислоту кристаллизуют в холодильнике в течение нескольких дней, фильтруют, промывают водой и ацетоном, затем сущат в вакууме, т. пл. 318°С; а д - 122° (, пиридип).
-KH-CH-CH2
где Ri имеет указанные значения, или их солен, закл 0чается в том, что сое ДИнение оби1ен формулы
СНR,-N
где RI и R2 имеют указанные значения, или его соль нодвергают восстановлению в жидком аммиаке или в растворе жидкого аммиака в органическом растворителе, например в спирте, эфире или тетрагидрофуране, с иомощыо щелочного металла, например натрия или калия.
Реакцию обычно проводят нри низкой температуре (минус 30 - минус 40°С). Полученное соединение выделяют или, если требуется, подвергают дальнейшему метилированию, например йодистым метилом, в том же растворе аммиака в присутствии сильиого осиоваиия. С этой целью для восстановления используют большой избыток ш,елочного металла, который превращают после восстановления 1 звестным методом в амид или алкоголят щелочного металла, используемый для метилирования. Метилирование можно осуществлять
Пример 2. Получение дигидроизолизергиновой кислоты.
Применяют ту же методику эксперимента, что и в примере 1, по в качестве исходного продукта используют изолизергиповую кисло ту. Дигидроизолизергиповая кислота (1)
плавится при 272°С; -82° (, пИриДип), Дигидроизолизергиповая кИслота -(2)-при 306°С; а о + 15° (, пиридип).
Пример 3. Получение 1-метилдигидролйзергиновой кислоты.
3 г металлического натрия растворяют приблизительно в 300 мл жидкого аммиака. После растворения добавляют 3,68 г тщательно измельченной и осушенной лизергиновой кислоты. Реакциоппую смесь иеремещивают при мипус 30 - мипус 40°С в течение 3-4 час. За ходом гидрогенизации можио следить с помощью тонкослойной хроматографии на силикагеле (используют смесь хлороформ : вода : метанол в соотношении 10: 1 :5). Гидрированный продукт не флуоресцирует в ультрафиолетовых лучах. После окончания реакции к смеси прибавляют абсолютированный этиловый спирт в количестве, достаточпом для исчезновения голубой окраски раствора, затем прикаиывают раствор 4,8 г йодистого метила в 5 мл абсолютированного эфира. Смесь перемешивают 10-15 мин и вынаривают досуха в вакууме. Остаток смачивают 5 мл этилового сиирта и растворяют в 20 мл воды. рП
0 раствора поддерживают 7-8 при охлаждении с помощью уксусной кислоты. 1-Метилдигидролизергиновую кислоту кристаллизуют в холодильнике в течение нескольких дней, затем фильтру от, промывают водой и ацетоном и
осушают в вакуумпом эксикаторе, т. пл. 235°С с разложением; а о +111° (, пиридин). Пример 4. Получение 1-метилдигидроизолизергииовой кислоты-(1). Методика эксперимента та же, что и в примере 1, ио в качестве исходного соединения применяют изолизергиновую кислоту, т. пл. продукта 217°С. Пример 5. Получение амида дигидролизергиповой кислоты. 2,6 г металлического натрия растворяют в 300 мл жидкого аммиака при перемен1иваиии, а затем добавляют 2,6 г сухого и тщательно размельченного амида лизергиновон кислоты. Раствор перемешивают в течение 4 час, затем к нему приливают 25 мл абсолютированного эфира, после чего раствор выпаривают в вакууме. К остатку добавляют 50 мл 1о/о-ного раствора тиофосфата натрия и 100 мл хлороформа. рН водного раствора поддерживают 8 с помощью хлористоводородной кислоты. После взбалтывания отделяют органический слой. Взбалтывание повторяют 5 раз, нрнмеияя по 50 мл хлороформа. Собрапные органические слои осушают безводиым сульфатом натрия, а затем выпаривают досуха. Сухой остаток растворяют в этиловом спирте и получают соль при взаимодействии с маленновой кислотой. Кристаллизации способствует добавление небольшого количества эфира. Основание амида дигидролизергиновой кислоты плавится при 276°С; а о -131° (, пиридин) . Пример 6. Получение бималеата амида 1-метилдигидролизергииовой кислоты. 2,6 г металлического иатрия растворяют при температуре ниже минус 40°С в 300 мл жидкого аммиака, затем добавляют 2,6 г амида лизергиновой кислоты. После перемешивания в течепие 4 час добиваются обеснвечивания голубого раствора путем добавления этилового спирта. Затем прикапывают раствор 1,2 г йодистого метила в 5 мл абсолютированного эфира и спустя 5 мин раствор выпаривают в вакууме. Остаток в дальнейшем обрабатывают по методике, описанной в примере 5, затем остаток после выпаривания раствора, содержащего хлороформ, снова растворяют в небольшом количестве хлороформа и осаждают петролейиым эфиром. Сырой продукт очищают хроматографически иа силикагелевой колоике, элюируют смесью хлороформа, воды и этанола. После выпаривания элюэнта сухой остаток обрабатывают спиртовым раствором малеиновой кислоты с образованием соли. Осиование амида 1-метилдигидролизергиновой кислоты плавится ири 256°С; а о -135° (, пиридин). Пример 7. Получение бималеата 1-амидо-4-оксибутандигидролизергиновой кислоты. Соединение получают из 3,38 г 1-амидо-4оксибутанлизергиноБОЙ кислоты по методике примера 6, т. пл. 132-Л34°С; а о -50,7° (,5, 500/о-ныи водный этанол). Пример 8. Получение бималеата 1-амидо4-оксибутан-1-метилдигидролизергиновой кислоты. Соединение получают из 3,38 г 1-амидо-4оксибутанлизергиновой кислоты по методике примера 6, т. пл. 123-125°С; а 0° -51,7° (,5, 50 /и-ный водн1з Й этанол). Пример 9. Получение бималеата амид(2) - 2-этил-1,3-диоксинропандигндролизергиновой кислоты. Соединение получают, применяя 2,3 г металлического натрия на 3,95 г амид-(2)-2-этил1,3-диоксипронанлизергиновой кислоты, по методике примера 5, т. пл. 118-120°С; а о -45,5° (,5, 501/о-ный водный этапол). Прнмер 10. Получение бималеата 1-метилднгидролизергил-(о-нитро- -арпп1ИН{)ла. А. Получение гидрохлорнда хлорида 1-метилдигидролизергиновой кнслоты. К 3,5 г пентахлорида фосфора, растворетнюго в смеси 60 мл ацетоиитрила и 60 мл треххлористого фосфора, добавляют 2,81 г сухой 1-метилднгидролизергиновой кислоты, полученной согласно методике примера 3. Раствор образуется временно п после дальнейшего перемешивания осаждается гидрохлорид хлорида 1-метилдигидролпзергиновой кислоты. Суспепзию перемешивают в течепие 30 мип при О-5°С. Затем реакциопную смесь выпаривают в вакууме, остаток сусиепдируют в 30 мл тетрагидрофурана и промывают повторно иетролейным эфиром, затем сушат при 40°С в вакууме. Б. Получеппе Ьметилдигидролизергил-сонитро-.-аргининметилового эфира. 3,1 г гидрохлорида L-(o-нитpoapгининмeтилового эфира растворяют в 50 мл диметилформамида при перемешивании. Раствор разбавляют 100 мл хлороформа и добавляют к нему 8,4 мл триэтиламина. Гидрохлорид хлорида 1-метилдигидролизергиновой кислоты, полученный по методике примера 10А, добавляют при охлаждении льдом и водой. Реакния ацилирования заканчивается в течение 1 час. Реакционную смесь вынаривают досуха в вакууме ири низкой температуре, затем суспеидируют Б 100 мл 1%-ного водного раствора винной кислоты и в 200 мл смеси хлороформа и изопропилового спирта (4:1). рН смеси доводят до 8 с иомон1ью водного раствора гидроокиси аммония. После взбалтываиия отделяют органический слой. Взбалтывание повторяют 4 раза, применяя но 50 мл упомянутой смеси хлороформа и изопропилового спирта. Собранные органические слои осущают безводным сульфатом иатрия, затем фильтруют и выпаривают досуха в вакууме. Остаток растворяют в хлороформе и высаживают иетролейпым эфиром. Осадок фильтруют, промывают эфиром и сущат в вакууме до постоянного веса,
С. Получение бималеата 1-метилдигидролизергил-(й-питро-/,-аргинипола.
5 г размельченного хлорида кальция растворяют в 200 мл абсолютированного этанола при иеремешивании. После растворения добавляют эфирное соединение, полученное но методике примера ЮБ. Раствор охлаждают ледяной водой до О-2°С и вводят 2,5 г боргидрида натрия при интенсивном перемешивании. Восстановление завершается через
4час. рН раствора доводят до 6 с помощью
. хлористоводородной кислоты, раствор выпаривают до сиропообразной массы при низкой температуре в вакууме. Остаток растворяют в 100 мл воды и подщелачивают гидроокисью аммония до рН 8, затем взбалтывают 8 раз, применяя по 50 мл смеси хлороформа н изопронилового спирта (4:1). Собранные органические слои осущают, фильтруют н вынаривают досуха. Изомер отделяют от сырого продукта хроматографически на силикагеле. Элюирование осуществляют смесью хлороформа, воды и этанола (90 : 4,5 : 30). Из очищенного продукта получают соль добавлением спиртового раствора малеиповой кислоты, т. пл. 144--145°С; -49° (: 0,5, бОо/о-ный водный этанол).
Пример И. Получение бималеата дигидролизергил-З-(ннтрофенил) - пропан-1,3-диоламида-(2).
Соединение получают из 4,4 г лизергил-3(нитрофенил)-пропан-1,3-диоламнда-(2), полученного по методике примера 5. Соль образуется из основания при добавлении малеиновой кислоты, т. пл. 114-1 5°С; а д -69,6° (,5, 50%-пый водный этанол).
Пример 12. Получение бималеата 1-метилдигидролизергил - 3-(питpoфeнил)нpoпaнl,3-диoлaмидa-(2).
Соединение получают по методике примера
6из 4,4 г лизергил-3-(нитрофеиил)нрона11-1,3диоламида-(2), т. пл. 121 -123°С; а о -74,2° (,5, 50/о-иый водный этанол).
Пример 13. Получение тартрата (4-)-бутаноламида 1-метилдигидролизергиновой кислоты.
А. Получение метилового эфира 2-амидобутирлизергиновой кислоты.
К смеси 150 мл абсолютированного хлороформа и 50 мл трет-бутанола при перемещивании добавляют 1,54 г гидрохлорида метилового эфира (+)-2-аминомасляной кислоты и 5,6 мл триэтиламина. Гидрохлорид лизергииовой кислоты, полученный в соответствии с примером 10А из 2,68 г лизергиновой кислоты, добавляют при охлаждении ледяной водой. Реакция сочетания протекает в течение 30 мин. Реакционную смесь разбавляют 150 мл хлороформа и взбалтывают с 100 мл 2%-ного водного раствора хлористоводородной кислоты. Выделенный водный слой взбалтывают (3 раза по 100 мл) с хлороформом прИ рН, равном 8. Собранные органические слои осушают безводным сульфатом патрия, фильтруют и сушат в вакууме. Остаток после выпаривания осушают пятиокисью фосфора.
Б. Получение (+)-бутаноламида лизергиновой кислоты.
В качестве исходного продукта используют эфирное соединение из примера 13А, методика получения та же, что в примере 10С. Д,лп восстановления применяют 3,5 г хлорида кальция и 1,75 г боргидрида натрия.
С. Полученке тартрата (-|-)-бутаноламида 1 -метилдигидролнзергиновой кислоты.
Соединение получают по методике примера 6 из вещества, описанного выше в пункте Б, т. пл. 143-145°С; -50° ,5, вода).
Пример 14. Получение дихлорфенилгндразида дигидролизергиновой кислоты.
Соединение получают в соответс1вни с методикой примера 5 из 4,27 г дн.хлорфенилгидразида лизергнновой кислоты, т. пл. его 200- 204°С; а л --47,9° (,5, 50%-ный водный этанол).
Пример 15. Получение дихлорфенилгидразида 1-метилдигндролизергиновой кислоты.
Соединение получают по методике примера 3 из 2,47 г дихлорфенилгидразида лизергиновой кислоты, т. пл. равна 256-258°С; а д : 0 -70,6° (с 0,5, пиридин).
Пример 16. Получение бималеата 2-амидо-1-оксн-З-индолилнропан - 1-метилдигидролизергиповой кислоты.
Соединение получают по методике, описанной в примере 10, из 2,82 г 1-метилдигидролизергиновой кислоты и 2,6 г гидрохлорида триптофанметилового эфира. Для восстановления применяют 4,5 г хлорида кальция и 2,25 г боргидрида натрня, т. пл. 140-142°С; -43,5° (с 0,5, 50%-ный водный этанол).
Пример 17. Получение бнмалеата 2-амиДО-1-ОКСИ - 3-имидазол ил пропан- -метилдигид5 ролизергнповой кислоты.
Соединение получают из 2,82 г 1-метилдигидролнзергиновой кислоты и 1,8 г гистидинметилового эфира но методике примера 10. Для восстановления используют 4,0 г хлорида Q кальция и 2,0 г боргидрида натрня, т. нл. 139-141°С; -55,1° (с 0,5, 50о/о-ный водный этанол).
Пример 18. Получепне бнмалеата (N-2оксипронил) нинеразида дигидролизергиновой кислоты.
Соединение сн1ггезируют из 3,95 г (N-2-оксипронил)пиперазида лизергпцовой кнслоты по методике примера 5, но для гндрогенизации используют 3,9 г металлического калия, т. пл. 206-207°С; -47,5° (с 0,5, 50%-пый водный этанол).
Пример 19. Получение (N-оксиэтилпиперазнно) - Ы-пропиламнд-1-бнмалеата дигидролизергиновой кислоты.
Соединение получают по методике примера 5 из 4,35 г (М-оксиэтилпиперазино)-Н-пропиламидолизергиновой кислоты, но для гидрогенизации применяют 6,8 г алкоголята натрия, т. пл. 158-160°С; -29,45° (с 0,5, 500/о-ный водный этанол).
Пример 20. Получение 3-диэтанол- (иминопропил) амида - (1) дигидролизергиновой кислоты.
К 3000 мл жидкого аммиака добавляют 2 мл абсолютированного этанола и 4,15 г 3-диэтанол- (иминопронил) амида- (1) лизергиновой кислоты. При перемешивании прибавляют небольшими порциями 4 г металлического натрия, а затем перемешивают в течение 2 час. После этого к раствору приливают 15 мл абсолютированного этанола, а затем выпаривают в вакууме. Сухой остаток растворяют в 100 мл 2%-ного водного раствора бисульфита натрия, рП раствора доводят до 8 водной хлористоводородной кислотой, смесь взбалтывают 7 раз, применяя по 50 мл смеси хлороформа и изопропанола (4:1). Собранные органические слои осушают безводным сульфатом магния, фильтруют и выпаривают.
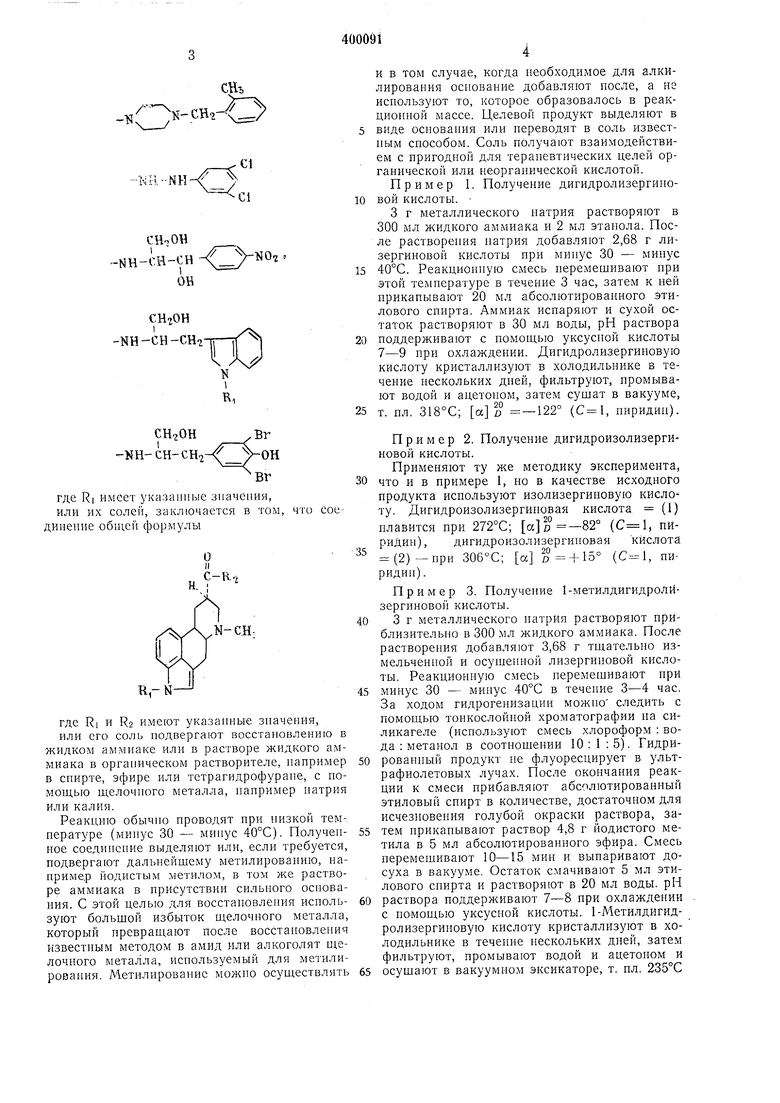
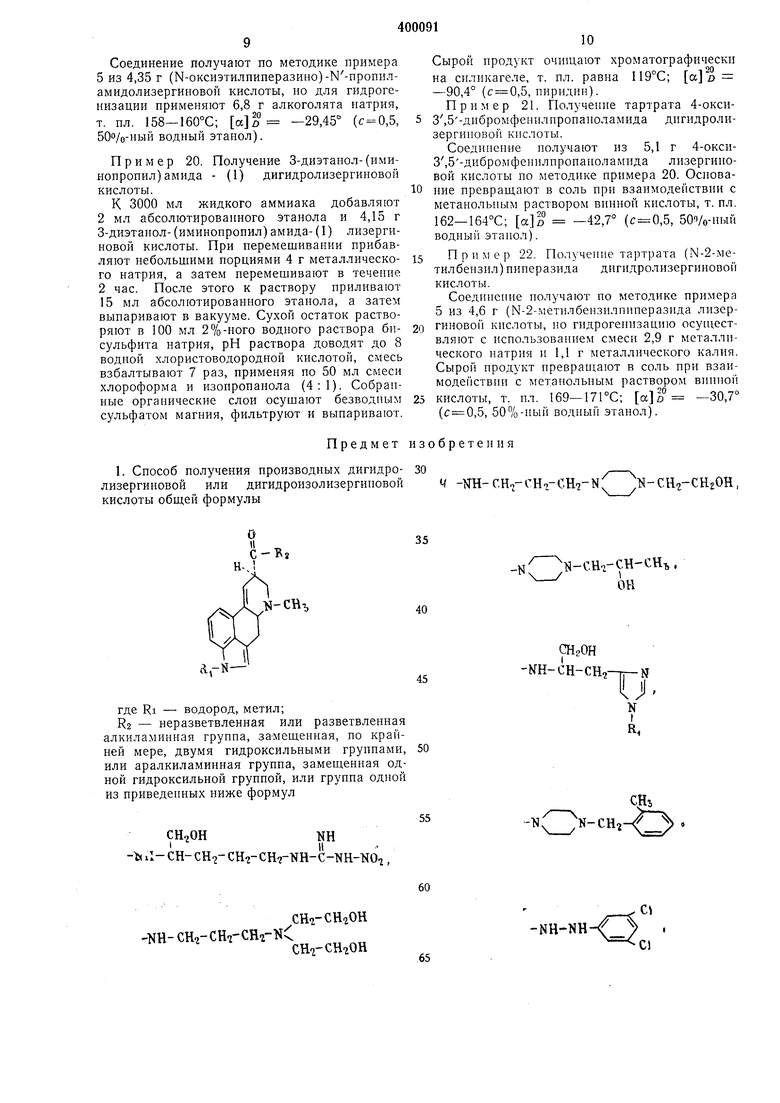
Предмет изобретения 1. Способ получения производных дигидро- 30
лизергиновои или дигидроизолизергиновои кислоты общей формулы .л, где RI - водород, метил; R2 - перазветвленная или разветвленная алкиламинная группа, за 1ещенная, но крайней мере, двумя гидроксильными груннами, или аралкиламинная группа, замещенная одной гидроксильиой группой, или группа одной из приведенных ниже формул СН.ОНNH -tt il- СН- CH-j- СН,- CH7-NH-C-KH-NO,
Сырой продукт очищают хроматографически
на силикагеле, т. пл. равна 119°С; -90,4° (с 0,5, пиридин).
Пример 21. Получение тартрата 4-окси3,5-дибромфе11илнропаноламида дигидролизергиновой кислоты.
Соединение получают из 5,1 г 4-окси3,5-дибромфенилпрона1юл амида лизергиновой кислоты но методике примера 20. Основание превращают в соль при взаимодействии с метанольным раствором винной кислоты, т. ил. 162-164°С; -42,7° (,5, 50«/о-ный водный этанол).
Пример 22. Получение тартрата (N-2-метилбензил)пиперазида дигидролизергиновой кислоты.
Соединение получают по методике примера 5 из 4,6 г (N-2-метилбензплппперазнда лизергиновой кислоты, но гидрогенизацию осуплествляют с использованием смеси 2,9 г металлического натрия и 1,1 г металлического калия. Сырой продукт превращают в соль при взаимодействии с метанольпым раствором виппой кислоты, т. пл. 169-171°С; -30,7° (,5, 50%-ный водный этанол).
V -tra-cH -rH.-cH7-N ;-н-сн2-снгОн, -е,Н2-с,н-сНь. он н-cн-cн2- г- J : -сн,-


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения амидов лизергиновой кислоты или их солей | 1976 |
|
SU604493A3 |
| Способ получения эрголиновых соединений или их солей | 1975 |
|
SU625612A3 |
| Способ получения амидов лизергиновой кислоты или их солей | 1973 |
|
SU468419A3 |
| Способ получения алкалоидов спорыньи | 1970 |
|
SU542475A3 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКАЛОИДОВ | 1973 |
|
SU372813A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКАЛОИДОВ | 1972 |
|
SU351369A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКАЛОИДОВ | 1970 |
|
SU417944A3 |
| Способ получения -2-галоид-6- метил-8-цианометил или -2-галоид6-метил-8-карбоксамидометилэрголинов | 1973 |
|
SU645581A3 |
| Способ получения д-2-замещенных-6-метил-8-цианометил8-цианометилэрголинов или их солей | 1974 |
|
SU584780A3 |
| Способ получения -замещенных сложных эфиров 9,10-дигидролизергиновой кислоты | 1978 |
|
SU784775A3 |

/
NH-CH -CHrCHrN
CH-i-CH OH
-NH-NH65
СН20Н
-NH-CH-CH -)-NO ОН
-NH-CH-СНг
-NH-CH-CH7-
где Ri имеет указанные значения, или их солей, отличающийся тем, что соединение общей формулы
12
.КСН.,
R,-N
где RI и Rs имеют указанные значения,
или его соль подвергают восстановлению в
жидком аммиаке или в растворе жидкого аммиака в органическом растворителе, например в снирте, эфире или тетрагидрофуране, с номощью щелочного металла, например натрия или калия, полученное нри этом соединение выделяют или подвергают дальнейшему метилированию в присутствии сильного основания с последующим выделением целевого продукта или переводом его в соль известным способом.


Даты
1973-01-01—Публикация