Данное изобретение относится к способу получения ацилпроизБОДНых сердечных гликозидов, обладающих ценными фармакологическими свойствами.
Известен способ получения моноацильных и диацильных производных просцилларидина А действием на последний хлористым ацилом в среде безводного пиридина. В зависимости от количества ацилирующего агента получается либо смесь диацетатов исходного просцилларидина А, либо смесь его моно- и диацетатов, разделяемых далее хроматографически. Действием на просцилларидин А ангидридов кислот получен его триацетат. Второй способ получения моно- и диацетильных производных заключается в действии на исходный гликозид ангидридов кислот в присутствии эфирата трехфтористого бора. В зависимости от температуры проведения реакции (15°-35°) полученная смесь содержит преимущественно либо диацетаты, либо моноацетаты соответственно.
Однако во всех указанных способах в результате реакции получаются смеси ацилпроизводных различной степени ацилирования или же смеси ди- или моноацильных производных.
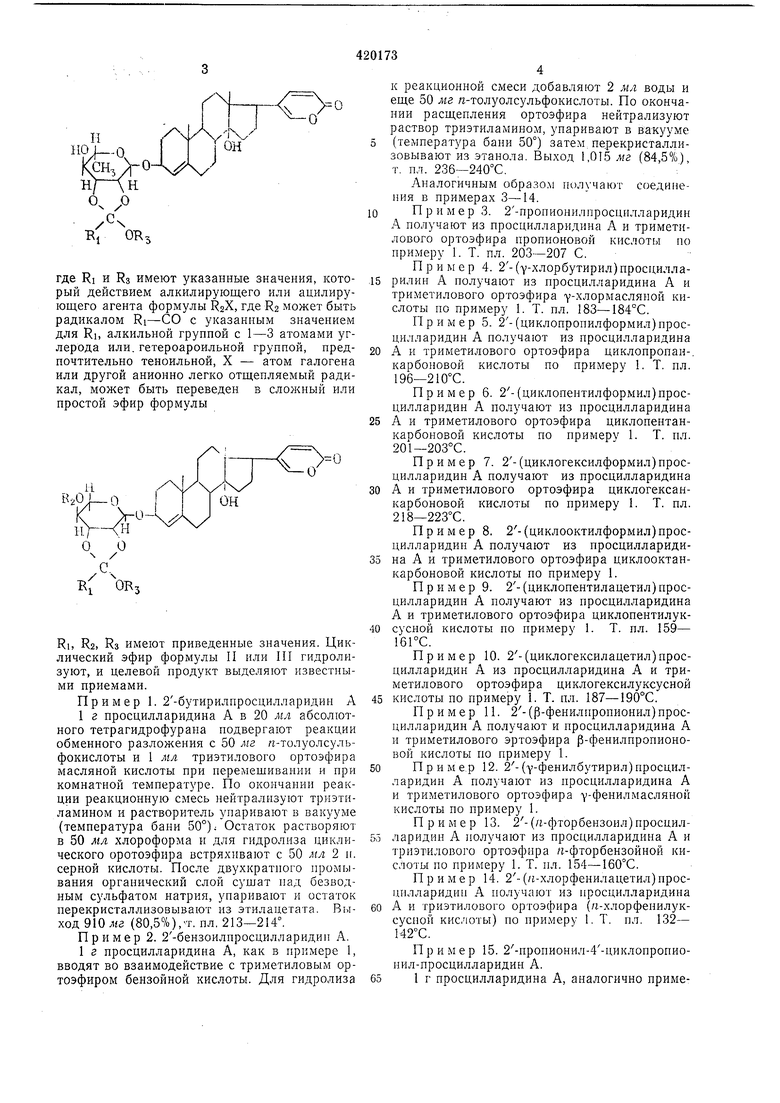
Предлагаемый способ позволяет получать индивидуальные, не описанные в литературе ацилпроизводные просцилларидина А технологически просто и с хорощими выходами. Способ заключается в том, что просцилларидин А общей формулы
10
ОН ОН
15
путем переэтерификации с ортоэфиром
RI-С(ОКз)з,
где RI - алкильная группа с 1-4 С - атомами, замещенная галогеном или циклоалкильным радикалом; алкильная группа с 2- 4 атомами углерода; циклоалкильный радикал с 3-8 атомами углерода или аралкильный или арильный радикал, ароматическое ядро которых может быть замещено галогеном, или метильная группа, или ацильная группа; и Rs - низщая алкильная группа, переводят в циклический ортоэфир формулы
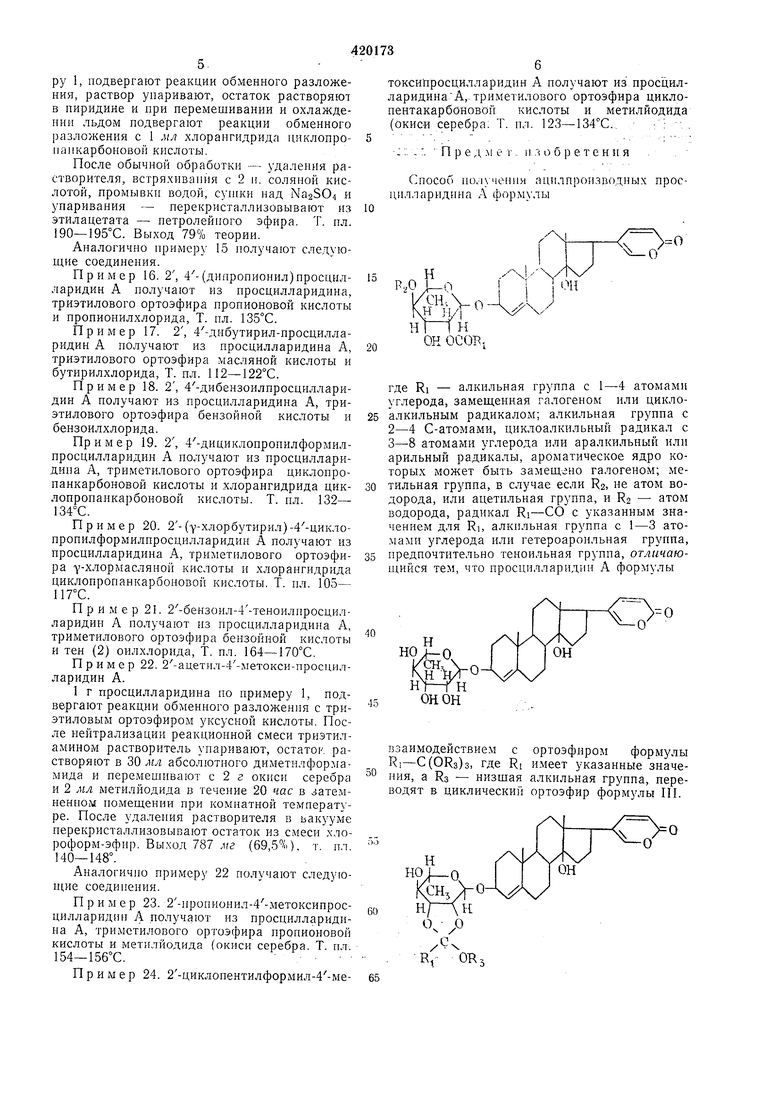
где Ri и Rs имеют указанные значения, который действием алкилирующего или ацилирующего агента формулы RsX, где R2 может быть радикалом Ri-СО с указанным значением для RI, алкильной групной с 1-3 атомами углерода или.гетероароильной группой, предпочтительно теноильной, X - атом галогена или другой анионно легко отщепляемый радикал, может быть переведен в сложный или простой эфир формулы
В
Ri, R2) RS имеют приведенные значения. Циклический эфир формулы II или III гидролизуют, и целевой продукт выделяют известными приемами.
Пример 1. 2-бутирилпросцилларидин А
1 г просцилларидина А в 20 мл абсолютного тетрагидрофурана подвергают реакции обменного разложения с 50 мг и-толуолсульфокислоты и 1 мл триэтилового ортоэфира масляной кислоты при перемешивании и при комнатной температуре. По окончании реакции реакционную смесь нейтрализуют триэтиламином и растворитель упаривают в вакууме (температура бани 50°); Остаток растворяют в 50 мл хлороформа и для гидролиза циклического оротоэфира встряхивают с 50 м.л 2 н. серной кислоты. После двухкратного промывания органический слой сушат над безводным сульфатом натрия, упаривают и остаток перекристаллизовывают из этилацетата. Выход 910 жг (80,5%),т. пл. 213-214°.
Пример 2. 2-бензоилпросциллариди11 А.
1 г просцилларидина А, как в примере 1, вводят во взаимодействие с триметиловым ортоэфиром бензойной кислоты. Для гидролиза
к реакционной смеси добавляют 2 мл воды и еще 50 мг л-толуолсульфокислоты. По окончании расщепления ортоэфира нейтрализуют раствор триэтиламином, упаривают в вакууме (температура бани 50°) затем пе.рекристаллизовывают из этанола. Выход 1,015 мг (84,5%) т. пл. 236-240С.
Аналогичным образо.м получают соединения в примерах 3-14.
Примерз. 2-пропионилпросцилларидин А получают из просцилларидина А и триметилового ортоэфира пропионовой кислоты по примеру 1. Т. пл. 203-207 С.
Пример 4. 2-(у-хлорбутирил)просцилларилин А получают из просцилларидина А и триметилового ортоэфира у-хлормасляной кислоты по примеру 1. Т. пл. 183-184°С.
Пример 5. 2-(циклопропилформил)просцилларидин А получают из просцилларидина А и триметилового ортоэфира циклопропан-, карбоновой кислоты по примеру 1. Т. пл. 196-210°С.
Пример 6. 2-(циклопентилформил)просцилларидин А получают из просцилларидина
А и триметилового ортоэфира циклопентанкарбоновой кислоты по примеру 1. Т. пл.
201-203°С.
Пример 7. 2-(циклогексилформил)просцилларидин А получают из просцилларидина
А и триметилового ортоэфира циклогексанкарбоновой кислоты по примеру 1. Т. пл.
218-223°С.
Пример 8. 2-(циклооктилформил)просцилларидип А получают из просцилларидина А и триметилового ортоэфира циклооктанкарбоновой кислоты по примеру 1.
Пример 9. 2-(циклопентилацетил)просцилларидин А получают из просцилларидина
А и триметилового ортоэфира циклопентилуксусной кислоты по примеру 1. Т. пл. 159-
161°С.
Пример 10. 2-(циклогексилацетил)просцилларидин А из просцилларидина А и триметилового ортоэфира циклогексилуксусной кислоты по примеру 1. Т. пл. 187-190°С.
Пример 11. 2-(р-фенилпропионил)просцилларидин А получают и просцилларидина А и триметилового эртоэфира р-фенилпропионовой кислоты по примеру 1.
Приме.р 12. 2-(Y-фeнилбyтиpил)пpocциллapидин А получают из просцилларидина А и триметилового ортоэфира у-фенилмасляной кислоты по примеру 1.
При м е р 13. 2- (rt-фторбензоил) просцилларидин У получают из просцилларидина А и триэтилового ортоэфира «-фторбензойной кислоты по примеру 1. Т. пл. 154-160°С.
Пример 14. 2-(д-хлорфенилацетил)просцилларидип А получают из просцилларидина
А и триэтилового ортоэфира (д-хлорфенилуксусной кислоты) по примеру 1. Т. пл. 132-
142°С.
П р и м е р 15. 2-нроиионил-4-циклопропионил-иросцилларидин А. 1 г просцилларидина А, аналогично примеру 1, подвергают реакции обменного разложения, раствор упаривают, остаток растворяют в пиридине и при перемеи1ивании и охлаждении льдом подвергают реакции обменного разложения с 1 мл хлорапгидрида циклопропапкарбоновой кислоты. После обычной обработки - удаления растворителя, встряхивапия с 2 п. соляной кислотой, промывки водой, сушки над Na2SO4 и упаривания - перекристаллизовывают из этилацетата - петролейпого эфира. Т. ил. 190-195°С. Выход 79% теории. Аналогично примеру 15 получают следующие соединения. Пример 16. 2, 4- (дипропионил)просцилларидин А получают из просцилларидина, триэтилового ортоэфира пропионовой кислоты и пропионилхлорида, Т. пл. 135°С. Пример 17. 2, 4-днбутирил-просдилларидин А получают из просцилларидина А, триэтилового ортоэфира масляной кислоты и бутирилхлорида, Т. пл. 112-122°С. Пример 18. 2, 4-дибензоилпросцилларидин А получают из просцилларидина А, триэтилового ортоэфира бензойной кислоты и бензоилхлорида. Пример 19. 2, 4-дициклопропилформилпросцилларидин А получают из просцилларидипа А, три.метилового ортоэфира циклопропанкарбоновой кислоты и хлорангидрида циклопропанкарбоновой кислоты. Т. пл. 132- 134°С. Пример 20. 2- (у-хлорбутирил) -4-циклопропилформилпросцилларидин А получают из просцилларидина А, триметилового ортоэфира Y-хлормасляной кислоты и хлорангидрида циклопропанкарбоновой кислоты. Т. пл. 105- 117°С. Пример 21. 2-бензоил-4-теноилпросцилларидип А получают из просцилларидина А, триметилового ортоэфира бензойной кислоты и тен (2) оилхлорида, Т. пл. 164-170°С. Пример 22. 2-ацетил-4-метокси-просцилларидин А. I г просцилларидина по примеру 1, подвергают реакции обменного разложения с триэтиловым ортоэфиром уксусной кислоты. После нейтрализации реакционной смеси триэтиламином растворитель упаривают, остаток растворяют в 30мл абсолютного диметнлформамида и перемешивают с 2 г окиси серебра и 2 мл метилйодида в течение 20 час в затемненном помещении при комнатной температуре. После удаления растворителя в ьакууме перекристаллизовывают остаток из смеси хлороформ-эфир. Выход 787 мг (69,5%). т. пл. 140-148°. Аналогично примеру 22 получают следуюп(ие соединения. Пример 23. 2-нропионил-4-метоксипросцилларидип А получают из просцилларидина А, триметнлового ортоэфира пропионовой кислоты и метилйодида (окиси серебра. Т. пл. 154-156°С..... Пример 24. 2-циклопентилформил-4-меоксипросцилларидин А получают из просциларидинаА,-триметилового ортоэфира циклоентакарбоновой кислоты и метилйодида (окис-и серебра: Т. пл. 123-134°С..,. ; , . : - -:. П р е д .м е т, и .ч обретения Способ получения ацилпроизводных просцнлларидппа А формулы ОН ОСОБ.. рде - алкильная группа с 1-4 атомами углерода, замещенная галогеном или циклоалкильным радикалом; алкильпая группа с 2-4 С-атомами, циклоалкильный радикал с 3-8 атомами углерода или аралкильный или арильный радикалы, ароматическое ядро которых может быть замещено галогеном; метильная группа, в случае если R2, не атом водорода, или ацетильная группа, и R2 - атом водорода, радикал Ri-СО с указанным значением для RI, алкильная группа с 1-3 атомами углерода или гетероароильпая группа, предпочтительно теноильная группа, отличающийся тем, что просцплларпдпн А формулы взаимодействием с ортоэфиром формулы R,-C(OR3)3, где Ri имеет указанные значеПИЯ, а Ra - низшая алкильная группа, переводят в циклический ортоэфир формулы П1.
где Ri и Ra имеют приведенные значения, который может быть далее переведен в простой или.сложный эфир общей формулы IV где Ri, R-г,-Кэ имеют приведенные значения, циклический эфир до или после этерификации частично омыляют, и целевой продукт выделйют известными приемами.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения ацилпроизводных дигоксина | 1972 |
|
SU511015A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ А42»22.БУФАТРИЕНОЛИД-РАМНОЗИДА | 1972 |
|
SU335836A1 |
| СПОСОБ ПОЛУЧЕНИЯ АМИПОЗАМЕЩЕННЫХ ТРЕТИЧНЫХ БУТАНОЛОВ | 1970 |
|
SU429584A3 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОГЕНПРЕГНАДИЕНОВ | 1972 |
|
SU332622A1 |
| Способ получения производных нафтиридинов | 1977 |
|
SU638258A3 |
| Способ получения производных 6- -амидинопенициллановой кислоты | 1975 |
|
SU566843A1 |
| Способ получения производных имидазо (1,2-а) симм-триазина | 1974 |
|
SU519135A3 |
| Способ получения производных оксиндола или их солей | 1972 |
|
SU464110A3 |
| СПОСОБ ПОЛУЧЕНИЯ АМИНОФЕПИЛ-ЦИКЛОАМИДИНОВ ИЛИ ИХ СОЛЕЙ | 1973 |
|
SU404240A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3,3-ТРЕХЗАМЕ1ЦЕННЫХ 3-АЗОЛИЛПРОПИНОВ | 1971 |
|
SU430551A1 |



Даты
1974-03-15—Публикация
1971-12-21—Подача