Изобретение относится к области получения пролзводны.х 4(ЗИ)-.хиназолинона, которые обладают улучн.1енны.ми лекаретвенны.ми евойства.мн и .могут найти нримененне в фармацевтической нро.мышленности. Предложен основанный на известной реакции енособ нолучения нроизводны.ч 4(ЗН)-.хина зол и но на обшей формулы ,,чЛ CH -CH-CH -R (-г, (ГN №)л-| 11 I ЧА где R - связанный через атом азота остаток вторичного амииа алифатичеекого, циклоалифатического или аралифатического ряда с 2--10 атомами углерода или остаток 5-, 6- нлн 7-Членного гстероцзпчличеекого азотсодержг:щего основания, которое может содержать в соответствующе.м случае дополнительны атом азота, атом кнслорода или атом серы; RI - водород, алкил е 1-4 ато.мамп углерода, бензиловый или феииловый остато :, причем оба последнн.х могут в еоответствую цем случае быть замещены -низшими алюиламн, низшими алкокснлами или галоидом нли же нирнднловый остаток; R2 - водород, нитро-, амино-, трифторме 1льная группы, низший алкохс гл с 1-4 атоами углерода; Кз - алкокснл с 1-4 атома.ми углерода; т - числа 1,2 нли 3. а // - 1-4. Способ заключается в том, что 2-ацилампобенза.мнд обшей формулы NH-CH -CH-CHo-K NH-CO-P.; где R, RI, Ro, RS. т и п имеют вышеуказанное значение, ;цнкл зуют в присутствии водоотни.маюших средств с последующим выделением целезы.х соединений )звестны.ми приемами в свободном виде нли в виде соле). В качестве зодоотн П1ающи.х средств нр;:гадны, 3 частиости, .хлорокнсь фосфсра, нятнхлор1 стын фосфор, хлористый тион;1Л, иолнфосфорная кислота и т. |И. Кроме того, можно использовать ангидр.иды или хлорангидриды кислот. При иснользоваи) ангидридов ;LTH .хлораигидрндов, полученны.х из кислот обИ1ей фО:рмулы RI-СООИ, где Ri имеет вышеуказанное значение, анилиро.ванне ортоаминогруппы и последующую циклизацию соединений формулы И можно осуществить г, одну стадию.
Исходные соедине.нпя формулы II получают известными способами.
Пример: 2 - Нитро - 3,4,5 - трнметоксп - К(-Д 13тилампно-р-ок€Ипропил)-бензам: д.
82,6 г (0,3 моль) 2-на1тро-3,4,5-тр1ПД етокспбензоплхлорпда растворяют в 200 мл безводного бензола п при размещиванпп по каплям добавляют в раствор 43,8 г {0,3 моль) y-iuiэтиламино - J5 - оксипропилампна и 30,3 г (0,3 моль) трпэтиламина в 500 мл беззодного бензола. Затем 3 час размешивают с обратным холодильником и по охлаждении концентрируют фильтрат в вакууме. Для дальнеГииел очистки сырой продукт растворяют в разбар,ленной соляной кислоте и после фильтрации ДОВОДЯ - водным раствором поташа ло щелочной реакции. Выделяющееся в виде масла осисвание -растворяют в этилацетате ц несколько раз лромывают водой. После высущнвания над иоташем концентрируют в вакууме н получают 2-иитpo-3,4,5-тpимeтoкcн-N-(Y-диэтиламнно-|:5-оксипропил)-бензаыид в виде желтоватого масла. Выход 91 г (79%).
2-Ннтро - 3,4,6 - тр1 Л етокси-Н- у-Д1 Этпламино-.р- (3,4,5-Т|рнметоксибензоксн) - пропил -бенза.мид.
38,5 2 (0,1 моль) 2-нитро-3,4,5-триметоксн-К(Y - диэ.тилами.но-р-окси пролил) - бензамида п 15,15 г (0,15 моль) триэтиламина растворяют в безводном бензоле (200 мл), после чего при размешивании добавляют раствор 34,5 г (0,15 моль) 3,4,5-триметоксибензоилхлсрида з 150 мл. бензола. Затем реакционную смесь разогревают до кипения н 6 час размешивают прн киненни с об1ратным холодильником. После охлаждения реакционную смесь смешнвают с 300 мл воды, бензольный слой отделяют. Далее бензольный слой встряхивают с -разбавленной соляной КНСЛОТОЙ-. Водный солянокислый раствор доводят водным раствором поташа до щелочной реакции, а выделяющееся в виде масла основание растворяют з этилацетате. Полученный таким образом pacTiBOp этилацетата промывают водой и после высушивания над Боташем концентрируют в вакууме. Для дальнейшей очи-стки сырой продукт перекристаллизовывают из спирта. Получают 2-нитро - 3,4,5-триметокси-К- у-диэтила.1ино-р(3,4,5-триметокснбензокси)-пропил - бензамид в виде бледножелтых кристаллов; т. ил. 107°С. Выход 46 г (79,5%).
2-Амино - 3,4,5-триметоксп - М- у-диэтиламнно-|3-(3,4,5-триметокснбензокси)-пролил - бейзам ид.
58 г (0,1 моль 2-нитро-3,4,5-триметокси-К у-диэтила.миио- 3-(3,4,5-триметоксибеизокси) .ироиил -бензамида растворяют в 250 мл метанола н по дабавлении никеля Ренея гидрируют лри 30-40° (при 70 атм, давления водорода. Затем отсасывают от катализатора и фильтрат концентрируют в вакууме досуха. Маслянистый остаток растворяют в этилацетате и осаждают путем добавлення эфирной соляной кислоты дигидрохлорид 2-aMiiiHO3,4,5-триметокси - Ы- у-диэтиламиио - р - (3,4,5триметоксибензокси)-проннл -бензамида в виде бесцветных игл; т. разл. 75°С. Выход 49 г (78,7%).
2-Метил-3- у-ДИЭтиламиио-р-(3,4,5-тримето ксибензокси)-иропил-6,7,8-триметокси - 4(ЗН)хиназолииои.
54,9 г (0,Ьно./гь) 2-амино-3,4,5-триметоксн-М -днэтиламн.но-р- (3,4,5-триметокси|бензокси) |ПрО|Г1Ил -бензамида растворяют ,в 250 мл ацетангидрида, после чего 16 час размешивают с обратным холодильником. По охлаждении реакционный раствор концентрируют в вакууме. Остаток смешивают с водным раствором соды, а выделяющееся в виде -масла основание растворяют в этилацетате. После высушивания над ноташем ири введении хлорводород«ого газа в раствор этилацетата получают гидро.хлорнд 2-метил-3- у - диэтилам 1но - р (3,4,5-триметокскбензокси) - пропил -6,7,8-тркметокси-4(ЗН)-хиназолиноиа в виде бесиветиых-игл, т. п. 148°С. Выход 26 г (43,5%).
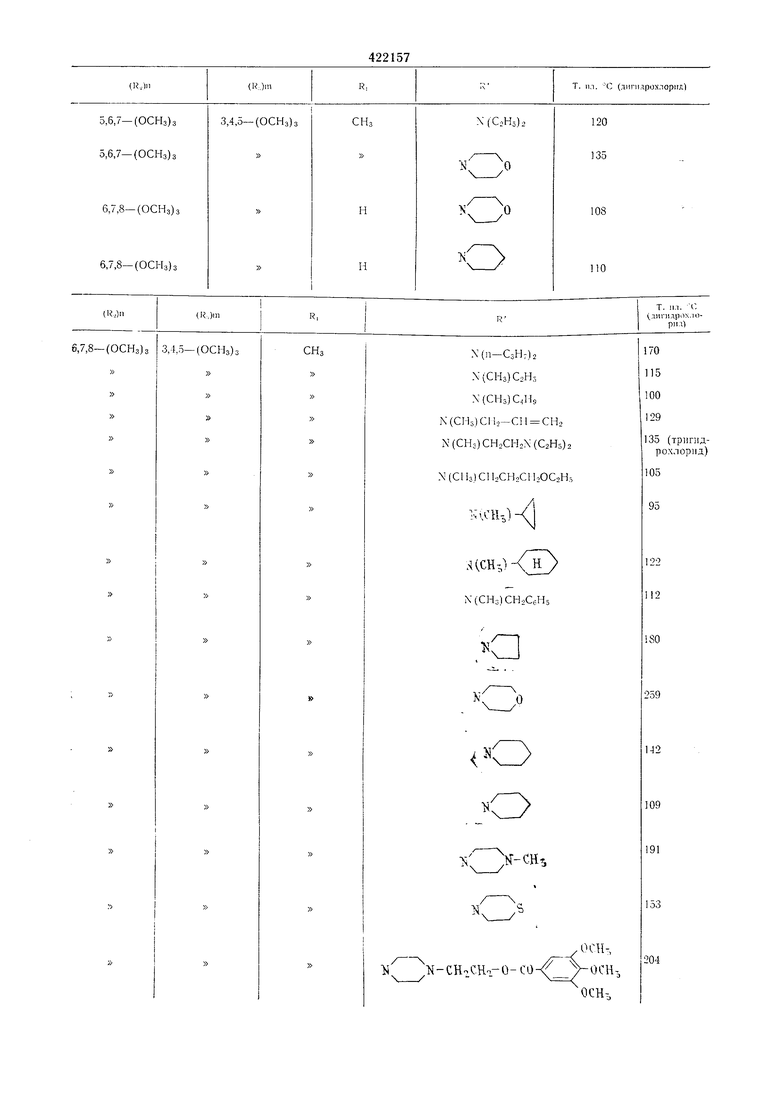
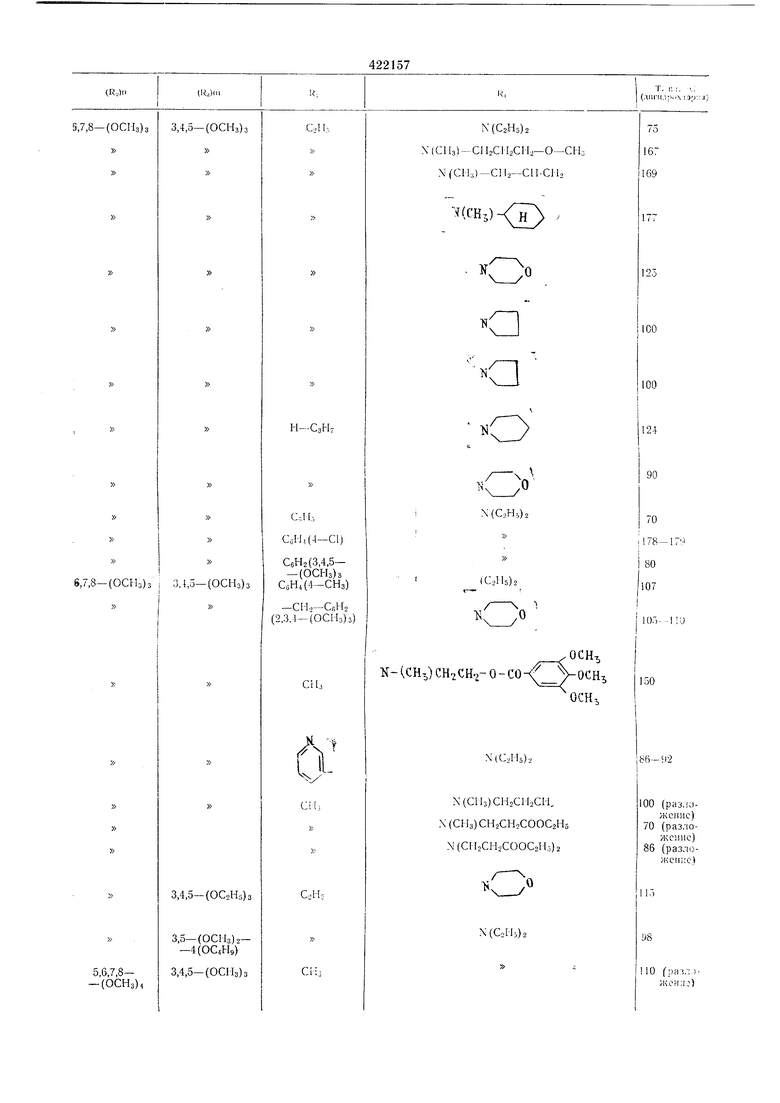
Аналогично приведенным пр-имерам можно получнть соединення, указанные в таблиие.
О
СНгСН-СЩ-В
i
/ R, СО
П-СЕДп
(ОСНз)з
3,4,5-(ОСНз)з (ОСИз)з
(ОСНз)з (ОСИз)з
т. 11,1. -с (лигпдрохлорп/Л
Х(СоН5)2
120
135
N .0
108
Ш Если сначала ацилировать 2-aмипo-3,4,5-тpи мeтoкcи - К- у-Диэтиламино-р-(3,4,5 - триметоксибензокси) - пропил - бензамид с помощью ацетилхлорида, .получая соответствующее ацетилампновое соединение, п затем циклпзовать его обычным способом с помощью уксусного ангидрида, xлoipoкиcи фосфора, тпонплхлорида, .пятихлористого фосфора или лолпфосфОрной кислоты, то это вещество также получают с большим выходом. Предмет п з о б р е т е п п я Сиособ получения производных 4(ЗН)-хиназолнио.на общей формулы
(
где R - связанный через атом азота остаток вторичного амина алифатического, циклоалих)атического или аралифатического ряда с .2-10 атомами углерода или остаток 5-, 6- или 7-членного гетероциклического азотсодержаjuero осиования, которое может содержать
20
CD
.
}.H-CO--R;
vRb).
где R, Ri, R2, Rs, т и п имеют вышеуказанное значение, цпклнзуют в присутствии водоотщепляющих средств, с последующим выделением целевых соединений известными приемами в свободном виде или в виде солей. полнительио атом азота, атом кислорода или атом серы; RI - водород, алкил с 1-4 атолшмп углерода, бензиловый или фениловый остаток, причем оба последних могут в соответствующем случае быть замещеиы низшими алкилами, низшими алкоксилами или галоидом, или же пиридиловый остаток; R2 - водород, иитро-, амино-, трифторметильная групяа, низший алкоксил с 1-4 атомами углерода: Rs - алкоксил с 1-4 атомами углерода; m - числа 1,2 или 3, а п - числа 1,4, or.ufчающийся тем, что 2-ациламипобеизамид общей формулы


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,2,|3-БЕНЗОТРИАЗИН-4(ЗН)-ОНА | 1972 |
|
SU334699A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2,4- | 1972 |
|
SU331553A1 |
| Способ получения производных алкоксикоричной кислоты | 1974 |
|
SU543340A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2,4- | 1972 |
|
SU335839A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ | 1971 |
|
SU416944A3 |
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВПОЗАМЕЩЕННЫХ ПРОИЗВОДНЫХ 1 | 1972 |
|
SU428602A3 |
| Способ получения производных простых ариловых эфиров или их фармацевтически приемлемых солей (его варианты) | 1980 |
|
SU997606A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПИПЕРАЗИНА | 1970 |
|
SU271412A1 |
| Способ получения производных 1-фенокси3-аминопропан 2-ола | 1973 |
|
SU493958A3 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ФЕНОКСИ-2-ГИДРОКСИ-3- ЦИКЛОАЛКИЛАМИНОПРОПАНОВ ИЛИ ИХ СОЛЕЙ | 1972 |
|
SU327664A1 |


Авторы
Даты
1974-03-30—Публикация
1971-04-23—Подача