Согласно предлагаемому изобретению, новые производные пиридина получаются путем конденсирования 3-гидразин-пиридина или его производных или продуктов переработки 2-гидразин-пиридина с алифатическими или смешанными алифатически ароматическими альдегидами или кетонами в присутствии или отсутствии растворителей.
Реакции конденсирования могут происходить при обыкновенной температуре, иногда при охлаждении или при повышенных температурах, и при участии конденсирующих веществ.
Конденсирование производных, в особенности галоидных и нитропроизводных 2-гидразин-пиридина с альдегидами и кетонами представляет особенный интерес в том отношении, что присутствие таких групп создает возможность изготовлять особенно ценные терапевтические продукты. Так, например, нитрогруппу можно перевести в аминогруппу, а эту далее опять заменить разными другими ценными заместителями.
Изготовление продуктов конденсации из 3-гидразин-пиридина и его производных иллюстрируется несколькими примерами.
Пример 1. Полученный диазотированием 3-аминопиридина и последующим восстановлением хлористым оловом 3-пиридил-гидразин заливается в избытке бензальдегидом. Продукт реакции, после некоторого стояния, промывается эфиром и перекристаллизовывается из алкоголя. Таким образом получают желтоватые иглы с точкой плавления 165-166°.
Пример 2. К 1 мол. 2-хлор-3-гидразин-пиридина прибавляют 1 мол. ацетоуксусного эфира; происходит конденсация с выделением тепла. Перекристаллизовав реакционную смесь из алкоголя, получают продукт конденсации в виде снежнобелых чешуек с точкой плавления 123-124°.
Пример 3. Приблизительно молекулярные количества 2-гидразин-5-нитро-пиридина и ацетоуксусного сложного эфира смешивают при нормальной температуре. Конденсация происходит с самопроизвольным разогреванием; постепенно масса застывает, при перемешивании, в твердое желтое тело. Выкристаллизовывается из алкоголя в желтых чешуйках с точкой плавления 93-95°.
Пример 4. 2 гидразин-5-нитро-пиридин растворяют в избытке ацетона и раствор оставляют на короткое время в покое. Затем избыток ацетона удаляют на водяной бане; оставшийся продукт промывают водой. После кристаллизации из лигроина получают желтые чешуйки с точкой плавления 163°.
Пример 5. То же количество исходного материала растворяется в 50% уксусной кислоты и заливается рассчитанным количеством бензальдегида. Продукт конденсации осаждается в виде лимонно-желтых хлопьев. После кристаллизации из алкоголя получают золотисто-желтые иглы с точкой плавления 226-228°.
Дальнейшие опыты показали, что при применении высоких температур, преимущественно превышающих 100°, реакции конденсирования могут быть продолжены далее, например, таким образом, что полученный (пример 3) из 2-гидразин-5-нитропиридина и ацетоуксусного эфира продукт конденсации подвергают нагреванию до температуры свыше 100°; при этом в боковой цепи замыкается кольцо и получается 5-нитро-2-пиридил-3′-метил 5′-пирозалон. Вместо того, чтобы сначала изготовить простые продукты конденсации и их затем в отдельных случаях, после предварительной изоляции, нагреванием подвергать дальнейшей переработке, можно поступать таким образом, что компоненты, т.е. например, 2-гидразин-5-нитропиридин с ацетоуксусным сложным эфиром нагревают сразу до температуры, необходимой для замыкания кольца в боковой цепи. В таком случае реакция протекает по следующему уравнению:
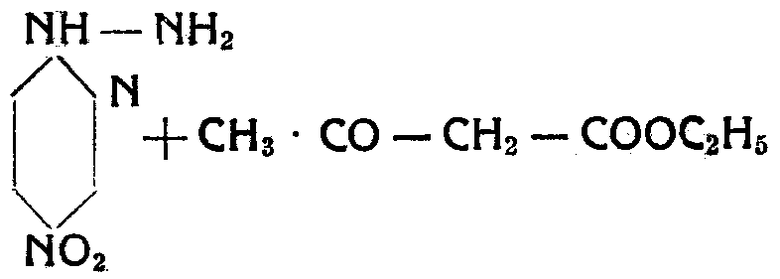
Пример 6. 2-гидразин-3-нитропиридин нагревают с молекулярным количеством или с небольшим избытком ацетоуксусного эфира в продолжение 6 часов до 120°. Получается твердая масса, которую превращают в порошок и перекристаллизовывают из большого количества алкоголя. Продукт выкристаллизовывается тонкими желтыми иглами, распадающимися между 240 и 260° без определенной точки плавления. Выход почти теоретический. В кислотах продукт растворяется с образованием бесцветного раствора, при нейтрализации выпадает снова, и в избыточной щелочи снова переходит в раствор с желтой окраской.
Пример 7. Приблизительно молекулярные количества 2-гидразин-5-нитропиридина и ацетоуксусного эфира смешиваются при нормальной температуре. Конденсация наступает при самонагревании; постепенно масса застывает при непрерывном перемешивании в твердое желтое тело.
Полученный таким образом промежуточный продукт, в случае надобности, после перекристаллизации может быть подвергнут нагреванию в масляной бане, при указанных в примере 1 условиях, и дает тот же продукт.
Согласно другой форме выполнения изобретения продукты конденсации, полученные из 3-гидразин-пиридина или производных 3-гидразин-пиридина и 2-гидразин-пиридина, могут быть переработаны далее таким образом, что их обрабатывают отщепляющими аммиак средствами, как хлористый цинк, спиртовый раствор хлористого водорода и т.п. Таким образом можно получить бициклические производные пиридина. При этом нет безусловной необходимости выделять промежуточные продукты, получаемые при конденсировании гидразин-пиридина с альдегидами и кетонами.
Пример 8. Изготовление 2-метил-5-хлор-пириндоля.
25 г продукта конденсации, полученного из ацетона и 2-хлор 5-гидразин-пиридина медленно нагревают с избытком хлористого цинка в масляной бане при постоянном размешивании до 200°. Сперва светло-коричневый сплав при этом темнеет. Полученную реакционную смесь растворяют в теплой воде с небольшой примесью соляной кислоты, затем подщелачивают и извлекают эфиром. После удаления эфира получают коричневые кристаллы, которые перекристаллизовывают с примесью животного угля; точка плавления 208-210°. Кристаллы растворяются в эфире, алкоголе, горячем толуоле и бензоле; в лигроине растворяются тяжело. Выход около 50%.
Пример 10. Изготовление 3-метил-5-хлор-пириндола.
Полученные из 2-хлор-3-аминопиридина и пропионового альдегида продукты конденсации обрабатываются избытком хлористого цинка, согласно примеру 9. При аналогичной обработке получают производную пириндола в форме белых волокнистых кристаллов с точкой плавления 190-202°, растворимых в эфире, алкоголе, горячем толуоле и бензоле и минеральных кислотах; в лигроине растворяются с трудом. Выход около 50%.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения мезо-амина-акридина и его производных | 1926 |
|
SU7960A1 |
| Способ получения производных пиридо-(3,2-е)-асимм-триазина или их солей | 1975 |
|
SU576941A3 |
| Способ получения кубовых красителей | 1928 |
|
SU14509A1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЛИ 3-ЭТИЛ-5-МЕТИЛ-2-(2-АМИНОЭТОКСИМЕТИЛ)-4-(2-ХЛОРФЕНИЛ)-6-МЕТИЛ-1,4-ДИГИДРО-3,5-ПИРИДИНДИКАРБОКСИЛАТА И БЕНЗОЛСУЛЬФОКИСЛОТЫ (БЕЗИЛАТА АМЛОДИПИНА) | 1998 |
|
RU2163597C2 |
| Способ получения производных изохинолина | 1972 |
|
SU539524A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,4-ДИГИДРОПИРИДИНА | 1972 |
|
SU357726A1 |
| Способ получения 1-замещенных пиразолонов-5 или их солей | 1974 |
|
SU545258A3 |
| Способ получения производных пурина или их солей | 1977 |
|
SU751325A3 |
| Способ получения аралкиаминов и их дериватов | 1926 |
|
SU12236A1 |
| ПРОИЗВОДНЫЕ МЕТИЛПИПЕРАЗИНАЗЕПИНА ИЛИ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ ЭТИХ ПРОИЗВОДНЫХ | 1991 |
|
RU2111966C1 |
1. Способ приготовления продуктов конденсации гидразин-пиридинов с альдегидами или кетонами, отличающийся тем, что конденсации с альдегидами или кетонами подвергают 3-гидразино-пиридин или замещенные в ядре производные 2- или 3-гидразин-пиридина.
2. Прием выполнения означенного в п. 1 способа, отличающийся тем, что конденсацию гидразин-пиридинов производят с ацетоуксусным эфиром с целью получения производных пиразолона.
3. Прием выполнения означенного в пп. 1 и 2 способа, отличающийся тем, что в качестве замещенных в ядре производых 2-гидразин-пиридина применяют галоидо- или нитросоединения.
4. Способ превращения означенных в пп. 1-3 продуктов конденсации в производные пириндола, отличающийся тем, что полученные продукты конденсации обрабатывают отнимающими аммиак средствами, как например, хлористым цинком или алкогольной соляной кислотой.
Авторы
Даты
1935-04-30—Публикация
1924-09-11—Подача