Изобретение относится к способу получения новых 18-метиленстероидов, обладающих физиологической активностью. Известен способ отщепления сульфогруппы под действием оснований. Применение известного способа позволило получить не описанные ранее стероидные соединения, обладающие ценными свойствами. Предлагаемый способ получения 18-метиленстероидов р-яда -лрегнана формулы I СН2 СНз где X - атом водорода или метильная группа; R - атом водорода, свободная или этерифицированная в сложный эфир оксигруппа, в которых в положениях 6,7 и в соединениях, где X - метильная группа, в положениях 6,7 и/или 1,2 может иметься еще одна двойная связь, заключается в том, что соединение формулы И имеющее двойные связи, исходящие из углеродного атома в положении 5, где X - атом водорода или метильная группа; RI - свободная или этерифицированная в сложный эфир оксигруппа вместе с атомом водорода или свободная или кетализованная оксогруппа; R-атом водорода или свободная или этерифицированная в сложный эфир оксигруппа; Ra - углеводородный остаток, обрабатывают сильным основанием, а в случае, когда Ri обозначает оксигруппу, то ее окисляют до 3-оксогруппы, когда Ri - кетализова нная оксогруппа, то ее переводят в свободную оксогруппу и целевой продукт выделяют или переводят в сложные эфиры известными приемами. В качестве основания применяют алкоголяты щелочного или щелочноземельного металла или амиды щелочного металла. Реакцию проводят при О-100°С; 3-кетализованную оксигруппу переводят в свободную путем обработки 60-80%-ной уксуспой или сульфоновой кислотой, преимущественно птолуолсульфоновой кислотой. Окисление 3оксигруппы до 3-оксогруппы осуществляют по методу Оппенауера. Исходное вещества получают согласно схеме. Пример 1. 14 мг ,3-этилeндиoкcи-18мeзилoкcи-20-oкcи-18a, 20-цикло-18-гомопрегнена, растворенные в 1 мл г/)ег-бутанола, прибавляют к 14 мг г/(гг-бутилата калия и перемешивают в атмосфере азота в течение 16 час при 60°С. Реакционную смесь охлаждают, к ней Прибавляют 0,1 мл ледяной уксусной кислоты, разбавляют льдом и водой и трижды экстрагируют метиленхлоридом. Вслед за тем растворы метиленхлорида промывают насыщенным раствором бикарбоната натрия, сушат и выпаривают в вакууме, получаемом с помощью водоструйного насоса. Получаемый сырой 18-метиленпрогестерон-З - монокетал (около 11 мг) растворяют в 2,5 мл ацетона, прибавляют 6 мг п-толуолсульфоновой кислоты и оставляют стоять при комнатной температуре. После переработки и последующей препаративной тонкослойной хроматографии сырого продукта на силикагеле (система толуол-уксусный эфир 4:1) получают 3 мг чистого 18-метиленпрогестерона, т. пл. 193 - 195°С. Исходное вещество можно получить следующим образом. 1,00 г ,3-этнлендиокси-20||3-оксиирегнен18-кислотный (18-20)-лактона растворяют в 25 мл толуола, прибавляют 25 мл раствора 2н. метилхлорида магния в тетрагидрофуране и кипятят в атмосфере азота в течение 4 лТ,ней с обратным холодильником. Охлажденную до температуры около 5°С реакционную смесь затем осторожно выливают, сильно перемещивая, на с .;есь льда и 100 мл -насыщенного раствора хлористого аммония. Водную фазу отделяют и дополнительно экстрагируют смесью простого эфира и метиленхлорида (4: 1), органический раствор по очереди промывают насыщенным раствором хлористого аммония и водой, сушат и выпаривают в ва кууме, получаемом с помощью водоструйного насоса. Получаемый кристаллический сырой продукт (1,0 г), представляющий собой (после тонкослойного хроматографирования) смесь ,3этнлепдыокси-18-метил-оксо-20р - оксипрегнена и А5-3,3-этилендиокси-18-метилен-18, 20оксидопрегнена, плавящуюся при 153-156°С, окисляют без очистки следующим образом. 1,0 т сырой смеси растворяют в 3 мл пиридина, прибавляют к окислительной смеси, полученной из 1,0 г окиси хрома (VI) и 15 мл пиридина, и реакционную смесь оставляют стоять в течение 40 час при комнатной температуре. После разбавления уксусным эфнром отфильтровывают от нерастворимых компонентов, остаток дополнительно промывают уксусным эфиром и фильтрат выпаривают в вакууме, получаемом с помощью водоструйного насоса. Полученный сырой продукт растворяют в метиленхлориде и фильтруют через загруженную,20 г основной окиси алюминия колонну. Из упаренного фильтрата получают -после однократной перекристаллизации из смеси метиленхлорида, простого эфира и петролейного эфира 719 г чистого 18-метил18-оксопрогестерон-З-монокетала, т. пл. 178- 180°С. К раствору 600 мг трет-бутилата калия в 25 мл т/оег-бутанола прибавляют 1,21 г 18метил-18-оксопрогестерон-З-монокетала и неремещивают в атмосфере азота в течение 25 мин нри комнатной температуре. Затем охлаждают до температуры около 10°С, прибавляют 2,5 мл ледяной уксусной кислоты, выливают на ледяную воду и трижды экстрагируют метиленхлоридом. Экстракты нромывают водой, насыщенным раствором карбоната натрия и вновь водой, сушат и упаривают в вакууме, получаемом с помон ью водоструйного насоса. Из остатка (1,2 г) получают после однократного растворения из смеси метиленхлорида и простого эфира 941 мг чистого д5,18а.2о . 3-3-этилендиокси - 18-оксо-18а, 20цикло-18-гомопрегнадиена с т. пл. 211-213°С. К раствору 820 мг полученного таким образом соединения в 8,5 мл метиленхлорида и 34 мл метанола прибавляют по каплям в течение 5 мин, перемешивая, при 50°С 12,6 мл 30%-ной перекиси водорода и 4,25 мл 10%ного натрового щелока и затем мутную смесь оставляют стоять в течение 60 час при 4°С. Затем разбавляют водой, экстрагируют трижды при охлаждении льдом, хлороформом, органические фазы промываю г водой до нейтрального состояния, супшт и упаривают в вакууме, получаемом с помощью водоструйного насоса. Из полученного таким образом аморфного остатка получают после кристаллизации из простого эфира 691 г чистого А-3,3этилендиокси-18-оксо-18а, 20-оксидо-18а, 20цикло-18-гомопрегнена, т. пл. 195-196°С. К суспензии 150 ыг литийалюминийгидрида в 10 мл тетрагидрофурана прибавляют при охлаждении (около 10°С) раствор 500 мг полученной эпокиси в 20 мл тетрагидрофурана и реакционную смесь кипятят в течение 5,5 час с обратным холодильником. Избыточный восстановитель затем разлагают, охлаждая прибавлением смеси 1,5 мл тетрагидрофурана и 0,75 мл уксусного эфира и затем 1,5 мл тетрагидрофурана и 0,75 мл воды. Выпавшую гидроокись алюминия и лития отфильтровывают на нутче после прибавления безводного сульфата натрия и фильтрат выпаривают в вакууме, получаемом с помощью водоструйного насоса. Остаток (500 мг) растворяют с целью очистки в смеси толуола и уксусного эфира (4:1) и хроматографируют на пятидесятиКратном весовом количестве безводного силикагеля. С помощью такой же
смеси растворителей элюируют 185 мг чистого ,3-этилендиокси-18, 20-диокси-18а, 20цикло-Ю-гомопрегнена, плавящегося после повторного растворения из смеси нетиленхлорида, метанола и простого эфира (172 мг) при 206-207°С.
150 мг полученного таким образом соединения растворяют в 1 мг пиридина, охлаждают приблизительно до -10°С, прибавляют 0,1 мл хлорида метансульфоновой кислоты и оставляют стоять в продолжение 18 час при температуре 0°С. После обычной переработки получают 107 мг пены, из которой кристаллизацией из смеси метиленхлорида и простого эфира получают 32 мг А-3,3-этилендиокси-18мезилокси-20-окси-1 За, 20-цикло-18-гомопрегнена, т. пл, 135-137°С (с разложением).
Пример 2. К смеси 10 мл диметилформамида и 1 мл тгег-бутапола прибавляют, перемешивая, 700 мг т.пег-бутилата калия. ПрИ -20°С -прибавляют 0.6 мл триэтилфосфита и через реакционный раствор проводят не слишком сильный поток кислорода. При неизменяющейся температуре прибавляют в течение 5 мин 0,1 г Л -Зр-ацетокси-18-метилен-20-оксопрегнена и смесь размешивают еще 30 мин, проводя поток кислорода. Затем, охлаждая, осторожно ПОДКИСЛЯЮТ и обрабатывают метиленхлоридом. Получаемый сырой продукт суспендируют с 2 мл ледяной уксусной кислоты, перемешивая и пропуская азот, прибавляют в течение 45 мин 1,2 мл трифторацетангидрида и продолжают перемешивать еще 4 час при комнатной температуре. Реакционную смесь выливают в -волу и обрабатывают простым эфиром. Хроматографической очисткой полученного таким образом сырого продукта получают чистый , 17а-диацетокси-18метилен-20-оксопрегнен. ИК-спектр: полосы при 5,75. 5,81, 6.10, 8.15 и 9,75 мкм.
П ри мер 3. К 1,27 г ,3-этилендиокси-18тозилокси-20-окси-18а. 20-цикло-18-гомопрегнена, растворенных в 42 мл т/7ег-бутанола и 10 мл диоксаиа, прибавляют 1,27 г грет-бутилата калия и размешивают в атмосфере азота в течение 17 час при 40°С. Смесь охлаждают, прибавляют 5,3 мл ледяной уксусной кислоты и разбавляют холодной как лед водой; осаждающийся осадок фильтруют на путче и промывают водой. Остаток растворяют в хлороформе, промывают до нейтрального состояния водой, насыщенным раствором бикарбоната натрия и опять водой, сушат и выпаривают досуха в получаемом с помощью водоструйного насоса вакууме.
Аморфный продукт очищают, растворяя в толуоле, и хроматографируют на пятидесятикратном весовом количестве силикагеля. Смесью толуола и уксусного эфира (95 : 51 элюируют смесь вещества, СОСТОЯЩУЮ из ,3-этилендиокси-18 - метилен-20-оксопрегнена и его эпимера А-3,3-этилендиокси-18-метилен-20-оксо-17р-Н-прегнена. 167 мг этой смеси растворяют в 3 мл ацетона и оставляют стоять (после прибавления 15 мг п-толуолсульфоновой кислоты) в течение 16 час при комнатной температуре. После разбавления ледяной водой экстрагируют дважды смесью простого эфира и метилена (4: 1), после чего органические фазы промывают водой, насыщенным раствором бикарбоната патрия и опять водой до нейтрального состояния сушат над сульфатом натрия п выпаривают досуха в получаемом при помощи водоструйнего «асоса вакууме. Препаративной тонкослойной хроматографией сырого продукта на силикагеле (средство, способствующее текучести, смесь цихлогексана и ацетона ПО ; 10) получают чистый 18-метиленпрогеотер У1 с
т. пл. 194 - 196°С и изомерный 18-метплен17р-Н-прогестерон, т. пл. 134-136 С.
18-Тозилоксисоединение (исходное вещество) ИЗ.ГОТОВЛЯЮТ следующим образом.
1,0 г А-3.3-этилендиокси-18. 20-липкгт-18а.
20-цикло-18-гомопрегнена растворято- р 1i -л пиридина, прибавляют 2.45 г хлорида Г - ОЛУолсульфоновой кислоты и разме ппряпт в течение 65 час при комнатной тeмпppят pe. Яатем разбавляют ледяной водой. ЭКСТПЛГППУЮТ
дважды хлороформом, органические чкстпякты промывают празбавленной соляной кцглотой, затем до нейтрального состояния насыщенным раствором бикарбоната натрия и опять водой, сущат над сульфатом натрпя и
выпаривают в получаемом с помощью водоструйного насоса вакууме.
Пример 4. Применяя описанный предыдущем примере способ для А-3-ок -1 -тоЗИЛОКСИ-20-ОКСИ-18, 20-цикло-1В-могопрегттена. получают А-3-окси-18-метилен-20-оксог1ПРГ1«н. Последний ацети,пируют в положении 3 полученный продукт переводят в 17 а-япртоксипроизводиое. После селективного омылент я в
положении 3 полученный продукт обрабатывают, как следует ниже.
1.00 г А -Зр-окси-17-а-ацетокси-18-метт1лен20-оксопрегнена растворяют в смегя ЯП мл толуола и 20 мл циклогексанона. Отгон от
60 мл толуола и прибавляют зате 1.8 г раствора алюминийизопропилата в 50 мл в то время, как отгоняют еще 30 мл толуола. Вслед затем прибавляют 20 мл толУола и реакпионную смесь кипятят затем в атмосфере
азота с обратным холодильником в течение 15 час. Затем прибавляют к охлажденно у раствору холодный как лед раствор сепной кислоты, метиленхлорида и простого эфира. Затем отделяют органический слой, промывают раствором бикарбоната натрия и водой, сушат и выпаривают в вакууме. Л аслянистый остаток перегоняют с вопяным и перерабатывают обычным образом. Полл-ирттиый сырой продукт очищают путем хппмтт-от-ряфии на силикагеле и пррекг)игтп--т, ртт-т оиз смеси метиленхлорида и эЛипя л. 3,20-диоксо-17а-ацетокси- 8 - МРТИТРН ПРПТРН (18-метилен-17а-ацетоксипрогестерон) показывает в ультрафиолетовом спектре полосы
при 5,75, 5,85, 6,01, 6,24, 8,15 и 9,70 мкм,
Исходное вещество получить путем частичного омыления , 17а-диацетокси18-метилен-20-оксопрегнена посредством воднометанольнОГО раствора бикарбоната калия и путем взаимодействия с хлорангидридом птолуолсульфокислоты в пиридине три «омнатной температуре.
Предмет изобретения
1. Способ получения 18-метиленстероидов ряда прегнана формулы I
сд сн.
где X - атом водорода или метильная Группа; R - атом водорода, свободная или этерифицированная в сложный эфир оксигруппа, в которых в положениях 6,7 и
в соединениях, где X - метильная группа, в положениях 6,7
и/или 1,2 может иметься еще одна
двойная связь.
отличающийся тем, что соединение формулы II
имеющее двойные связи, исходящие из углеродного атома в положении 5, где X - атом водорода или метильная группа;
RI - свободная или этерифицированная в
сложный эфир оксигруппа вместе с
атомом водорода или свободная или
кеталиЗОванная оксогрупиа;
R - атОМ водорода или свободная или
этерифицированная в сложный эфир
оксигруппа;
R2 - углеводородный остаток, обрабатывают сильным основанием и, когда RI обозначает оксигруппу, то ее окисляют до 3-оксогруппы, когда Ri - кетализоваииая оксогруппа, то ее переводят в свободную оксогруппу и целевой продукт выделяют или переводят в сложные эфвры известными приемами.
2.Способ по п. 1, отличающийся тем. что в качестве сильного основапия примепяют, например, алкоголяты щелочного или щелочноземельного металла или амиды щелочиого металла.
3.Способ по ПИ. 1 и 2, отличающийся тем, что 3-кетализованную оксогруппу переводят в свободную путем обработки 60-80%ной уксусной или сульфоновой кислотой, преимущественно ге-толуолсульфоновой кислотой.
4.Способ по пп. 1 и 2, отличающийся тем, что окисление З-оксигруппы осуществляют по методу Оппенауера.
Конвенционный приоритет по признакам:
22.12.67при X - метильная группа.
25.11.68при X - атом водорода, о о сн %/ Ч
он
он
НО СН, /RSO,-0. СИ, /
с-сн, с-снз
СН.. сНьО СНчч/СНь СО со



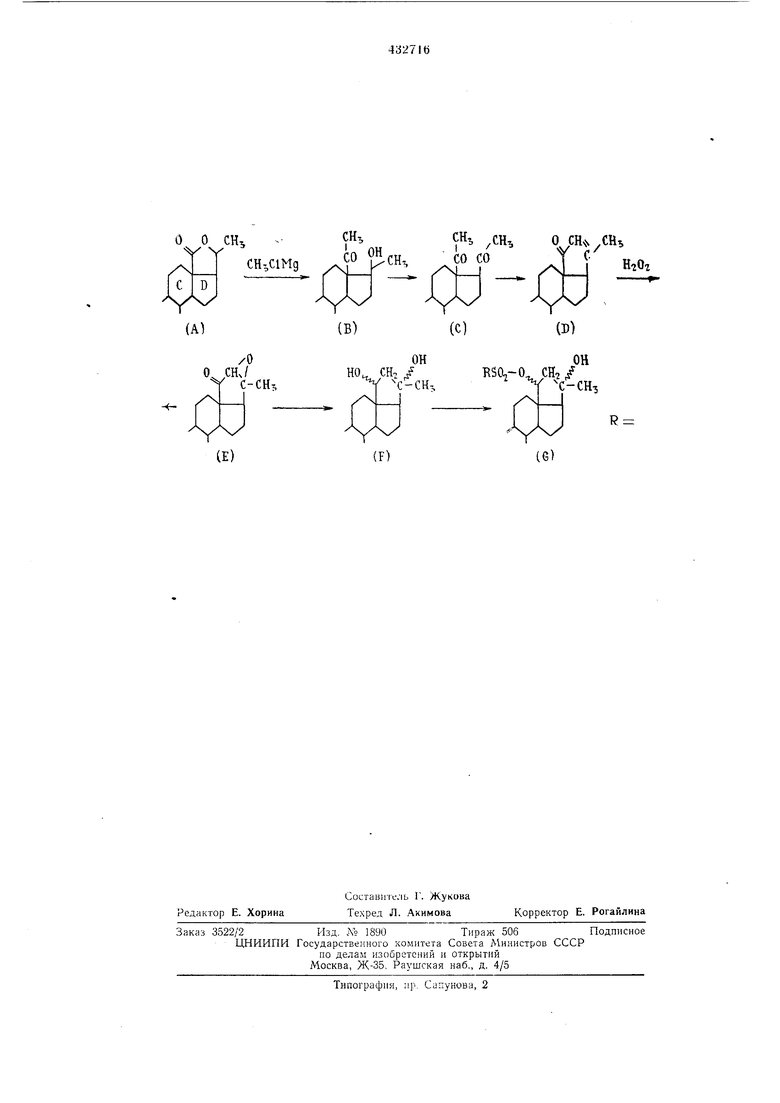


Даты
1974-06-15—Публикация
1968-12-20—Подача