1
Изобретение относится к новому способу получения новых соединений, а именно 2-замещенных 4,6-дихлор-4-тиахиназолинов формулы I
V
N
С1
С1
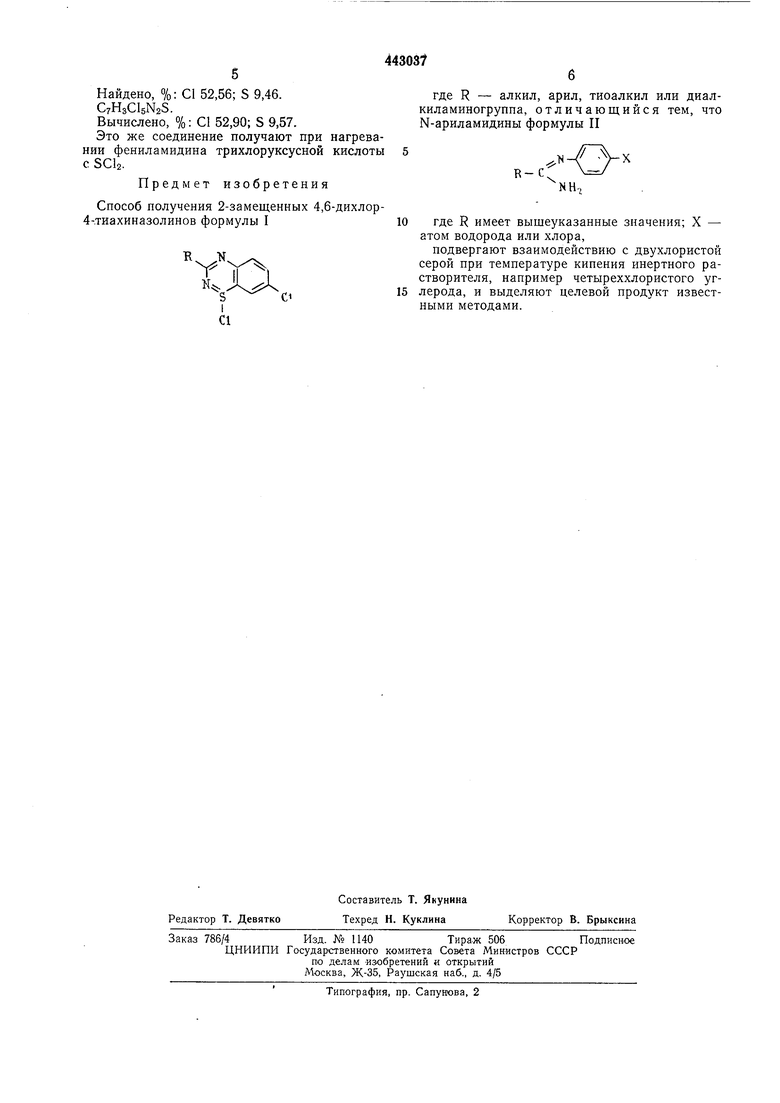
где R - алкил, арил, тиоалкил или диалкиламиногруппа, которые могут найти применение в синтезе различных производных тиахиназолина (с амино-, алкокси- и другими группами в тиахиназолиновом цикле), обладаЕОЩих физиологически активными свойствами.
Предлагаемый способ заключается в том, что N-ариламидины формулы И
R-C
где R имеет вышеуказанные значения; X - атом водорода или хлора,
подвергают взаимодействию с двухлористой
серой при температуре кипения в среде инертного растворителя, например четыреххлористого углерода, и выделяют целевой продукт
известными методами.
При взаимодействии двухлористой серы с фениламидинами трихлоруксусной кислоты или бензойной кислоты (где X - атом водорода) образование тиахиназолинового цикла сопровождается хлорированием фенильных радикалов.
Образование новой гетероциклической спстемы подтверждено независимым синтезом.
Например, при взаимодействии бензтиадиазина 1а с хлором получают 2-фенил-4,6-дихлор4-тиахиназолин Ilia
N
СьНз-С N
C-t-HCl
s Cl
(ш)
(la; Хлорирование бензтиадиазина 16 приводит к тиахиназолина III6 образованию 2-трихлорметил-4,6-дихлор-4HN
X
(КП
() При гидролизе описанных в заявке 1,2,4-тиадиазины IV
- -HCl KN
SCi
Cl (Ш)
Строение соединений IV подтверждено независимым синтезом и ИК спектрами. Кроме того, строение тиахиназолинов III подтверждено реакцией с диалкиламинами. Являясь
М-
s II о
Cl (IV)
хлорангидридами N-замещенных иминосульфиновых кислот циклического строения, они легко реагируют с диалкиламинами, давая соответствующие амиды тиахиназолинов III получают 1-оксо-3-К-5,6-бензоI j I -ьЕ.ХгГНа
.N
,/
. „. SLl
I
ИКг

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных хлорметилхинолина | 1983 |
|
SU1516010A3 |
| Способ получения производных бензо/в/тиофена или их солей | 1972 |
|
SU486510A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 0-АНИЛИНО- ФЕНИЛЭТИЛОВЫХ СПИРТОВ | 1973 |
|
SU381217A1 |
| Способ получения производных пирида-зиНОНА или иХ СОлЕй | 1977 |
|
SU845781A3 |
| ЗАМЕЩЕННЫЕ БЕНЗИМИДАЗОЛЬНЫЕ СОЕДИНЕНИЯ, СПОСОБЫ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, ОБЛАДАЮЩАЯ АНТИВИРУСНЫМ ДЕЙСТВИЕМ | 1993 |
|
RU2141952C1 |
| Способ получения производных флавана или их солей | 1979 |
|
SU1072805A3 |
| Способ получения производных фенилимидазолилалкила | 1971 |
|
SU451244A3 |
| 2-САХАРИНИЛМЕТИЛАРИЛКАРБОКСИЛАТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И КОМПОЗИЦИЯ, ИНГИБИРУЮЩАЯ АКТИВНОСТЬ ПРОТЕОЛИТИЧЕСКОГО ФЕРМЕНТА | 1991 |
|
RU2114843C1 |
| Производные 5-(2,4-диэтиленимино)-(симм. триазинил-6) амино-1,3 диоксана, проявляющие противоопухолевую активность , и способ их получения | 1975 |
|
SU507037A1 |
| N-(2-Карбокси-4,6-дихлорфенил)- @ -аланин как исходный продукт для получения 6,8-дихлор-2,3-дигидрохинолин-4(1Н)-она | 1986 |
|
SU1356393A1 |

где R - CfiHs, СС1з.
Пример 1. Получение 2-дихлорфенил-4,6дихлор-4-тиахиназолина.
0,02 г-моль фенилбензамидина, 15-20 мл двухлористой серы и 40 мл ССЦ кипятят в течение 8-10 ч до исчезновения осадка, затем раствор фильтруют. Фильтрат упаривают в вакууме водоструйного насоса. В остатке 2-дихлорфенил-4,6 - дихлор - 4-тиахиназолин. Очистка кристаллизацией из дихлорэтана с добавкой 0,5-1 мл двухлористой серы. Красные нрнзмы, т. пл. 196 -197°С, выход 76%.
Найдено, %: С1 41,44; S 8,67; N 7,64.
CisHfiCUNsS.
Вычислено, %: Cl 39,00; S 8,79; N 7,64.
Пример 2. Получение 2-дихлорфенил-4,6дихлор-4-тиахиназолина.
0,02 г-моль N-rt-хлорфенилбензамидина, 15-20 мл двухлористой серы и 40 мл CCU кипятят в течение 8-10 ч до исчезновения осадка, раствор фильтруют. Фильтрат упаривают в вакууме водоструйного насоса. В остатке 2-дихлорфенил-4,6-дихлор-4-тиахиназолин. Очистка кристаллизацией из дихлорэтана с добавкой 0,5-1 мл двухлористой серы. Красные призмы, т. пл. 196-197°С, выход 79%.
Найдено, %: С1 41,62; S 8,78; N 7,63.
CisHeCUNsS.
Вычислено, %: Cl 39,0; S 8,79; N 7,64.
Пример 3. Получение 2-трихлорметил-4,6дихлор-4-тиахиназолина.
0,025 г-моль N-фенилтрихлорацетамидина, 10 мл двухлористой серы и 40 мл ССЦ кипятят в течение 6-10 ч до исчезновения осадка. Раствор фильтруют. Фильтрат упаривают в вакууме водоструйного насоса. В остатке 2трихлорметил-4,6-дихлор-4-тиахиназолин, который кристаллизуют при растирании с гексаном. Очистка кристаллизацией из гептана с добавкой нескольких капель двухлористой серы. Желтые призмы, т. пл. 137-138 С, выход 69%.
Найдено, %: С1 52,67; S 9,75.
СтНзСЬМгЗ.
Вычислено, %: CI 52,90; S 9,57.
Пример 4. Получение 2-трихлорметил-4,6дихлор-4-тиахиназолина
0,025 г-моль N-n-хлорфенилтрихлорацетамидина, 5 мл двухлористой серы и 40 мл ССЦ кипятят в течение 6-10 ч до исчезновения осадка. Раствор фильтруют, фильтрат упаривают в вакууме водоструйного, а затем масляного насоса при 20-30°С. В остатке 2-трихлорметил-4,6-дихлор-4-тиахипазолин, который кристаллизуют при растирании с гексаном. Очистка кристаллизацией из гептана с добавкой нескольких капель двухлористой серы. Желтые призмы, т. пл. 137-138°С, выход 71%.
Найдено, %: Cl 52,56; S 9,46.
СуНзСЬЫгЗ.
Вычислено, %: Cl 52,90; S 9,57.
Это же соединение получают при нагревании фениламидина трихлоруксусной кислоты с SCb.
Предмет изобретения
Способ получения 2-замещенных 4,6-дихлор4-тиахиназолинов формулы I
где R - алкил, арил, тиоалкил или диалкиламиногруппа, отличающийся тем, что N-ариламидины формулы II
R-C
где R имеет вышеуказанные значения; X - атом водорода или хлора,
подвергают взаимодействию с двухлористой серой при температуре кипения инертного растворителя, например четыреххлористого углерода, и выделяют целевой продукт известными методами.
Авторы
Даты
1974-09-15—Публикация
1972-05-19—Подача