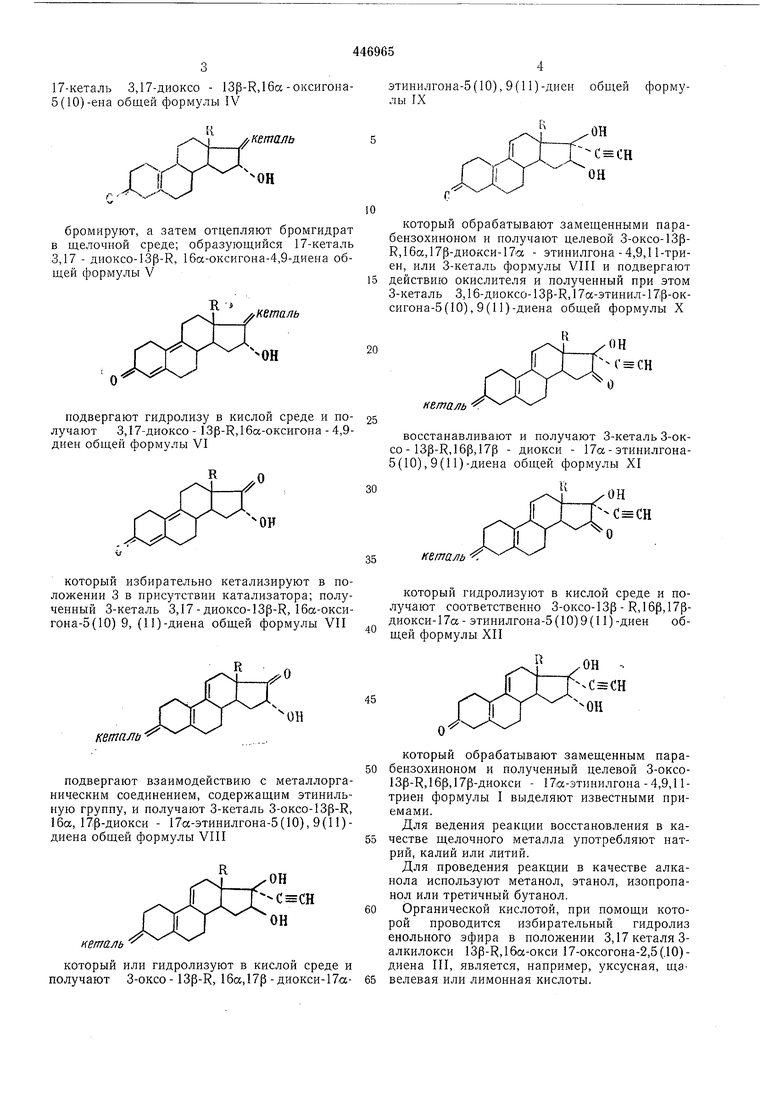
17-кеталь 3,17-диоксо - 13p-R,16a-oкcигoнa5(10)-eнa общей формулы IV
x-xj у/ кеталь
rrW-H
г ..
этинилгона-5(10), 9(11)-диен
общей формулы IX
бромируют, а затем отцепляют бромгидрат в щелочной среде; образующийся 17-кеталь 3,17 - диоксо-13р-К, 16а-оксигона-4,9-диена общей формулы V
Т1
кеталь
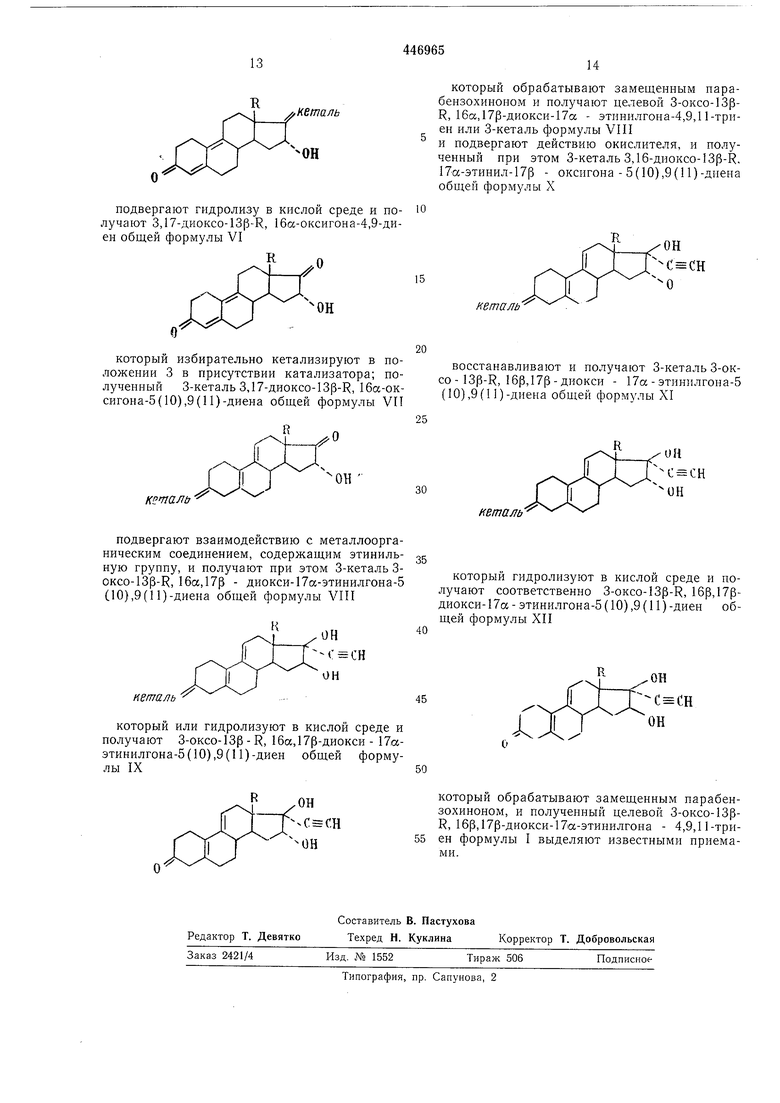
подвергают гидролизу в кислой среде и получают 3,17-диоксо- 13р-К,16а-оксигопа-4,9диен общей формулы VI
ОН
который избирательно кетализируют в положении 3 в присутствии катализатора; полученный 3-кеталь 3,17-диоксо-13р-К, 16а-оксигона-5(10) 9, (11)-диена общей формулы VII
который обрабатывают замещенными парабензохиноном и получают целевой 3-оксо-13рR,I6a,17|3-диoкcи-17a - этинилгона-4,9,11-триен, или 3-кеталь формулы VIII и подвергают
действию окислителя и полученный при этом 3-кеталь 3,16-диoкco-13|3-R,17a-этинил-17|3-oксигона-5(10), 9(11)-диена общей формулы X
R
он
rr-N-/.
кеталь г
восстанавливают и получают 3-кеталь 3-оксо - 13|3-R,16p,17p - диокси - 17а-этинилгона5(10), 9(11)-диеиа общей формулы XI
rr-si- И
1 1 Г
/Ои
ккталь
который гидролизуют в кислой среде и получают соответственно 3-оксо-13р - R,16p,17pдиокси-17а- этинилгона-5(10)9(11)-диен общей формулы XII
R
гг-М;-
rvV
кеталь
подвергают взаимодействию с металлорганическим соединением, содержащим этинильную группу, и получают 3-кеталь 3-OKCO-13p-R, 16а, 17|р-диокси - 17сс-этинилгона-5(10), 9(11)диена общей формулы VIII
кеталь
который или гидролизуют в кислой среде и получают 3-оксо- 13p-R, 16а,17р -диокси-17акоторый обрабатывают замещенным парабензохиноном и полученный целевой 3-оксо13р-Н,16р,17р-диокси - 17а-этииилгона-4,9,11триен формулы I выделяют известными приемами. Для ведения реакции восстановления в качестве щелочного металла употребляют натрий, калий или литий.
Для проведения реакции в качестве алканола используют метанол, этанол, изопропанол или третичный бутанол.
Органической кислотой, при помощи которой проводится избирательный гидролиз енольного эфира в положении 3,17кеталяЗалкилокси 13р-Н,16а-окси 17-оксогона-2,5(.10)диена III, является, например, уксусная, щавелевая или лимонная кислоты.
Для бромирования и отщепления бромгидрата из 17-кеталя 3,17-диоксо-13|3-К,16сс-оксигоиа-5(10)-ена формулы IV предпочтительио употреблять пербромид пиридина в присутстЕии пиридина.
Для гидролиза 17-кеталя 3,17-диоксо-13р-К, 16а-оксигона-4,9 диена V, применяют соляную, серную или паратолуолсульфокислоту.
Избирательную кетализацию в положении 3,3,17-диоксо- 13р-К,16а-оксигона-4,9-диена VI проводят алканолом, содержащим от 1 до 4 атомов углерода, например, метанолом, бутанолом и др., алкиленгликолем, имеющим от 2 до 4 атомов углерода, например, этиленгликолем или пропиленгликолем, диоксоланом, нанример 2-метил-2-этилдиоксоланом, 2-метил-2-феннл - диоксоланом, 2-метил-4-(4-метилбензил) -диоксоланом, 2,2-диметил-4- (4-метилбензил) -диоксоланом, 2-хлорметилдиоксоланом, 2)-хлорэтилдиоксоланом или 2-метил2-изопропилдиоксоланом.
Кетализацня проводится в присутствии кислого катализатора, например соляной, хлорной, серной, паратолуолсульфокислоты, ацетилхлорида пли трифторид,а бора.
В качестве органометаллического реактива, содержащего этинильную группу, используют магнийгалогенэтинил, причем галогеном может быть хлор, бром или йод, либо ацетиленид Н1елочного металла, в частности лития, натрия или калия.
В качестве окислителя соединения формулы VIII применяют окись хрома, двуокись марганца N-бромсукцинимид или N-бромацетамид.
Окисление можно также проводить с помощью реакции Онпенауера, т. е. употреблять в виде акцептора водорода кетон или альдегид, как то циклогексанон, бензохинон, хлоранил или анисовый альдегид, в присутствии катализатора, такого как фенолят алюминия или изопропилат алюминия, бутанолат алюминия или пентанолат алюминия.
Для восстановления 3-кеталя 3,16-диоксо13p-R, 17а-этинил- 17р-оксигона-5(10),9(11)диена формулы X употребляют преимущественно гидроборид щелочного металла или литийалюминийгидрид.
Это восстановление может быть также проведено по реакции Меервейна-Понндорфа, причем в качестве источника водорода применяют изопропиловый спирт, в присутствии изопропилата алюминия в качестве катализатора.
В качестве кислоты, употребляемой для гидролиза 3-кеталя формулы VIII или формулы XI используют уксусную, щавелевую, соляную, серную или паратолуолсульфокислоту.
В качестве замещенного парабензохинона, действию которого подвергают соединение IX или соединение XII применяют, например, 2,3-дихлоро-5,6-дицианопарабензохинон, 2,3дибромо-5,6-дицианопарабензохинон, 2,3,5,6тетрахлорпарабензохинон, 2,3-дициано-5-хло
ронарабензохинон или 2,3-дицианопарабензохинон.
Реакцию окисления парабензохиноном проводят в органическом растворителе, например 5 в хлористом метилене, дихлорэтане, бензоле, толуоле, диоксане, этилацетате, диметилформамиде или этиловом эфире.
Пример 1. 3-Оксо-13р-этил-16а,17р-диокси-17а-этинилгона-4,9,11 -триен.
10
A.3-метокси - 13р-этил-16а - окси - 17,17-этилендиоксигона-2,5(10)-диен 550 см жидкого аммиака охлаждают в инертной атмосфере до -70°С, доводят до -40°С и прибавляют смесь 14 г 3-метокси-13р-этил-16а-окси-17,1715 этилендиоксигона-1,3,5(10)-триена, 280 мл тетрагидрофурана и 210 мл третичного бутанола; прибавляют 23 г натрия нри -35°С и неремещивают в течение 45 мин при -40нн-50°С; выпаривают аммиак, доводят реак20ционную смесь до комнатной температуры, избыток натрия удаляют прибавлением 100 см этанола; выливают в смесь воды со льдом, экстрагируют этилацетатом, промывают водой органический слой, сущат над сер25нокислым натрием и перегоняют досуха в вакууме. Получают 15 г 3-метокси 13р-этил-1босокси-17,17 - этилендиоксигона - 2,5(10)-диена, который употребляется в данном виде в следующей стадии.
0
Для анализа нродукт перекристаллизовывают из этилацетата. Т. пл. 181°С, ИК спектр (в хлороформе) показывают присутствие С С связи при 1693 и 1664 , кеталя и ассоциированного комплекса ОН.
5
Б. 3-Оксо - 13Р-ЭТИЛ - 16а-окси-17,17-этилендиоксигона-5(10)-ен.
Перемещивают в течение 1 ч в атмосфере азота 32 г 3-метокси-13р - этил- 6a-oкcи-17,17этилeндиoкcигoнa-2,5(10)-диeнa н ПО мл ук0сусной кислоты, содержащей 25% воды. К раствору прибавляют 300 мл воды, отсасывают, осадок промывают водой и сушат в вакууме. Получают 30 г продукта хроматографией сырого продукта на двуокиси кремния и S элюированием смесью бензол-этилацетат (в соотнощении 6 : 4) получают 19,5 г 3-оксо-13рэтил-16а-окси - 17,17-этилендиоксигона15(10)ена в виде твердого, бесцветного продукта, растворимого в хлористом метилене, нераст0воримого в воде, плавящегося при 176°С.
ИК снектр (в хлороформе) показывает присутствие несопряженного кетона при кеталя и ассоциированного комплекса ОН.
5
B.3-Оксо-13р-этил - 16сс-окси - 17,17-этилeндиoкcигoнa-4,9-диeн.
В течение 1,5 ч перемещивают в атмосфере азота и при комнатной температуре смесь, состояц;ую из 19,5 г 3-оксо-13р-этил, 6а-гидро0кси-17,17-этилендиоксигона-5(10)-ена, 100 см- пиридина и 25 г пербромида пиридина. Суспензпю выливают в воду и доводят до рН 3 прибавлением 2 н. раствора соляной кислоты, экстрагируют хлорист1лм метиленом, промывают водой органический слой, сущат над сернокислым натрием и перегоняют в вакууме. При этом получают 18 г 13|3-этил-16а-окси-17,17-этилендиоксигона-4,9-диен-3-оксо, который употребляется в данном виде в следующей стадии. Хроматографией иа двуокиси кремния и элюированием смесью бензол-этилацетат (в соотношении 5 : 5) получают аморфное аналитически чистое соединение, плавящееся при 148°С. ИК спектр (в хлороформе) показывает присутствие кеталя, ОН и диеноиа. УФ спектр (в этаноле) Перегиб около 238 нм, Е{°С„ 143 Максимум при 304-305 нм, Е Гсм 546, т. е. 6 18800. Г. 3,17-диоксо- 13|3-этил-16а-оксигона-4,9-диен. Смесь 18 г 3-оксо-13р-этил-16а-окси-17,17этилендиоксигона-4,9-диена, 180 см ацетона и 45 см 2 и. раствора соляной кислоты нагревают с обратным холодильником в течение 1 ч. Раствор доводят до комнатной температуры, выливают его в воду, экстрагируют хлористым метиленом и перегоняют досуха в вакууме. Получают 15 г сырого продукта, к которому прибавляют 7,2 г того же продукта, полученного другим методом. 22,2 г хроматографируют на двуокиси кремния и элюируют смесью бензол-этилацетат (в отнощепии 5:5). Получают II г 3,17-Диоксо-13р-этил16а-рксигона-4,9-диена, который употребляют в данном виде в следующей стадии. Для анализа продукт перекристаллизовывают из этилацетата. Получают бесцветный, твердый продукт, плавящийся при 166°С, растворимый в хлороформе и этаноле, нерастворимый в воде, имеющий а 130° ± 2 (с 0,9%, СНС1з), мол. вес 300,40. Найдено, %: С 75,7; Н 8,1. С19Н24ОзВычислено, %: С 75,97; Н 8,05. ИК сиектр (в хлороформе) показывает присутствие ассоциированной ОН группы при 3543 , 17-кетогруппы при 1744 см и диенона. УФ спектр (в этаноле) Максимум ири 213 пм, Е}7м 197 Перегиб у 229 им, НГЛ, 162 Перегиб у 236 нм, ЕГсм 154 Максимум при 302 нм, E/CM 689, т. е. е 20 700. Д. 3,3 - Диметокси - 13р-этил-16а - окси-17оксогоиа-5(10) ,9 (11) -диен. В течение 15 мин иеремещивают в атмосфере азота и при комнатной температуре смесь, состоящую из 10,5 г 3,17-диоксо-13рэтил-16а-оксигона-4,9-диена, 100 см 2,2-диметоксипропана и 10 см метанола, содержащего 1% ацетилхлорида. Раствор нейтрализуют прибавлением триэтиламииа и перегоняют досуха в вакууме. Остаток хроматографируют на двуокиси кремния и элюируют месью бензол-этилацетат (в отиощеиии :3). Получают 9,5 г 3,3-диметокси-13|3-этил6а-окси - 17-оксогона-5(10),9(11) -диена, коорый употребляют в даииом виде в следуюей стадии. Соединение представляет собой аморфный родукт, растворимый в этаноле и хлорофоре, нерастворимый в воде, плавящийся при 0°С. ИК спектр (в хлороформе) показывает рисутствие циклоиеитаиоиа С О-группы ири 1742 cм ОН группы ири 3531 и С-О-С-связь. УФ спектр (в этаноле) Максимум при 237 нм, 415 Максимум при 242 им, Е i см 430, т. е. е 14900 Перегиб около 250 им, 290 Максимум ири 293 нм, , 32 Е. 3,3-Диметокси - 13р-этил-16а,17р-диокси17«-этинилгопа-5(10),9(11)-диен 80 г магния вводят в 1 800 мл эфира и в течение 5 ч барботируют метилбромид в инертной атмосфере, перегоняют эфир, прибавляя тетрагидрофураи до постоянного объема. Получают 0,8 М раствор магнийбромметила в тетрагидрофуране. Ацетилен барботируют в течение 30 мин в 600 мл тетрагидрофурана в инертной атмосфере, а затем прибавляют 500 мл 0,8 М раствора магиийбромметила и иеремещивают в течение 30 мин, иоддерживиая барботироваиие ацетилена в ииертиой атмосфере при комнатной температуре. К 5 г 3,3-диметокси-13р-этил-16а-окси-17-оксогоиа-5(10),9(11)-диеиа в 120 см тетрагидрофураиа ири барботировании ацетилена в инертной атмосфере прибавляют 250 см выщеуказанного раствора магиийбромэтииила при 25°С и перемащивают в течение 40 мни ири барботаже ацетилена и в инертной атмосфере. Избыток магиийоргаиического соединения разрущают прибавлением 100 см иасыщенного водного раствора хлористого аммоиия, экстрагируют этилацетатом, экстракт досуха уиаривают в вакууме, получают 5,6 г. Остаток хроматографируют на двуокиси кремния и элюируют смесью беизолэтилацетат (в отиощении 5:5). Получают таким образом 2,74 г 3,3-диметокси - 13р-этил-16а,17|3-диокси17р - этинилгона - 5(10),9(11)-диена, в виде аморфного продукта, растворимого в хлороформе и нерастворимого в воде. ИК спектр (в хлороформе) показывает присутствие ОН при 3592 и 3563 CM-I, С СН при 3 297 см-1 и С -О-С. Ж. 3-Оксо-13р-этил-16а,17(3-диокси - 17сбэтинилгона-5 (10) ,9 (11) -диен. Смесь 2,42 г 3,3-диметокси-13р-этил-16а,17рдигидрокси-17а -этинилгопа-5 (10) ,9 (11) -диеиа, 30 см уксусной кислоты и 6 см воды иеремещивают в течение 1 ч при комнатной темиературе в атмосфере азота, выливают раствор в воду, экстрагируют хлористым метиленом и
упаривают экстракт досуха в вакууме. При этом получают 1,90 г 3-оксо-13р-этил-16а,17рдиокси-17а - этинилгона-5(10),9(11)-диена в виде твердого продукта, растворимого в бензоле и хлороформе, нерастворимого в воде, плавящегося при ISOC.
3. 3-0ксо-13р - этил - 16а, 17р - диокси - 17аэтинилгона-4,9,11-триен.
Растворяют 1,90 г 3-оксо-13р-этил-16а, 17рдиокси-17а - этинилгона-5(10),9(11)-диена в 85 см диоксана, прибавляют 2,75 г 2,3-хлоро5,6-дицианобензохииона и перемешивают в течение 7 ч в атмосфере азота при комнатной температуре. После отсасывания промывают фильтр бензолом. Разбавленный двумя объемами бензола фильтрат промывают водным раствором тиосульфата натрия до обесцвечивания, а затем водой. После высушивания над сернокислым натрием и выпаривания досуха в вакууме остаток растворяют хлористым метиленом, кристаллы отсасывают, промывают хлористым метиленом и сушат. Вес остатка 1,34 г. После перекристаллизации из этнлацетата с обратным холодильииком получают 0,580 г 3-оксо-13р-этил-1 бос, 17р - диоксй-17аэтинилгона-4,9,11 -триена в виде твердого продукта, плавящегося при 180°С, растворимого в хлороформе и этаноле, нерастворимого в воде, «2° -L 137,5 ± 3,5° (с 0,5%, хлороформ).
Упариваем досуха различных маточных растворов, хроматографией остатка на двуокиси кремния и элюированием смесью бензол-этилацетат (в отношении 4:6), рекуперируют вторую порцию в 0,61 г продукта, мол. вес 324,41.
Найдено, %: С 76,9; П 7,4. Cs.HavOs.
Вычислено, %: С 77,26; Н 7,48. ИК спектр (в хлороформе) показывает присутствие С СН при 3 29cS см-, ОН и триенона.
УФ спектр (в этаноле) Максимум при 237 нм, ЕГсм 181 Максимум при 269-270 нм, ЕГ,,, 109 Максимум при 342 им, ВГсм 905, т. е. .- - 29350
Пример 11. 3-0ксо-13р-этил-16р,17р-диокси-17а-этинилгона-4,9,11 -триен.
А. 3,3-Этилендиокси-13р-этил-16а - окси-17оксогона-5(10),9{11)-диеи.
Нагревают нри 60°С 2 г 3,3-диметокси-13рэтил-16а-окси - 17-оксогона-5(10),9(11)-диена, полученного в примере 1Д, с 8 см гликоля, прибавляют 100 мг хлоргидрата пиридина и перемешивают в течение 10 мнн при 60°С. Доводят реакционную смесь до комнатной температуры и прибавляют раствор 0,3 см триэтиламина в 200 см воды, после чего экстрагируют этилацетатом, промывают водой органнческий слой, сушат над сернокислым натрием, отсасывают, иромывают фильтр хлористым метиленом и упаривают фильтрат досуха в вакууме. При этом получают 1,13 г
3,3-этилеидиокси - 13р-этил-16а-окси-17-оксогона-5(10),9(11)-диена в виде светло-желтого аморфного продукта, растворимого в хлороформе и хлористом метилене, нерастворимого в воде.
Б. 3,3-Этилендиокси-13р - этил-16а,17р-диокси- 17а-этинилгона-5 (10) ,9 (11) -диен.
1,8 г 3,3-Этилендиокси- Зр-этил-1ба-оксигоиа - 5(10) ,9(11)-диен - 17 - она растворяют в 70 см тетрагидрофурана, прибавляют в течение 30 мин нри барботировании ацетилеиа 140 см раствора магнийбромэтинила (полученного из раствора 0,3 н. метилмагния, в котором барботирован ацетилен) и перемешнвают в течение 1 ч при комнатной температуре при барботаже ацетилена. Затем прибавляют насыщенный водный раствор хлорнстого аммония, экстрагируют этилацетатом, нромывают водой органический слой, сушат пад сернокислым патрнем и упаривают досуха. Остаток хроматографнруют на двуокиси кремиия, элюируют смесью бензол-этнлацетат (в отношении 4 : 6) и получают 1,2 г 3,3 - этилендиокси-13р-этил-16а,17р - днокси 7а - этинилгона-5(10) ,9(11) - днена в виде аморфного желтого продукта, растворимого в хлороформе, нерастворимого в воде.
ИК спектр (в хлороформе) показывает присутствие , С-О-С, ОН и отсутствие кетона.
В. 3,3-Этиленднокси-13р-этил - 16-оксо-17аэтннил-17р-оксигона-5(10),9(1 )-диен.
1,1 г 3,3-Этилендиокси-13р-этил-16а,17р-диокси-17сх-этинилгона-5 (10) ,9 (11) -диена растворяют в 20 см ацетона, охлаждают раствор до 0°С и прибавляют 1,6 см раствора Герброн-Жонес следующего состава: Хромовый ангидрид, г270
Концентрированная серная кислота,
Вода, л1
Реакционную смесь пере сшивают в течение 1 ч при 0°С, затем прибавляют 0,5 см метанола, экстрагируют хлористым метнленом, нромывают водой органический слой, экстрагируют водный слой х.юристым метиленом и экстракты упаривают в вакууме. Остаток хроматографируют на двуокиси кремния и элюируют смесью бензол- тилацетат (в отношении 4:6). Получают 500 мг 3,3-этилендиокси-13р-этил - 16-оксо-17а-этинил - 17р-оксигона-5( 10) ,9(11)-диена в виде твердого, бесцветного продукта, растворимого в хлороформе, малорастворимого в эфире, нерастворимого в воде, плавящегося при 142°С.
ИК снектр (в хлороформе) показывает присутствие при 3305 см- кетона при 1 759 см-1, ОН и кеталя.
Г. 3,3-Этилендиокси - 13р - этил-16р,17р-диокси-17а-этииилгона-5(10),9(11)-диен.
500 мг 3,3-Этилендиокси - 13р-этнл - 16-оксо17а-этинил-17 - оксигона - 5(10) ,9(11)-диена
смешнвают с 8 см метанола, охлаждают дс
0°С, прибавляют 100 мг боргидрида натрия
и перемешивают суспензию в течение 2 ч прь 0°С, затем доводят до 20°С, прибавляют 60 мл боргидрида натрия, перемешивают в течепие 1 ч при 20°С, а затем выливают реакционную смесь в воду и экстрагируют этилацетатом. Органический слой промывают водой, сушат над серпокислым натрием и упаривают в вакууме досуха. Вес остатка 0,355 г. Остаток хроматографируют на двуокиси кремния, элюируют смесью бензол-этилацетат (в отношении 4:6), получают 210 мг 3,3-этилендиоксп-13р-этил - 16|3,17|3 - диокси-17а-этинилгопа-5(10),9(11)-диена в виде бесцветного твердого продукта, плавящегося при 190°С, растворимого в хлороформе и метаноле, нерастворимого в воде. ИК спектр (в хлороформе) показывает присутствие ОН группы при 3588 см С Ссвязи и указывает на отсутствие кетона. Д. 3-Оксо-13|3-этил - 16р,17р-диоксн-17а-этипилгона-5(10),9(11)-диен. 200 мл 3,3-Этилепдиокси-13р-этил-16р,17рдиокси - Па - этипплгопа - 5(10),9(11) -диена растворяют в 6 см 95%-ой уксусной кислоты и перемешивают в течение 30 мин при комнатной температуре. Затем прибавляют 1 см воды и выдерживают реакционную смесь в течепие 12-15 ч при комнатной температуре, после чего выливают раствор в воду, экстрагируют хлористым метиленом, промывают органический слой водой, сушат над серпокислым натрием и упаривают досуха в вакууме. Получают 170 мг 3-оксо-13р-этил-16р,17р-диокси-17а-этинилгона-5 (10) ,9 (11) -диена, который употребляют в данном виде в следующей фазе. Е. 3-Оксо-13(5-этил - 16(3,17р-диокси-17а-этипилгона-4,9,11 -триеп. 170 мг 3-Оксо-13р-этил-16р-17р-диокси-этинилгона-5(10),9(11)-диена и 0,250 г 2,3-дихлор-5,6-дициапобензохипона растворяют в 7,6 см дпоксапа п перемешивают при 20°С в атмосфере азота. Реакционную смесь выдерживают в течение 12-15 ч при комнатной температуре, разбавляют бензолом, промывают бензольный слой насыщенным водным раствором тиосульфата натрия до полного обесцвечивания промывпых вод. Эти воды экстрагируют бензолом. Объединенные бензольные порции сушат над сернокислым натрием, фильтруют и упаривают досуха. Остаток хроматографируют па двуокиси кремния и элюируют смесью бензол-этилацетат (в отнощении 5:5). Получают 100 мг 3-OKCo-13ipэтил-16р,17р - диокси-17а - этинилгона-4,9,11триена в виде светло-желтого аморфного продукта, растворимого в хлороформе и бепзоле, нерастворимого в воде, имеющего « +35,5 + 2° (с 0,55%, этанол). ИК спектр (в хлороформе) показывает присутствие и ОН. УФ спектр (в этаноле) Максимум при 237 нм, Е Максимум при 265 нм, Е Перегиб у 282 нм, ЕГсм 122 Максимум при 343 нм, Е|°С„ 758, т. е. 24 600 Предмет изобретепия Способ получения триеновых стероидных оединений общей формулы I где R (в формулах I-ХН) - радикал алил, содержащий I-3 атома углерода, гидросильная группа в положении 16 иаходится ибо в положении а, либо в положении р по тношению к стероидному ядру, отличаюийся тем, что 17-кеталь 3-алкилокси-13р, 16а-окси - 17-оксогона-1,3,5 (10)-триена обей формулы II а л кил -О подвергают восстановлению щелочным меаллом в жидком аммиаке в присутствии алаиола; образующийся епольный эфир 17-кеаля 3-алкилокси - 13p-R, 16а-окси - 17-оксогона-2,5(10)-диена общей формулы III . кеталь r- N-/ избирательно гидролизуют с помощью органической кислоты; полученный при этом 17-кеталь 3,17-диоксо-13р-R,I6a - оксигона-5 (10)-ена общей формулы IV кеталь бромируют, а затем отщепляют бромгидрат в щелочной среде и образующийся 17-кетал1) 3,17-диоксо-13р-Н, 16а - оксигона-4,9-диен общей формулы V






Авторы
Даты
1974-10-15—Публикация
1972-08-23—Подача