(54) СПОСОБ ПОЛУЧЕНИЯ ДИУРЕТАНОВ ХИНАЗОЛОНА
(III) применяется не как растворитель, то на
1моль соединения формулы (II) преимущественно вводят I-10 моль, лучше 2,2-6 моль, соединения формулы (III).
Если гидроксильное соединение является одновременно растворителем, то рекомендуется добавлять небольшое количество (0,1-5% от веса исходной смеси) основного катализатора, например триэтиламин, пиридин, триэтилендиамин или дйметилциклогексиламин.
Пример 1. (метоксикарбониламино)-фенил -3 - фенил-6 - метоксикарбониламино-4- (ЗН) -хиназолон.
Смесь из 38 вес. ч. 2-(3-изоцианатофенил)3-фенил - 6-изоцианато - 4-(ЗН) -хиназолона,
2об. ч. триэтиламина и 200 об. ч. метанола нагревают 30 мин до кипения. Затем реакционную массу смешивают с водой и выделившийся продукт перекристаллизовьгвают из этанола. Выход 36 вес. ч. (81% теории); т. пл. 243-245°С.
Найдено, %: С 64,7; Н 4,7; О 18,2; N 12,8.
Вычислено, %: С 64,86; Н 4,54; О 18,0; N 12,61.
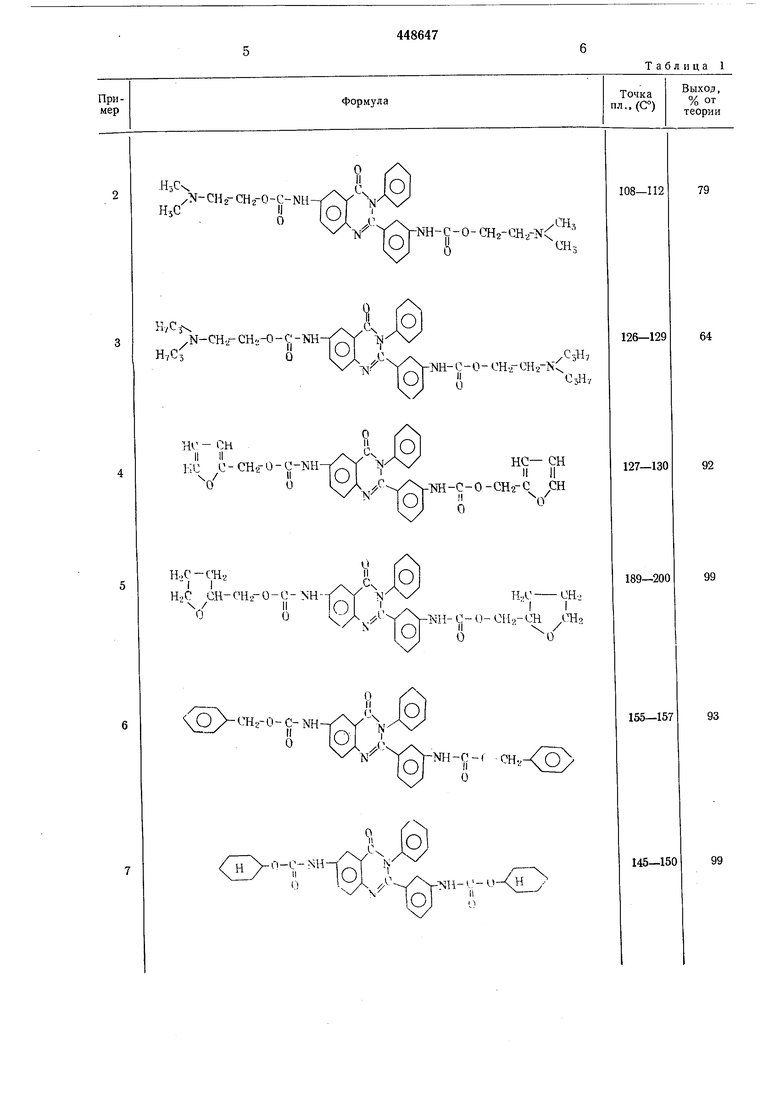
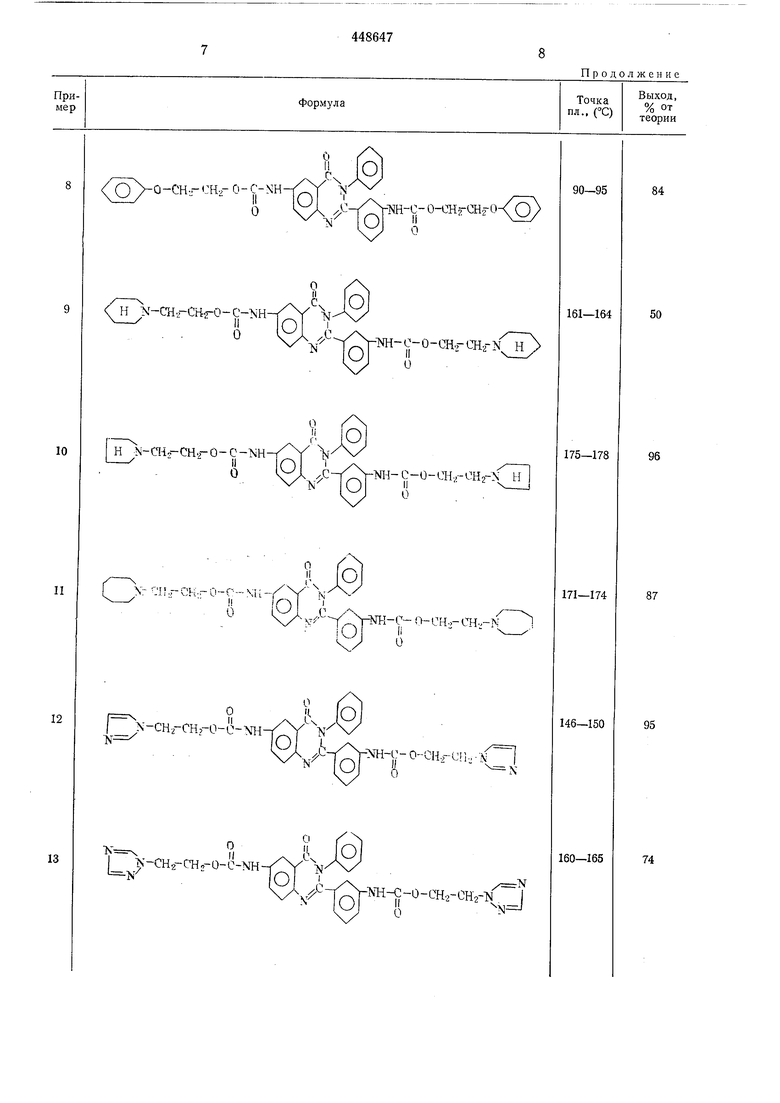
Пример 2-13. Аналогично примеру 1, из соответствуюшего диизоцианата и спирта получают диуретаны хиназолона, представленные в табл. 1.
Пример 14. (р,7-диоксипропилоксикарбониламино)-фенил -3 - фенил-6-(р,7ДИоксипропилоксикарбониламино)-4-(ЗН) - хиназолон.
13 вес. ч. 2-(З-изоцианатофенил)-З-фенил-6изоцианато-4- (ЗН) -хиназолона растворяют в 60 об. ч. диметилформамида. Затем прибавляют 60 вес. ч. глицерина, растворенных в 60 об. ч. безводного диметилформамида, и 5 об. ч. триэтиламина. Потом дополнительно
перемешивают 1 час при комнатной температуре и 4 час при 60°С, смесь выливают в воду, осадок отсасывают и высушивают. Выход 15 вес. ч. (67% теории); т. пл. 172-174°С. Найдено, %: С 59,1; Н 5,1; О 24,9; N 10,0.
Вычислено, %: С 59,6; Н 4,96; О 25,55; N 9,95.
По данным ЯМР-спектроскопии полученный
продукт содержит лишь небольшие количества изомерного (бисоксиметилметоксикарбониламино)-фенил - З-фенил-6 - (бисметилметоксикарбониламино) -4- (ЗН) -хиназолона.
Пример 15. (метокситиокарбониламино) -фенил -3 - фенил-6 - метокситиокарбониламино-4-(ЗН)-хиназолон.
5 вес. ч. металлического натрия растворяют в 150 об. ч. абсолютного метанола. Затем прибавляют 34 вес. ч. 2-(3-изотиоцианатофенил)2-фенил-6-изотиоцианато-4- (ЗН) -хиназолона и дополнительно перемешивают 1,5 час при комнатной температуре ( 20С) и 1 час при 40°С. Раствор отсасывают и удаляют небольшое количество нерастворившегося осадка. К фильтрату добавляют воду и подкисляют его соляной кислотой. Осадок отсасывают и высушивают при 50°С в вакууме.
Выход целевого продукта 30,5 вес. ч. (78% теории); т. пл. 155-158°С.
Найдено, %: С 60,1; Н 4,5; О 10,4; N 12,0; S 13,0.
Вычислено, %: С 60,5; Н 4,2; О 10,1; N 11,75; S 13,4.
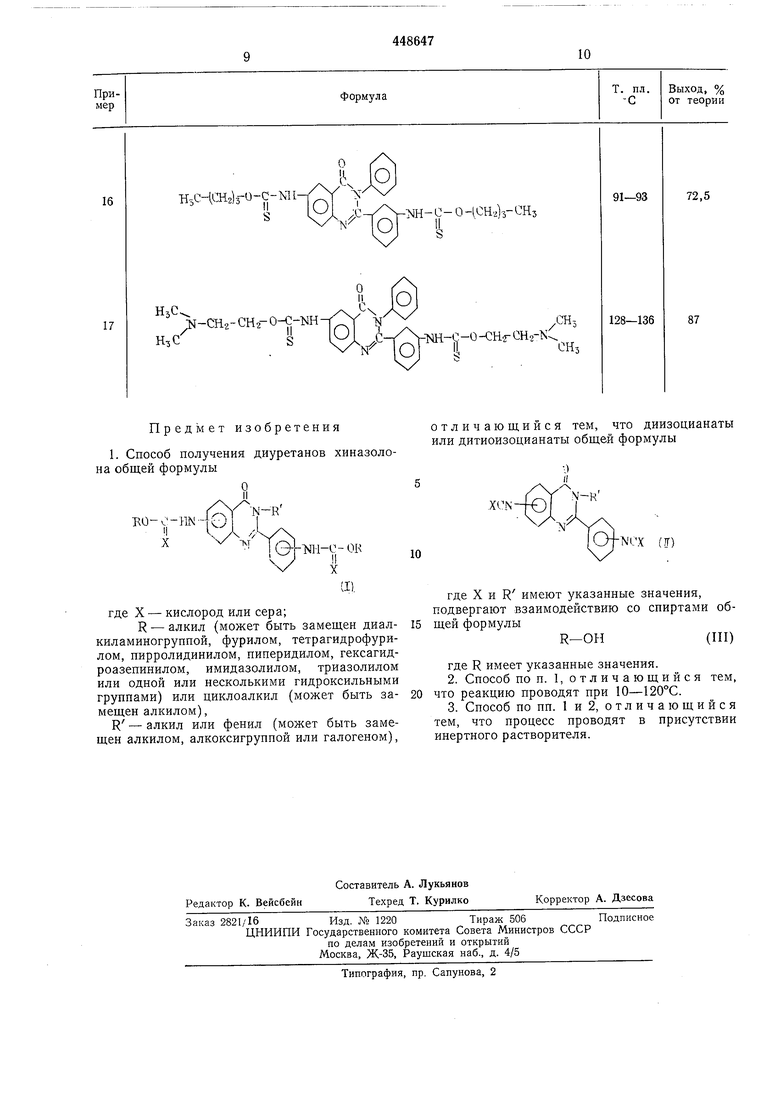
Пример 16-17. Аналогично примеру 15
из 2- (З-изотиоц анато) -З-фенил-6-изотиоцианато-4-(ЗН)-хиназолона и соответствующих
алкоголятов натрия получают указанные в
табл.2 дитиоуренаты хиназолона.
Таблица 1

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИУРЕТАНОВ ХИНАЗОЛОНА | 1973 |
|
SU406356A1 |
| Способ получения производных аминокислоты | 1985 |
|
SU1468411A3 |
| Способ получения 6-(ациламиноарил)-4,5-дигидро-3(2Н)-пиридазинопроизводных или их фармацевтически приемлемых солей | 1984 |
|
SU1648250A3 |
| Способ получения пенициллинов или их солей | 1972 |
|
SU527139A3 |
| Способ получения производных 1-алкилзамещенных бензимидазолов | 1988 |
|
SU1637663A3 |
| Инсектицидное средство | 1977 |
|
SU841570A3 |
| Способ получения простых пиридиниламино-АлКилОВыХ эфиРОВ или иХ физиОлОгичЕСКипРиЕМлЕМыХ СОлЕй | 1978 |
|
SU850002A3 |
| Способ получения гетероциклических кислот или их солей | 1985 |
|
SU1545940A3 |
| Способ получения растворимых ароматических полиамидов | 1972 |
|
SU471729A3 |
| Способ получения производных аминокислот или их физиологически совместимых солей | 1987 |
|
SU1836335A3 |

i lOl
CH.-CH -O-C-NH- V
II п
о 1 /
х/ -(/ /4/
CH.-CH.-O-C-MiY Y
-W
ч{ )
о {U е
N/ М НО - СИ IX о-сн.го-е-№1 , о Рл /
шс-ш. 1 I
НгС CH-CHf-O( Шг и-С ШIII f-. О.
79
108-112
01,
,-NH-C-0-CH2-OH,-N UI Шз
,
С. |0,
126-129
64
./С-.Нт
МН- с - о - OHvr он 2-N ОзНу О .Т -С-099
189-200
н.,с-ш.. I I
с - о- ОИ,- СН Шо
д ./
о
0 -NH-C-( ОНКО НС- СН 127-130 СН2-С JCH 155-157
0-0-NH II
о
99
145-15(
v -NH--- - 45O
и
,С
/.
СН-г-Ш.-0-C-NHоII О
j
f-CH-CH.rO-C- H-t V
..с
о
Продолжение
90-95
84
-Ш-С-О-СНгСНг-оХ О,
1Q
50
161-164
- Ш-с-о - Ш.-Шг
,сн.о-с-ш-.
Н N-CH10о 1Ул /,с
175-178
96
х
, NH-C-0-CH./-OH2-N Ы
О
о
о II
|
.r-CH.O-r-NU-/V ГЛ -1
О ..v-Ч/ кг уШ-С-0-СНо-CH,-N
Ю N-CHrCHrO-C-NliY Y N Nо L ТсГЧ К- I -сн2-снс-о-е- чТ{ W L.j-/ ,/ ш-с о171-174
87
/ О
146-150
95
160-165
74 щ,
Пример
Н5С-1Ш2)гО-С-М1-| Y S
-N YoY r С-Ш -СНг-СНг-0-С-Ш
Предмет изобретения
О
Ч/
БО-0-Ш-4О
X .„,.ок
V I
где X - кислород или сера;
R - алкил (может быть замещен диалкиламиногруппой, фурилом, тетрагидрофурилом, пирролидинилом, пиперидилом, гексагидроазепинилом, имидазолилом, триазолилом или одной или несколькими гидроксильными группами) или циклоалкил (может быть замещен алкилом),
R - алкил или фенил (может быть замещен алкилом, алкоксигруппой или галогеном),
Выход, %
Т. пл.
Формула
- / от теории
72,5
91-93
ib
128-136
87
отличающийся тем, что диизоцианаты или дитиоизоцианаты общей формулы
.XCN
NCX (Ц)
10
где X и R имеют указанные значения, подвергают взаимодействию со спиртами общей формулы
R-ОН(III)
где R имеет указанные значения.

Авторы
Даты
1974-10-30—Публикация
1971-10-11—Подача