(54) СПОСОБ ПОЛУЧЕНИЯ ТИОЛФОСФОНАТОВ




| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛЕН(АРИЛЕН)-БИСОРГАНОТИОЛФОСФОНАТОВ | 1971 |
|
SU432157A1 |
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНОТИОЛФОСФОНАТОВ | 1973 |
|
SU406839A1 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕШАННЫХ ДИОРГАНОДИТИОЛФОСФОНАТОВ | 1973 |
|
SU390099A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИОРГАНОДИТИОЛАМИДОФОСФАТОВ | 1972 |
|
SU341802A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛИЧЕСКИХ АЛКИЛЕНГЛИКОЛЬ-5-ОРГАНОТИОФОСФАТОВ | 1973 |
|
SU389101A1 |
| СПОСОБ ПОЛУЧЕНИЯ ?ЯС-(ОРГАНОТИОЛ)-ПЕНТАЭРИТРИТФОСФАТОВ | 1973 |
|
SU374324A1 |
| СПОСОБ ПОЛУЧЕНИЯ О-АЛКИЛ-8-ОРГАНОХЛОРТИОФОСФАТОВ | 1973 |
|
SU395372A1 |
| СПОСОБ ПОЛУЧЕНИЯ О-АРИЛДИОРГАНОДИТИОЛФОСФАТОВ | 1973 |
|
SU406838A1 |
| Способ получения хлорангидридов тиоловых эфиров кислот пятивалентного фосфора | 1972 |
|
SU446510A1 |
| СПОСОБ ПОЛУЧЕНИЯ S-ОРГАНОАМИДОТИОФОСФОНАТОВ | 1973 |
|
SU395373A1 |

I Изобретение относится к фосфороргани, ческой химии, а именно к способу получения новых тиолфосфонатов общей формулы - замещенный или незамещенный фенил или бензил; R - незамещенный или замещенный фенил, аралкил, циклоалкил, алкенил, алкинил, этилтиоэтил, алкоксиэтил, арилоксиэтил или группа -( С(СН); R - алкил или арил. Известен способ получения тиолфосфона-J тов взаимодействием дихлорфосфинов с i сульфенилхлоридами, разложением аддукта f сернистым газом и обработкой образующегося эфирхлорангидрида спиртами.J Однако соединения указанной формулы i являются новыми. Они обладают физиоло- , гической активностью и могут найти применение в сельском хозяйстве. Предлагаемый способ заключается в том, что соответствующий дихлорфосфин подвергают взаимодействию с сульфенилхлоридом в присутствии уксусной кислоты с последующей обработкой образующегося эфирхлорангидрида фенолом, спиртом или ацетоксимом в присутствии третичного амина, Предлагаексый способ проводят смещением примерно эквимолярных количеств реагентов в инертном органическом раст ворителе при минус 5О - плюс 8О°С. Целевые продукты вьвделяют известными приемами. Они представляют собой вязкие жидкости, растворимые в органических растворителях и нерастворимые в воде. В качестве исходного сульфенилхлори- j да во многих случаях целесообразно использовать продукт взаимодействия соответствующего тиола или дисульфида с эквимолярным количеством хлора или хлористого сульфурила.
Пример 1. Получение - 0-4-хлорфенил- S -метилбензилтиофосфоната.
К раствору 0,52 г «моль диметилдисульфида в 30 мл сухого хлороформа при минус 40-5 0°С добавляют эквимолярное количество хлора или хлористого сульфурила. Температуру смеси доводят до комнатной и получают раствор А. ; К смеси 0,1 г моль бензилдихлорфос- фина и 0,1 г. моль ледяной уксусной кис- лоты в ЗО мл хлороформа при минус 4О-ЗО С приливают раствор А. Температуру смеси доводят до комнатной, раство- .ритель и летучие удаляют в вакууме, в , остатке получают промежуточный -метилбензилхлортиофосфонат. К смеси 0,25 г моль промежуточного эфирхлорангидри
да и 0,25 г . моль 4-хлорфенола в ЗО мл .бензола при, Ю-15°С прибавляют О,О25 i г-моль триэтйла мина и киГЁптяТ 2 час. FSакционную массу промывают водой, сушат азеотропно, растворитель удаляют в вакууме и продукт вьщеляют перегонкой, т. кип. 23О-232°С/2 мм рт. ст., вещество при стоянии кристаллизуется, т. пл. 53-54 С, выход 72%,
Найдено, %: С1 11,10; Р 9,65; 810,40.
Вычислено, %: С1 11,35; Р 9,94; 810,22.
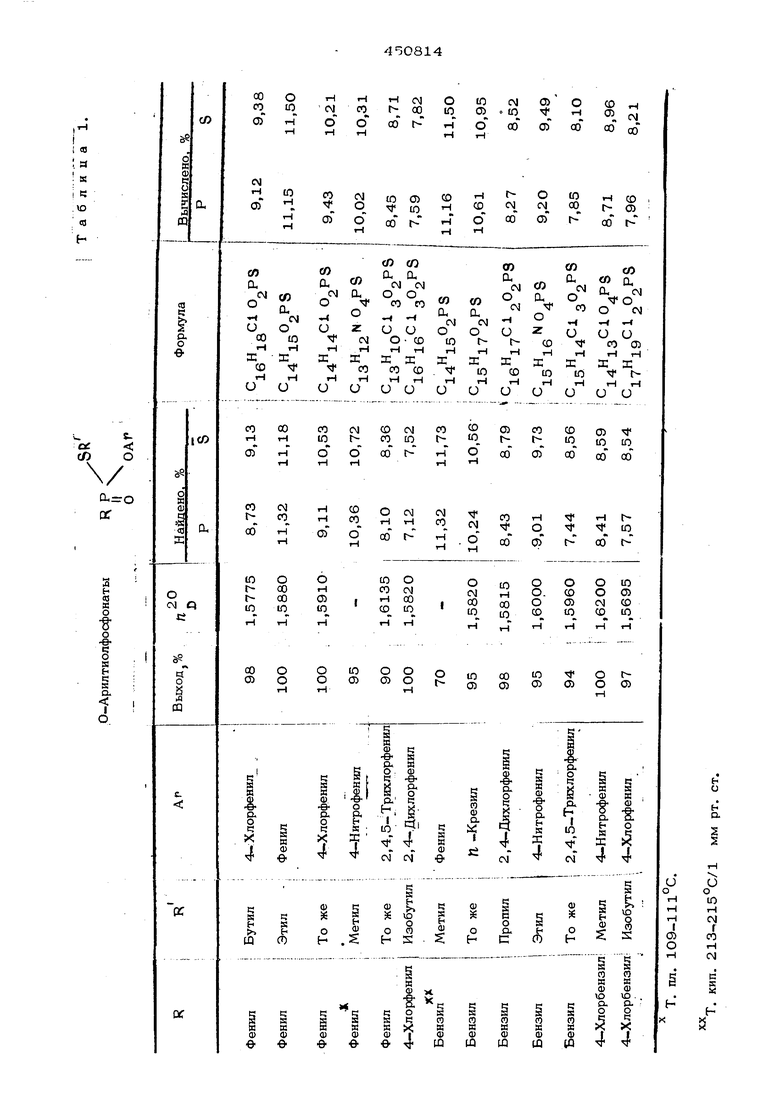
В условиях прим||ра 1 получают другие тиолфосфонаты, выход и некоторые свойства которых приведены в таблице 1.
i 0
. Я
e: ,ю « Ь
s.
CO
/
S л §
§ s ь
s
о
и
о ю
гЧ CvJ
со н CN
П р и м е р 2. Получение О- П -крезил- S -2,5-дихлорфенил-2,4-диметилбензилтиофосфоната.
К смеси 0,03 г. моль 2,4-диметилбензил дихлорфосфина и 0,03 г . моль уксусно кислоты в ЗО мл хлороформа при О - минус 5 С прибавляют раствор 0,03 г г мол 2,5-дихлорфенилсульфенилхлорида в 2О мл хлороформа. Температуру смеси доводят до комнатной, растворитель и летучие удаляют в вакууме, в остатке получают промежуточный S -2,5-.дихлорфенил-2,4-диметилбензилхлортиофосфонат.
В смесь 0,15 г. моль промежуточного эфирхлорангидрида и 0,015 г.моль fl -крезола в 30 мл бензола при 5-10°С вводят 0,015 г моль триэтиламина. Смес кипятят 2 час, промьтают водой, органи- ;ческий слой сушат азеотропно, раствори- 1тель удаляют в вакууме при 1ОО°С/1015 мм рт. ст., в остатке получают целевой продукт, fl 1,5 82 О; выход 98%.D
Найдено, %: С1 15,41; Р 6,54;
37,62.
S2 2lC4VS
Вычислено, %: С 15,75; Р 6,87;
87,10..
П р и м е р 3. Получение S -бутил-О- (4-хлорфенокси)этилбензилтиофосфона- та.
К раствору 0,О26 г.моль дибутилдисульфида в 20 мл сухого хлороформа при минус 4О-5О С прибавляют эквимолярное количество хлора или хлористого сульфурила. Температуру смеси доводят до комнатной и получают раствор А. В раствор 0,05 г . моль,:бензилдихлорфосфина и 0,05 г. моль ледяной уксусной кислоты в ЗО мл хлороформа при минус 30-4О С вводят раствор А. Температуру смеси доводят до комнатной, растворитель и летучие удаляют в вакууме при 1ОО С/Ю-15 мм рт. ст. Остаток растворяют в 30 мп бензола и к полученному раствору при 0-5 С приливают раствор 0,05 г моль j3 (4-хлорфенокси)этанола и 0,05 г . моль
|хгриэтиламина в 30 мл бензола. Смесь | нагревают в течение 3 час при 50-бО-С, промывают водой, органический раствор сушат азеотропно, растворитель удаляют в вакууме и в остатке получают пелевой
продукт, п 1,5660;j20
4
1,2233; MRjj найдено 106,0; вычислено 106,9, выход 98%.
Найдено, %: С1 8,48; Р 7,51;. . 88,36.
SPS Вычислено %: С1 8,91; Р 7,76; S 8,03.
I Пример 4. Получение О-( S 1 -этилбензилтиофосфонил)ацетоксина.
В условиях примера 1 из 0,О52 г. моль этилмеркаптана и эквимолярного количества хлора или хлористого сульфурила получают раствор А.
К смеси 0,05 г- моль бензилдихлорфосфина и 0,О5 г. моль ледяной уксусной кислоты при минус ЗО-4О°С прибавляют раствор А. Температуру реакционной мае- сы доводят до комнатной, растворитель и летучие удаляют в вакууме и остаток растворяют в 30 мл бензола. К полученному раствору при 5-10 С приливают раствор 0,05 г моль ацетоксима и 0,О5 г моль триэтиламина в 30 мл бензола. Смесь нагревают 2 час при 50 С, охлаждают, промьшают водой, сушат азеотропно, растворитель удаляют в вакууме и в остатке получают целевой продукт,
1,555; d 1,1676; MR
найдено 74,6; вычислено 74,9; выход 96%.
Найдено, %: N 5,36; Р 11,14; 811,59.
N 2
Вычислено, %:М5,17; Р 11.43; 311,81.
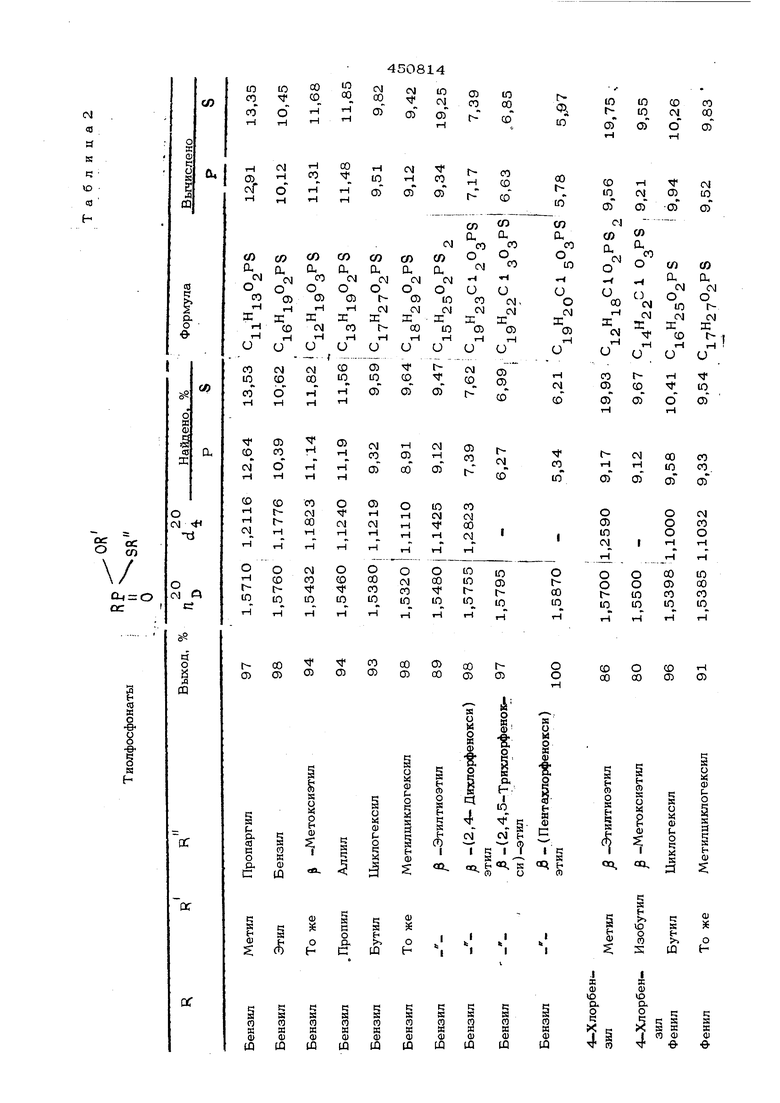
В условиях примеров 3 и 4 получают другие вещества, выход и некоторые свойства которых приведены в табл. 2.
см
о
я
S
п ю еа
н Пример 5. Получение 3-2,5-дихлорфенил-О-пропаргил-2,4-диметилбензилтиофосфоната. К смеси 0,ОЗ г . моль 2,4-диметш1бенi зилдихлорфосфина и. 0,ОЗ г . моль ледяной уксусной кислоты в 30 мл хлороформа при О- минус 5°С прибавляют раствор О.ОЗ г. моль 2,5-дихлорфенилсульфенилхло1рида 30 мл хлороформа. Температуру смеси до водят до комнатной, растворитель и летучие удаляют в вакууме при 100 С/10-15 мм рт. ст. и остаток растворяют в бензоле. В полученный раствор при вводя смесь 0,ОЗ г моль пропаргилового спирта и 0,ОЗ г-г моль триэтиламина в 2О мл бензола. Смесь нагревают 2 час при 50 С промьшают водой, сушат азеотропно, растворитель удаляют в вакууме, в остатке получают целевой продукт, Ц 1,5750; i2O d У 1,2078, выход 96%. 17,56; Р 7,49; Найдено, %; С1 S 8,37. Вычислено, %: С1 17,73; Р 7,75; S 8,01. В условиях примера 5 получают вещест во, приведенное в табл. 2 последним. Предмет изоб ретения Способ получения тиолфосфонатов общей ормулы где R - замещенный или незамещенный фенил или бензил; ( - незамещенньй или замещенный фенил, аралкил, циклоалкил, алкенил, алкинил, этилтиоэтил, алкоксиэтил, арилоксиэтил или группа - N asCCCH,); алкил или арил, отличающийся тем, что соответствующий ди- хлорфосфин подвергают взаимодействию с сульфенилхлоридом в присутствии уксусной кислоты с последующими обработкой образующегося эфирхлорангидрида фенолом, спиртом или ацетоксимом в присутствии третичного амина и вьщелением целевого продукта известными приемами.
Авторы
Даты
1974-11-25—Публикация
1971-08-23—Подача