1
Изобретение относится к области получения новых производных изоиндолина, которые могут найти применение в фармацевтической промышленности.
Используя известные реакции - обменную или алкилирования применительно к соединениям изоиндолинового ряда, можно получить повые соединения общей формулы I
Z представляет собою атом кислорода или серы; п 0 или 1.
Иредлагаемый способ получения производных изоипдолина общей формулы I заключается в том, что в случае, когда Z представляет собой атом кислорода, пиперазин общей формулы II Ar - фочпльный радикал, замещенный или иезамещеишяи. Реакция обычно осуществляется в органическом растворителе, таком как ацетонитрил и при температуре около 20°С. В случае, когда Z - атом кислорода пли серы, иинеразин общей формулы IV Ci-CZ-N N-KI И где Z и RI имеют выщеуказанные значения подвергают взаимодействию с щелочной солью производного изонпдолина общей формулыгде X, Y и п имеют вышеуказанные значения. Обычно реакция осуществляется в органи ческом растворителе, таком как диметилформамиде, при температуре ниже 50°С. Новые соединения формулы I могут, быть очищены физическими способами, такими как дистилляция, кристаллизация, хроматография, или химическими, такими как солеобразование, кристаллизация солей, затем разложение в щелочной среде. В этих операциях природа аниона соли не имеет значения, существует единственное условие, которое заключается в том, что соль должна быть соверщенно определенной и легко кристаллизующейся. Новые вещества согласно изобретению могут быть преобразованы в аддитивные соли с кислотами. Эти аддитивные соли могут быть получены путем воздействия новых соединений на кислоты в соответствующих растворителях. В качестве органических растворителей применяют, например, спирты, эфиры, ацетоны или хлорированные растворители. Образованная соль осаждается при достижении необходимой концентрации из своего раствора и отделяется путем фильтрации или отстаивания. Пример 1. Неремещивают при температуре около 20°С и в течение 48 час смесь из 3,5 г смешанного карбоната фенила и 1-окси(пиридил-2)-2-изоиндолипила-3 с 2 г метил-4пиперазина в 20 см ацетонитрила. Затем отфильтровывают откристаллизованное нерастворимое белое вещество и собирают таким образом после высушивания 2,5 г вещества с г. пл. 170°С. Путем повторной кристаллизации в 30 см ацетонитрила получают 2,1 г 4-метилпиперазинокарбонилокси) - 3-(ниридил-2) - 2изоиндолинона-1 с т. пл. 171°С. Смсп1а ный карбонат фенила и окиси-1(ниридил-2) -2-изоиндолинила-З может быть получен путем добавления в течение 80 мин при перемешивании и поддержании темнературы в пределах 5-8°С, 145,3 г хлороформиатафенила к раствору из 200 г 3-окси-(пиридил-2)-2-изоиндолинона-1 в 1000 см безводного пиридина. Затем реакционную смесь оставляют на 4 час при температуре около 20°С, потом сливают ее в 3000 см воды. Вещество кристаллизуется с последующим выделением его путем фильтрации; его промывают три раза 400 см воды и высушивают. Таким образом получают 297 г белых кристаллов с т. нл. 155°С. Путем повторной кристаллизации в 1000 см ацетопитрила собирают 173,9 г смешанного карбоната фенила и 1-окси-(ниридил2)-изоиндолинила-3 ст. пл. 164°С. 3-Окси- (пиридил-2) -2-ИЗОИНДОЛИНОН-1 может быть получен путем медленного добавления при перемешивании и поддержании температуры между 20-30°С, раствора из 2 г борогидрида калия в 18 см воды и 2 см 1 н. гидроокиси натрия в суспензию из 11,2 г 2-фталимидопиридина в 50 см метанола. После 20 час при температуре около 20°С отделяют нерастворимое вещество путем фильтрации, затем его высушивают. Таким образом получают 8,3 г 3-окси-(пиридил-2)-2-изоиндолинопа-1 ст. пл. 140°С. Пример 2. В суспензию из 2,8 г гидрида патрия (покрытого на 54% минеральным маслом) в 30 см безводного диметилформамида быстро добавляют раствор из 12,9 г 3-окси(пиридил-2)-2-изоиндолинона-1 в 100 см безводного диметилформамида, поддерживая температуру около 27°С. Когда заканчивается выделение газов, медленно добавляют, поддерживая температуру между 25-35°С, 9,3 г 4-метилхлоркарбонил-1-пиперазин. Перемешивают еще в течение 20 мин после окончания добавления, затем сливают реакционную смесь в 1000 см ледяной воды. Полученное откристаллизованное вещество отделяется путем фильтрации, затем его промывают в 150 см воды. После высушивания получают 18,7 г вещества с т. пл. 169-170°С. Путем повторной кристаллизации в 160 см ацетонитрила получают 16,4 г 4-метил-(пиперазинокарбонилокси)-3 - (пиридил-2) - 2-изоиндолинона-1 с т. пл. 172°С. Пример 3. В суспензию из 19 г смещанного карбоната фенила и 1-окси-5-хлор-(пиридил-2)-2-изоиндолинила-З в 100 см ацетотонитрила добавляют 10 г 4-метилпиперазина в 25 см ацетонитрила. Затем оставляют суспензию на 24 час при температуре около 20°С, потом отделяют нерастворимое вещество путем фильтрации. Таким образом собирают 12,8 г твердого вещества с т. пл. около 162- 164°С. Это вещество растворяется в 650 см ацетона. Отделяют легкий нерастворимый осадок путем фильтрации, затем добавляют в фильтрат 34,5 см молярного раствора пикриновой
кислоты в ацетоне. Желтое вещество медленно кристаллизуется. Его выделяют путем фильтрации и получают 21,8 г кристаллов с т. пл. 240°С.
Соединение перемешивают в смеси из 300 см воды, 400 см метиленхлорида и 40 см I и. раствора гидроокиси лития. Органический слой отделяют и из водной фазы экстрагируют за два раза 100 см метиленхлорида. Соединенные органические фракции промывают в 250 см воды и высушивают 40 г карбоната калия и 20 г окиси алюминия. После фильтрации выпаривают летучие веш,ества под небольшим давлением и таким образом получают 12,7 вешества, которое повторно кристаллизовано в 150 см этанола, дает 11,2 г 4-метил-(пиперазино)-карбонил-3окси-5-хлоро-(ниридил - 2)-изоиндолинона-1 с т. пл. 165--16б°С.
Смешанный карбонат фенила и 1-окси-5хлоро- (пиридил-2) -2-изоиндолинила-З может быть получен путем добавления в процессе перемешивания при 20°С 35,2 г хлороформиата фенила к 39 г 5-хлоро-3-окси-(пиридил2)-2-изоиндолинона-1, растворенного в 750 см безводного пиридина. Через 15 час содержания при температуре около 20°С сливают реакционную смесь в 4 л дистиллированной воды. Веш,ество кристаллизуется с иоследуюШИР«1 выделением его путем фильтрации и после высушивания получают 56,8 г смешанного карбоната фенила и 1-окси-5-хлоро-(пиридил-2)-2-изоиндолинила-З с т. пл. 160°С.
5-Хлоро-З-окси-(пиридил-2) - 2 - изоиндолинон-1 может быть получен путем добавления в течение 30 мин при температуре 25- 35°С раствора 17,75 г борогидрида натрия в 200 см метанола в суспензию из 161 г (4хлорфталимидо)-2-пиридина в 870 см метанола. Сначала происходит растворение, затем в активной среде осаждается твердое вещество. Перемешивают еще в течение 2 час при 20°С. Появившийся осадок отделяют фильтрацией. После высушивания собирают 143 г вещества с т. пл. 180°С. Это вещество растворяется в 800 см диметилформамида нагреванием с обратным холодильником. После охлаждения выделяют 40,1 г нерастворимого вещества, затем выпаривают фильтрат под небольшим давлением и остаток растворяют в 7000 см ацетона. Отделяют еще 11,7 г нерастворимого вещества путем фильтрации, затем добавляют к ацетоновому раствору 63,6 г пикриновой кислоты, растворенной в 200 см ацетона. Выкристаллизовывается желтое вещество, которое отделяется путем фильтрации. После высушивания получают 93,9 г пикрата ст. пл. 210°С.
Пикрат берут в суспензии в 940 см дистиллированной воды, затем добавляют раствор 8,1 г гидроокиси лития (концентрации 57%) в 200 см воды. Перемешивают в течение 2 час. После фильтрации получают 104 г сырых кристаллов с т. пл. 190°С. Путем повторной кристаллизации в 900 см бутанола получают 43,8 г 5-хлор-3-окс1 -(11пр11Дил-2)-2-изоиндолпнона-1 с т. пл. 193°С.
(4-Хлорфталимидо) -2-пиридин может быть получен нагреванием до 200°С в течение 10 мин смеси 128 г 4-хлорфталевого ангидрида и 65,8 г 2-аминопиридина в 350 см окиси фенила. Реакционную смесь оставляют при 35-40°С и добавляют 350 см эфира анестезина. Кристаллизованный продукт выделяют фильтрацией, затем высушивают. Таким образом получают 161 г (4-хлорфталимидо)-2пиридина с т. пл. 155°С.
Пример 4. Добавляют 10,2 г 4-метилпиперазина к суспензии из 20 г смешанного карбоната фенила и 6-нитро-1-окси-(пиридин2)-2-изоиндолинила-З в ПО см ацетонитрила. После выдержки в течение 18 час появляются кристаллы, их отделяют фильтрацией. Таки.м образом получают 18,8 г вещества с 0 т. пл. 205°С.
Вещество растворяется в 2200 см бензола. После удаления легкого нерастворимого осадка путем фильтрации раствор пропускают через 470 г силикагеля, находящегося в колон5 ке диаметром 5,8 см. Затем SiOo элюируют 1000 см смеси бензолэтилацетат (с объемным соотношением 1:1), 3500 см смеси бен золэтилацетат (с объемным соотношением 1:3), 500 см- чистого этилацетата и 1000 мл 0 смеси этилацетатметанол (в объемном соотношении 95:5). Все эти элюаты отделяются. Затем Эv юиpyют 6000 см смеси этилацетата метанола. Полученный раствор выпаривают под небольшим давлением. Получают 16,4 г 5 вещества с т. пл. 218°С (с превращением при 210°С). Путем повторной кристаллизации в 600 см ацетонитрила собирают 14,8 г (4-метилпиперазино)-карбонил-3-окси-6-нитро - (пиридил-2)-2-индолинона-1 с т. пл. 218°С (с пре0 вращением нри 210°С). Структура этого вещества подтверждается спектром ядерного магнитного резонанса.
Смешанный карбонат фенила и 6-нитро-1окси- (пиридил-2) -2-изоиндолинила-З может 5 быть получен путем добавления 23 г хлопоформиата фенила к суспензии из 26,9 г 3-окси-6-нитро- (пиридил-2) -2-изоиндолинола-1 в 550 см безводного ниридина, поддерживая температуру около 6°С. Оставляют в течение 0 18 час при температуре около 20°С, затем сливают реакциопную смесь в 2700 см воды. Вещество кристаллизуют для отделения его фильтрацией. После высушивания нолучают 37,4 г смешанного карбоната фенила и 6-ии55 тро-1-окси-(пиридил-2) - 2 - изонндолинила-3 ст. ил. 210°С.
З-Оксн-6-нитро-(пиридил-2) - 2 - изоиндолинон-1 может быть получен, как указано в примере 5.
60 Пример 5. В суспензию из 13.4 г смешанного карбоната фенила и 5-нитро-1-окси-(ниридил-2)-2-изоиндолинила-З в 67 см ацетонитрила добавляют 7,4 г 4-метилнинеразина. Температура поддерл ивается около 25°С, затем оставляют на 18 час при 20°С. Потом отделяют кристаллы путем фильтрации и, после высушива пг/, получают 12,2 г вещества с т. пл. 238-245°С. Эти кристаллы растворяют в 1500 см бензола и полученный раствор пропускают через 300 г силикагеля, содержащегося в колонке диаметром 4,4 см. Элюируют 500 см смеси бензол-этилацетат (в соотношении объемном 1:1), 500 см чистого этилацетата и 500 см смеси этилацетат-метанол (в объемном соотнощении 95 : 5). Все эти элюаты отделяют. Затем элюируют 800 см смеси этилацетатметанол с объемным соотношением 9:1. После вынарнвания растворителей под низким давлением получают 10,6 г кристаллизованного веш,ества. После двух новторных кристаллизации в диметилформамиде получают 7,2 г 4-метил-(ниперазино)-карбонил-3-окси-5-нитро-(пиридил-2) - 2-изоиндолннона-1 с т. пл. 258°С.
Структура этого вещества подтверждается спектром ядерного магнитного резонанса.
Смешанный карбонат фенила и 5-нитро-1окси-(пириднл-2)-2-нзоиндолинила - 3 может быть получен при воздействии 11,5 г хлороформиата фенила на суспензию из 13,2 г 3-окси-5-нитро-(пиридил-2) - 2 - изоиндолинона-1 в 270 см безводного пиридина, поддерживая температуру около 5°С. Затем оставляют в течение 18 час при температуре около 20°С, затем сливают реакционную смесь в 1380 см воды. Отделяют кристаллы путем фильтрацнн и промывают их 3 раза в 100 см воды. После высушивания получают 19,1 г вещества с т. пл. порядка 175-179°С. Путем повторной кристаллизацией в 160 см ацетонитрила собирают 13,4 г смешанного карбоната фенила и 5-нитро-1-окси-(пиридил-2)-2-изоиндолинила-3 с т. пл. 188°С.
З-Окси-6-нитро- (ниридил-21) -2-изоиндолинон-1 и 3-окси-5-нитро-(ниридил-2) - 2 - изоиндолинон-1 могут быть получены следуюшим образом.
Добавляют 6,8 г борогидридонатрия в растворе в 105 см метанола к суспензии из 64 г (4-нитрофталимидо)-2-пиридина в 320 см метанола, поддерживая температуру 20°С. Оставляют реакционную смесь на 2 час нри этой температуре, затем отделяют нерастворимый осадок путем фильтрации. Получают 58,5 г кристаллов с т. пл. 234-236°С. Их растворяют в 295 см кипящего диметилформамица. Горячий раствор обрабатывают обесцвечивающим углем, фильтруют, затем охлаждают. Выделяют кристаллы и собирают таким образом 29,5 г 3-окси-6-нитро-(пиридил-2)-2изоиндолинона-1 с т. пл. 268°С.
Маточные растворы затем выпаривают под низки.м давлением. Получают 29,6 г желтооранжевого осадка, который растворяется в 5000 см ацетона. Легкое нерастворимое вещество отстаивается с целью удаления его путем фильтрации, затем добавляют в фильтрат раствор 24,5 г пикриновой кислоты в 50 см ацетона. Желтое вещество медленно кристаллизуется. После выдерживания при
4°С в течение 12 час отделяют путем фильтрации кристаллы и получают 22,2 г вещества с т. пл. 226-227 С. Путем концентрации ацетонового раствора получают еще 7,1 г вещества ст. пл. 215--216°С.
Оба предыдущие вещества соединяют, затем взвешивают в суспензии в 550 см воды. Добавляют при перемешивании раствор из 2,9 г гидроокиси лития (концентрация 57%) в
80 см воды. Энергично перемешивают в течение 4 час, затем фильтруют. После высушивания получают 16,1 г 3-oкcи-5-нитpo-(ниpидил-2)-2-изoиндoлинoнa-l с т. пл. 224-225°С. (4-Нитрофталимидо)-2-пиридин молсет быть
получен нутем нагревания в атмосфере азота в течение 25 мин до 190°С, смеси 45,5 г 4-нитрофталевого ангидрида и 22,2 г 2-аминониридина в 135 см окиси фенила. Оставляют остывать, затем добавляют 225 см этанола.
Отделяют кристаллизованный нродукт путем
фильтрации. Таким образом получают 60,9 г
(4-нитрофталимидо-2)-пиридина с т. пл.
183°С.
Прим ер 6. К суспензии из 2,22 г гидрида
натрия (на 50% покрытого минеральным маслом) в 80 см безводного диметилформамида добавляют суспензию из 10,4 г 3-окси-(5-хлорпиридил-2)-2-изоиндолинона-1 в 80 см безводного диметилформамида, ноддерживая
температуру около 27°С. Когда прекращается выделение газов, добавляют раствор из 7,15 г хлорокарбонила-1-4-метилпиперазина в 15 см безводного диметилформамида, поддерживая температуру около 30°С. Перемешивают еше
в течение 1 час после окончания добавления, затем сливают реакционную смесь в 800 см ледяной воды. Клеевидное вешество, которое осаждается, ностененно отвердевает. Оно отделяется путем фильтрации, затем промывается в 200 см воды. После высушивания под низким давлением (30 мм рт. ст.) получают 15,2 г вещества с т. нл. 165-167°С.
После повторной кристаллизации в 170 см ацетонитрила получают 13,9 г вещества с
т. нл. 170°С. Это вещество растворяется в 100 см хлороформа и раствор пропускают через 175 г силикагеля, находящегося в колонке диаметром 4,5 см. Затем элюируют в 1500 см хлороформа, этот элюат удаляют. Промывают в 1000 см этилацетата и в 1000 см метанола. Полученные растворы соединяют, выпаривают под пониженным давлением (30 мм рт. ст.). Путем повторной кристаллизации полученного таким образом вещества в 180 см
ацетонитрила получают 11 г 4-метилпиперазинокарбонил-3-окси(5-хлорнириднл - 2) - 2-изоиндолинона-1 с т. пл. 171°С.
3-Окси-(5-хлорпиридил-2) - 2 - изоиндолинон-1 может быть нолучен путем медленного
добавления нри неремешивании и при ноддержании температуры около 6°С раствора 2,65 г борогидрида калия в 26,5 см воды и 3,3 см 1 н. раствора NaOH в суспензию 17,1 г 2-фталимидо-5-хлоропиридина в 330 см метанола. После выдерживания в течение 15 час
при температуре около 20°С нерастворимое вещество отделяют путем флотации, затем промывают 40 см метанола. После высушивания получают 15,3 г 3-oкcи-(5-xлopoпиpидил2)-2-изoипдoлинoнa-l с т. пл. 185-186°С.
2-Фталимидо-5-хлорпиридин может быть получен путем нагревания с обратным холодильником в течение 1 час смеси из 14,8 г фталеБого ангидрида и 12,85 г 2-амино-5-хлорпиридина в 150 см уксусной кислоты. После охлаждения сливают реакционную смесь на 500 г льда. Вещество, которое кристаллизуется, отделяют фильтрованием, затем промывают в 200 см воды. После высушивания нолучают 20 г 2-фталимидо-5-хлорпиридина с т. пл. 150°С.
Пример 7. В суспензию 1,35 г гидрида натрия, покрытого на 50% минеральным маслом, в 50 с.м безводного диметилформамида, добавляют раствор 6,5 г 3-окси-(6-хлорпиридил-2)-2-изоиндолинона-1 в 50 см безводного диметилформамида, ноддерживая температуру около 27°С. Когда прекращается выделение газов, добавляют раствор 4,55 г 1-хлоркарбонил-4-метилпиперидина в 10 см безводного диметилформамида, поддерживая температуру около 30°С. Перемешивают еще в течение 1 час после окончания добавки, затем сливают реакционную смесь в 540 см ледяной воды. Вещество, которое кристаллизуется, отделяют фильтрацией, затем промывают в 100 см воды. После высушивания получают 9,1 г вещества с т. пл. 174-175°С.
Путем повторной кристаллизации в 175 см этанола получают 7 г (4-метилпиперазнно)карбонил-3-окси-(б-хлорпиридил-2) - 2 - изоиндолинона-1 с т. пл. 179°С.
3-Окси-(6-хлорпиридил-2)-2-ИЗОИНДОЛИНОП-1 может быть получен при медленном добавлении при перемешивании и температуре около 6°С раствора 1,15 г борогидрида калия в 12 см воды и 1,5 см 1 н. раствора едкого натра к суспензии 7,3 г 2-фталимидо-6-хлорпиридина в 150 см метанола. После выдерживания в течение 20 час при 20°С перастворимое вещество отделяют фильтрацией, затем промывают 20 см метанола. После высушивания получают 6,1 г 3-окси-(6-хлорпиридил-2)-2-изоиндолинона-1 с т. пл. 164°С.
2-Фталимидо-6-хлорпиридин может быть получен путем нагревания с обратным холодильником в течение 2 час 40 мин смеси 5,45 г фталевого ангидрида и 4,7 г 2-амино-6-хлорпиридина в 50 см уксусной кислоты. После о.хлаждения сливают реакционную смесь на 150 г льда. Появившееся кристаллизованное вещество отделяют путем фильтрации, затем промывают в 100 см воды. После высушивания получают 7,3 г 2-фталимид-6-хлорпиридпна ст. пл. 177°С.
Пример 8. В суспензию 1,7 г гидрида натрия (покрытого на 50% минеральным маслом) в 65 см безводного диметилфермамида добавляют суспензию 8,3 г 3-окси-(3-хлорпиридил-2)-2-изоиндолинона-1 в 65 см безводного диметилформамида, поддерл ивая температуру около 27°С. Когда прекращается выделение газов, добавляют раствор 5,65 г 1-хлоркарбонил-4-метилниперазина в 10 безводного диметилформамида, поддерживая температуру около 30°С. Перемешивают еще в течение 1 час после окончания добавления, затем сливают реакционную смесь в 700 ледяной воды. Маслянистый продукт, который
не растворяется, экспрагируется с помощью 1000 см хлороформа. Полученный раствор промывают в 200 см воды, высушивают сульфатом натрия, затем выпаривают под пониженным давлением. Получают 14,3 г масляпястого вещества, которое путем кристаллизации в из 100 см циклогексана и 200 см окиси изопропила образует 9,1 г (4-метилпиперазино)-карбонил-3-окси - (3-хлорпиридил2)-2-изоинодолинона-1 с т. пл. 100°С (сельватированиого 8% циклогексаном).
3-Окси-(3-хлорпцридцл-2) - 2 - изопндолинон-1 может быть получен путем медленного добавления при перемешивании и температуре около 6°С раствора 2,97 г борогидрида
калия в 30 см воды и 3,7 см раствора NaOH в суспензии из 19,1 г 2-фталимидо-З-хлорпиридин в 380 см метанола. После 15 час выдерживания при температуре около 20°С перастворимое вещество отделяют путем фильтрации, затем промывают 20 см метапола. После высуцшвания получают 8,3 г 3-оксп-(3хлорпиридил - 2) - 2-изоиндолпнона-1 с т. пл. 240°С.
2-Фталимид-3-хлорпирид1:и может быть иолучей путем narpenaniiCM с обратным холодильником в течение 2 час 32,2 г фталевого ангидрида и 28 г 2-амин-З-хлорпиридина в 280 см- уксусной кислоты. После охлаждения сливают реакцпопную смесь на1000 г льда. Вещество, которое осаждается, экстрагируется с 500 см хлороформа. Полученный раствор промывается 100 см 1 н. раствора NaOH, затем 200 см воды, высушивают сульфатом патрия и выпаривают досуха
при пониженном давлении (30 мм рт. ст.). Таким образом получают 19,3 г 2-фталимцдо3-хлорпиридима с т. пл. 140°С.
Пример 9. В суспензию из 1,47 г гидрида натрия (покрытого на 50% минеральным маслом) в 55 см безводного диметилформамида добавляют суспензию из 7,15 г 3-окси(4-хлорпиридил-2) - 2 - изоиндолинона-1 в 55 см безводного диметилформамида, поддерживая температуру около 27°С. Когда прекращается выделение газов, добавляют раствор 4,8 г 1-хлоркарбонил-4-.метилпиперазина в 10 см безводного диметилформамида нри 30°С. Перемсгнивают еще в течение 1 час поеле окончания добавления, затем сливают реакционную смесь в 600 см ледяной воды. Вещество, которое кристаллизуется, отделяют фильтрацией, зате.м промывают 60 см воды. После высушивания получают 10,3 г вещества с т. пл. 190-192°С.
11 После двойной рекристаллизации, первой в 200 см ацетонитрила и второй в 450 см ацетона, получают 6,3 г {4-метилпиперазино)-3карбонилокси-(4-хлорпиридил-2) - 2 - изоипдолинона-1 с т. пл. 193°С. 3-Окси-(4-хлорпиридил-2) - 2 - изоиндолинон-1 может быть получен путем медленного добавления при перемешивании и 7°С раствора 1,2 г борогидрида калия в 12 см воды и 1,5 см 1 и. раствора iNaOH в суспензию из 8 г 2-фталимидо-4-хлорпиридина в 160 см метанола. После выдерживания в течение 20 час при 20°С нерастворимый продукт отделяют фильтрацией, затем промывают в 20 см метанола. После высушивания получают 7,15 г 3-окси(4-хлорпиридил-2)-изоиндолинона-1 с т. пл. 196-197°С. 2-Фталимидо-4-хлорпиридин может быть получен путем нагревания с обратным холодильником в течение 90 мин смеси 3,7 г фталевого ангидрида и 3,2 г 2-амиио-4-хлорпиридина в 35 см уксусной кислоты. После охлаждения сливают реакционную смесь на 150 г льда. Продукт, который кристаллизуется, отделяют путем фильтрации, затем промывают в 60 воды. После высушивания получают 4,2 г 2-фталимидо-4 - хлорпиридина с т. пл. 157-158°С. Пример 10. В суспензию из 9,8 г смешанного карбоната фенила и 1-окси-5-нитро(5-хлорпиридил-2)-2-изоиндолинила-З в 60 см ацетонитрила добавляют 4,6 г 1-метилпиперазина. Оставляют затем суспензию в течение 18 час при температуре около 20°С, затем отделяют нерастворимое вешество путем фильтрации. Собирают таким образом 12,8 г твердого вещества с т. пл. 180-182°С. Путем рекристаллизации в 140 см ацетонитрила получают после высушивания 6,15 г (5-хлорпиридил-2)-2-(4-метилпиперазино) - 3карбонилокси-5-нитроизоиндолинона-1 с т. пл. 187-188°С. Смешанный карбонат фенила и 1-окси-5-нитро- (5-хлорпиридил-2) -2-нзоиндолинила-З может быть получен путем добавления в суспензию 9,5 г (5-хлорпиридил-2)-2,3 - окси-5-нитроизоиндолинона-1 в 190 см безводного пиридина, 7,5 г хлорформиата фенила, поддерживая температуру около 5°С. Затем оставляют реакционную смесь в течение 16 час при температуре около 20°С, затем сливают ее в 1350 см ледяной воды. Продукт, который кристаллизуется, отделяют путем фильтрации, затем промывают в 100 см воды. Таким образом получают 13,7 г продукта с т. пл. 185°С. Путем рекристаллизации в 185 см ацетонитрила получают 10,4 смешанного карбоната фенила и 1-окси - 5 - нитро-(5-хлорпиридил-2)2-изоиндолинила-З с т. пл. 194°С. (5-Хлорпиридил-2) - 2,3 - окси-5-нитроизоиндолинона-1 может быть получен путем добавления 4,6 г борогидрида калия в суспензию из 33,5 г К-(5-хлорпиридил-2)-4-нптрофталимида в 335 см диоксана, поддерживая
12 емпературу около 15°С. Реакционную смесь ыдерживают при 22°С в течение 5 час, заем охлаждают при 10°С. В этом случае доавляют сразу 116 см воды; продукт, который ристаллизуется, отделяют путем фильтрации, атем промывают в 30 см смеси вода-диксан с объемным соотношением 2:1. В ильтрат добавляют сразу же 580 см воды вещество, которое осаждается, отделяют утем фильтрации, затем промывают в 60 с.м оды. После высушивания получают 7 г (5-хлорпиридил-2)-2,3 - окси-5-нитро - 5-изоиндолинона-1 с т. пл. 244-246°С. Ы-(5-Хлорпиридил-2)-4-нитрофталимид с т. пл. 180°С может быть получен пагреванием в атмосфере азота в течение 25 мин и при 190°С смеси 4-нитрофталевого ангидрида и 2-амино-5-хлорпиридина в окиси фенила. Пример 11. Действуя как в примере 10, из 6,2 г смешанпого карбоната фенила и 1-окси-5-хлоро-(5-хлорпиридил-2) - 2 - изоиндолинила-3 и 5 г 1-метилпиперизина получают 4,35 г (5-хлорпиридил-2)-2-(4-метилпиперазино) - 3 - карбонилокси-5-хлоризоиндолинона-1 с т. пл. 154°С. Смешанный карбонат фенила и 1-окси-5хлоро-(5-хлорпиридил-2) - 2-изоиндолинила-З с т. пл. 128°С может быть получен путем воздействия (5-хлорпиридил-2)-2,3-окси-5 - хлоризоиндолинона-, на хлороформиат фенила при 5°С. (5-Хлорпиридил-2)-2,3 - окси - 5-хлоризоиндолинон-1 может быть получен путем добавления 5,8 г борогидрида калия в суспензию из 40,5 г N-(5-хлорпиридил-2)-4-хлорфталимида в 600 см метанола, поддерживая температуру около 10°С. Затем оставляют реакционную смесь в течение 1 час при 20°С, затем нерастворимый продукт отделяют путем фильтрации и промывают в 100 см метанола. После высушивания получают 32,6 г продукта с т. пл. 185-190°С. Это вещество растворяют в 250 см кипяшего диметилформамида. При охлаждении продукт кристаллизуется, затем его отделяют путем фильтраци;, промывают 20 см диметилформамида. Фильтрат выпаривают досуха при пониженном давлении и полученный осадок обрабатыБа:от 700 см ацетона при 25°С. Нераствори.ый осадок отделяют фильтрацией, затем в фильтрат добавляют 50 см хлоргидридного эфира около 3 п., затем 100 см эфира. Медленно кристаллизующийся продукт отделяют фильтрацией, затем промывают в 20 см ацетона. После высушивания получают 10,7 г продукта с т. пл. с разложением. Этот продукт обрабатывают 100 см насыщенного водного раствора бикарбоната натрия и 200 см хлороформа, Водный слой отстаивается, затем его экстрагируют дважды с 100 см хлороформа. Органические экстракты соединяют, промывают три раза в 100 см воды, высушивают сульфатем натрия, затем выпаривают сухим путем под пониженным давлением. Таким образом получают 8,4 г вещества с т. пл. 180°С. После двух рекристаллизации - первой в 85 см 1,2-дихлорэтана, второй - в 70 см хлороформа, получают 4 г (5-хлорпиридил-2)-2,3-окси-5-хлор - 5 - изоиндолинопа-1 ст. пл. 184-185°С. N- (5-хлорпиридил-2) -4-хлорфталимид может быть получен путем нагрева с обратным холодильником в течение 2 час смеси 50 г 4-хлорфталевого ангидрида и 35,2 2-амино-5хлорпиридина в 550 см уксусной кислоты. Продукт, который кристаллизуется путем охлаждения, отделяют путем фильтрации, затем промывают в 200 см эфира. После высушивания получают 40,5 г Ы-(5-хлорпиридил-2)-4хлорфталимида с т. пл. 160°С. Пример 12. Производя те же операции, как и в примере 10, из 17,3 г смешанного карбоната фенила и 1-окси-(пиридил-2)-2-изоиндолинила-3 и 11,4 г 1-этилпиперазина получают 10,5 г (пиридил-2)-2-(4-этилниперазино)карбонил-З-оксиизоиндолинона-1 с т. пл. 145°С. Пример 13. Производят те же операции, как и в примере 10, из 10,4 г смешанного карбоната фенила и 1-окси-(пиридил-2) - изоиндолинила-3 и 7,8 г 1-оксиэтилпиперазина получают 12,7 г (пиридил-2)-2-(4-оксиэтилпиперазино)-3-карбонилоксиизоиндолинона-1 с г. пл.168°С. Пример 14. Производя те же операции, как и в примере 10, из 17,3 г смешанного карбоната фенила и (1-оксипиридил-2)-2-изоиндолинила-3 и 12,8 г 1-изонренилниперазина получают 14 г (пиридил-2)-2-(4-изопропилпиперазино) - 3-карбонилокси - изоиндолинона-1 ст. пл. 118-120°С. Пример 15. Производя те же операции, как и в примере 10, из 17,3 г смешанного карбоната фенила и 1-окси-(пиридил-2)-2-изоиндолинила-3 и 12,5 г 1-аллилпиперазина получают 9,3 г (пиридил-2)-2-(4-аллилпиперазино)-3-карбонилоксиизоиидолинона-1 с т. пл. ИЗ-114°С. Пример 16. Производя те же операции, как в примере 10, из 29 г смешанного карбоната фенила и 1-окси-(5-нитропиридил-2)-2изоиндолинила-3 и 29,6 г 1-метилпиперазина получают 13,5 г (5-нитропиридил-2)-2-(4-метилпиперазино-3 - карбонилоксиизоиндолинона-1 с т. пл. 214°С. Смешанный карбонат фенила и 1-окси-(5нитропиридил-2)-2-изоиндолинона-3 с т. пл. 180-183°С может быть получен путем воздействия (5-нитропиридил-2)-2,3-оксиизоиндолкнона-1 на хлороформиат фенила при 50°С. (5-Питропиридил-2) -2,3-оксиизоиндолинон-1 может быть получен за счет добавки 4,05 г борогидрида калия в суспензию из 26,9 г 2-фталимидо-5-нитропиридина в 1000 см метаиола, поддерживая температуру около 20°С. Реакционная смесь выдерживается при 20°С еще около 3 час после окончания добавки. Нерастворимое вещество отделяется путем фильтрования, затем промывается в 100 см етанола. После высушивания получают 23 i ещества с т. пл. 250-252°С. После повтор ой кристаллизации в 900 см уксусной кис оты получают 20,2 г (5-нитропиридил-2)-2-3 ксиизоиндолинона-1 с т. пл. 255°С. 2-Фталимидо-5-нитропиридин с т. пл. 222°С ожет быть получен путем воздействия 2-ами о-5-нитропиридина на фталевый ангидрид ксусной кислоте с обратным холодильником Пример 17. Действуя так же, как в при мере 10, из 11,1 г сметанного карбоната фе ила и 1-окси-(5-Щ1анопиридил-2)-2--изоиндо инила-3 и 6 г 1-метплпиперазина получаю ,2 г (5-цианопиридил-2)-2-(4-метилпиперази но)-3-карбонилоксиизоиндолинона-1 с т. пл 206°С. Смешанный карбонат фенила и 1-окси-(5 цианопиридил-2)-2-изоиндолинила-3 с т. пл 154-155°С может быть получен путем воз действия (5-цианопиридил-2) -2-3-оксиизоиндо линона-1 на хлорформиат фенила при 5°С. (5-Пианопиридил-2)-2,3-оксиизоиндолинонс т. пл. 223°С может быть получен путем воз действия борогидрида калия на 2-фталимидо 5-цианопиридин в метаноле при температур около 20°С. 2-Фталимидо-5-цианопиридин с т. пл. 195°( молсет быть получен воздействи: 2-амино-5-цианопиридина на фталевый ангил рид в уксусной кислоте с обратным холодиль Пример 18. Действуя так же, как в при мере 10, из 14,5 г смешанного карбоната фе нила п I -окси- (пиридил-2) -2- (5,6-дихлоризоин долинила)-3 и 7 г 1-метилпиперазина получа ют 8,8 г (пиридил-2)-2-(4-метилпиперазипо) 3-карбонилокси - 5,6 - дихлоризоиндолинонас т. пл. 188°С. Смешанный карбонат фенила и 1-окси-(пр ридил-2|)-2-5,6-дихлоризоиндолинила-3 с т. ш 204-205°С может быть получен путем воздег ствия (пиридил-2)-2-3-окси-5,6 - дихлоризоиь долинона-1 на хлороформиат фенила при 5°С (Пиридил-2)-2,3-окси-5,6-дихлоризоиндол1 нон-1 с т. пл. 250°С может быть получен путе воздействия борогидрида калия на (4,5-др хлорфталимидо)-2-пиридин в гидрометанол( вой среде при 20-30°С. (4,5-Дихлорфталимидо)-2-пиридин с т. п. 230°С может быть получен путем воздействи 4,5-дихлорфталевого ангидрида на 2-амин( пиридин в окиси фенила при 200°С. Пример 19. В суспензию из 3,2 г гидр да натрия (покрытого на 54% минеральны маслом) в 30 см безводного димeтилфop амида добавляют раствор из 16,5 г (5-хлор-( метилпиридил-2)-2.3-оксиизоиндолинона - 1 85 см безводного диметилформамида, подде живая температуру около 25°С. После окончания выделения газов добавл5 ют, поддерживая температуру около 25°( 10,7 г 1-хлоркарбонил-4-метилпиперазина. П ремешивают еще 2 час после окончания Д( банки, затем сливают реакционную смесь 810 см ледяной воды. Вещество, которое кр1 ;таллизуется, отделяется путем фильтрования, атем промывается в 150 см воды и 100 см жиси изопропила. После высушивания полу ают 23,7 г вещества с т. пл. 180°С. Путем )екристаллизации в 440 см ацетонитрила по1учают 20,2 г (5-хлор-б-метилпиридил-2)-2-(4.1етилпиперазино)-3 - карбонилоксиизоиндолиюна-1 с т. пл. 180°С. (5-Хлор-6-метилпиридил - 2) - 2,3 - оксиизо ндoлинoн-l с т. пл. 155-156°С может быть юлучен путем воздействия борогидрида калия la 2-фталимидо-5-хлор-6-метилпиридин в гид)ометаноловой среде при 20-30°С. 2-Фталимидо-5-хлор-6-метилниридин с т. пл. .58°С может быть получен путем воздействия зталевого ангидрида на 2-амино-5-хлор-6-меилпиридин в окиси фенила при 200°С. 2-Амино-5-хлор-6-метилпирид,ин может быть юлучен путем добавки 150 см насыщеппой кислородом воды (55 объемных частей О) в )аствор из 54 г 2-a rинo-6-мeтилпиpидинa в 550 см коипентрированпой соляной кислоты (d 1,19), поддерживая температуру около ЭД°С. Реакционная смесь выдерживается в течение 1,5 час при 25°С. затем доводится до эН 4 путем добавки 490 см раствора гидроокиси натрия (d 1,33), все время поддержизая температуру около 25°С. Осажденный тродукт отделяют фильтрованием, затем промывают в см воды. Фильтрат подщелачивают при рН 9 путем добавки 33 см раствоэа гидроокиси патрия (d 1,33). Осал деннь Й дродукт в этом случае отделяют фильтрованием, затем промывают в 40 см воды. После зысущивяния получают 44,8 г продукта с г. пл. 63°С. Путем рекристаллизации в 380 см ексана получают 25.5 г 2-амино-5-хлор-6-мегилпиридина с т. пл. 73°С. Пример 20. Действуя, как в примере 19, яз 9.8 г (5-хлор-4-метилпиридил-2)-2.3-оксиизоиндолипона-1 и 6,4 г 1-хлоркарбонил-4-мегилпиперазина получают 11.4 г (5-хлор-4-мегилпиридил-2)-2-(4-метилпиперазино) - 3-кар5онилоксиизоиндолинона-1 с т, пл. 157- 158°С. (5-Хлоро-4-метилпиридил-2) -2,3 - оксиизоипцолинон-1 с т. пл. 232-233°С может быть подучен путем воздействия борогидрида калия на 2-фталимидо-5-хлор-4-метилпнридин в гицрометаноловой среде при 20-30°С. 2-Фталимидо-5-хлор-4-метилпиридин с т. пл. 152°С может быть получен путем воздействия фталевого ангидрида на 2-амино-5-хлор-4-метилпиридин в окиси фенила при 200°С. 2-Амино-4-метил-5-хлорпиридин может быть получен путем добавки 180 см насыщенной кислородом воды (55 об. ч. Og) в растворе из 65 г 2-амино-4-метилпиридина в 650 см концентрированной соляной кислоты (d 1,19), поддерживая температуру около 80°С. Реакционную смесь затем выдерживают в течение 3 час при 25°С, доводят до рН 4, добавляя 566 см раствора гидроокиси натрия (d 1,33), поддерживая все- время температуру .около 25°С. Осажденный продукт Отделяют путем фильтрования, затем промвшают в 210 см воды. Фильтрат подщелачивают при рН 9 путем добавки 34 см раствора гидроокиси натрия (d 1,33). Продукт, осаждающийся в этом случае, отделяют фильтрованием, затем промывают в 240 см воды. После высушивания получают 45,6 г вещества с т. пл. 85-85°С. Это вещество размешивают в суспензию в 250 см гексапа, кипятят с обратным холодильником в течение 15 мин. Нерастворимый продукт отделяют путем фильтрования в горячем виде, затем промывают в 50 см кипящего гексана. После высушивания получают 8,8 г 2-амино-4-метил-5-хлоропиридина с т. пл. 152-153°С. Пример 21. Действуя так же, как в примере 19, из 11,8 г (5-метилпиридил-2)-2,3-оксиизоиндолипопа-1 и 8,8 г 1-хлор-карбонил-4-метилнинеразина получают 12,6 г (5-метилпириДил-2)-2-(4-метилпиперазино) - 3 - карбопилоксиизоиндолинопа-1 с т. пл. 180°С. (5-Метилпиридил-2)-2,3-оксиизоипдолинон-1 с т. пл. 189-190°С может быть получен путем воздействия борогидрида калия на 2-фталимидо-5-метилпиридин в гидрометаноловой среде при 20-30°С. 2-Фталимидо-5-метилпиридип с т. пл. 180°С может быть получен путем воздействия фталевого ангидрида на 2-амино-5-метилпиридин в окиси фенила при 200°С. Пример 22. Действуя, как и в примере 19, из 6,7 г (5-метоксипиридил-2)-2,3-оксиизоиндолинона-1 и 4,5 г -хлоркарбонил-4-метилпиперазина получают 8,3 г (5-метоксипиридил2)-2-(4-метилпиперазипо) - 3 - карбонилоксиизоиндолинона-1 ст. пл. 156°С. (5-Метоксипиридил-2) - 2,3-оксиизоиндоликон-1 с т. пл. 166°С может быть получен путем воздействия борогидрида калия на 2-фталимидо-5-метоксипиридин в метаноле при 20°С. 2-Фталимидо-5-метоксипиридин может быть получен добавкой раствора 6,95 г д етилсульфата в 70 см ацетона в суспензию из 12 г 2-фталимидо-5-оксипиридина и 13,8 г безводного карбоната калия в 240 см ацетоиа, соединяя их в колбе с обратным холодильником, ц нагревают в течение 80 мин после окончания добавки. После охлагкдепия реакционную смесь фильтруют и полученный раствор концентрируют сухим методом под низким давлением. Полученный пастообразный осадок перемешивают с 500 см зтилацетата при 50°С. После отделения маслянистого нерастворимого вещества этилацетат промывают отстаиванием в 225 см воды, затем высушивают карбонатом калия в присутствии обесцвечивающего угля. Раствор, полученный после фильтрации, выпаривают до 100 см. Продукт, который кристаллизуется путе.м охлаждения, отделяют фильтрованием, затем промывают в 45 окиси изопропила. После высушивания получают 6,1 г 2-фталимидо-5-метоксипиридина ст. пл. 144°С. 2-Фиалимидо - 5 - гидроксипиридин может быть получен нагреванием с обратным холо17
дильнпко.м в течение 80 мин раетвора пз 6,4 г 2-амино-5-оксипиридина и 8,8 г фталевого ангидрида в 90 ем уксусной кислоты. Кипящий раствор обрабатывают 1,5 г обесцвечивающего угля, фильтруют горячим методом. Продукт, который кристаллизуется охлаждением, отделяют фильтрованием, затем промывают в 10 см уксусной кислоты и 45 см эфира. После высущивания получают 6,45 г 2-фталимидо-5-оксипиридина с т. пл. 285°С.
Пример 23. Действуя, как и в примере 19, из 12,3 г {6-метоксипиридил-2)-2,3-оксиизоиндолинона и 8,4 г 1-хлоркарбонпл-4-метилпиперазина получают 10 г (6-мстоксипиридил-2) - 2 - (4-метилпинеразино)-3-карбонилоксиизоиндолинона-1 с т. нл. 125°С.
(6-Метоксипиридил) -2,3-оксиизоиндолинон-1 с т. пл. 148°С может быть получен воздействием борогидрида калия на 2-фталимидо-6-метоксипиридин в гидрометаноловой среде при 20-30°С.
2-Фталимидо-6-метоксипиридин с т. пл. 258°С можно получить воздействием фталевого ангидрида на 2-амино-6-метоксипиридин в уксусной кислоте в противотоке.
Пример 24. Действуя, как и в примере 19, из 15,2 г (5-бромпиридил-2)-2,3-оксиизоиндолинона-1 и 8,9 г 1-хлоркарбонил-4-метилпиперазина получают 12 г (5-бромпиридил-2)2-(метилпиперазино) - 3 - карбопилоксиизоиндолинопа-1 с т. пл. 153°С.
(5-Бромпиридил-2)-2,3 - оксиизоиндолинон-1 с т. пл. 198°С может быть получен путем воздействия борогидрида калия па 2-фталимидо5-бромпирпдип в гидрометаноловой среде при 20-30°С.
2-Фталимидо-5-бромпиридин с т. пл. 160°С получают воздействием фталевого ангидрида па 2-амино-5-бромпиридин в уксусной кислоте в противотоке.
Пример 25. Действуя, как и в примере 19, из 14 г (6-метилпиридил-2)-2,3-оксиизоиндолипона-1 и 10,5 г 1-хлоркарбонил-4-метилпиперазипа получают 14,2 г (6-метилпиридил2)-2 - (4-метилниперазино) - карбонилокси-3изоиндолипона-1 ст. пл. 124°С.
(6-Метилпиридпл-2)-2,3 - оксиизоиндолинон с т. пл. 126-127°С может быть получен воздействием борогпдрида калия па 2-фталимидо-6-метилпиридпп в гидрометаполовой среде при 20-30°С.
2-Фталимидо-6-метилпиридип с т. пл. 192°С может быть получен путем воздействия фталевого ангидрида на 2-амино-6-метилпирпдип в окиси фенила при 200С.
Пример 26. Действуя, как и в примере 19, на 15 г (5-хлорпиридил-2)-2,3-окси-5-метилизоиндолинопа-1 и 10,3 г 1-хлоркарбонил-4метилпиперазина получают 11,5 г {5-хлорпиридил-2)-2-(4-метилпиперазипо) - 3-карбонилокСи-5-метилизоиндолинопа-1 с т. пл. 149°С.
(5-Хлорпиридил-2)-2,3-окси-5 - метилизоиндолинон-1 может быть получеп путем добавки, 10,5 г борогидрида калия в раствор 10,5 г Ы-(5-хлорпиридил - 2)-4-метилфталимида в
18
105 СМ диоксана. Спустя 3 час прп 25°С до
бавляют 105 см воды, затем поддерживаю
перемещивание еще в течение 1,5 час. Добав
ляют 105 см воды, перемещпвают в течени
I час; нерастворимый продукт отделяют nyre
фильтрации, промывают в 50 см воды. Посл(
высущивапия получают 8,8 г (5-хлорпиридил)
2,3-окси-5-метилизоиндолипона-1 с т. пл. 196°С
N- (5-хлорпиридил-2) - 4 - метилфталимид (
т. пл. 152°С может быть получен путем воз действия 4-метилфталевого ангидрида па 2 амипо-5-хлорпиридин в окиси фенила пр: 200°С.
Пример 27. В суспензию 2,64 г гидрид;
натрия (покрытого на 50% минеральным мае лом) в 20 см безводного дпметилформамид; добавляют раствор 13,7 г (З-метил-5-хлорпи ридил-2)-2,3-оксиизоиидолипопа-1 в 100 см безводного диметилформамида, поддержпва5
температуру около 20°С. Когда закапчиваетс5
выделение газов, добавляют раствор 9 :
1-.хлоркарбонил-4-метилппперазипа в 20 см
безводпого диметилформа: 1ида.
После окончания добавки перемещиваю
еще в течение 3 час при температуре околс 20°С, затем сливают реакционную смесь j 1000 см ледяной воды. Клейкое вещество, ко торое осаждается, экстрагируют с 500 см эфира. Органический слой отстаивается, ег(
промывают в 100 см воды, высущивают суль фатом натрия, выпаривают досуха. Получен ный осадок растворяют в 200 см смеси мети ленхлорид - этилацетат с соотнощением объе мое 3: 1. Полученный раствор пропускают че
рез 180 г силикагеля, помещенного в кoлoнк диаметро.м 4 см. Затем последовательно обра батывают 400 см смесп метилепхлорид-этил ацетат (соотпошепие объемов 3:1) и 800 см смеси метилен.хлорид-этилацетат (соотноще
ние объемов 1:1). Все элюаты отделяют. За тем обрабатывают с помощью 2800 см чисто го этилацетата, 200 см смеси этилацетата- метанола (соотноиление объемов 3:1). Элюа ты соединяют и выпаривают при пониженнол
давлении. Таким образом получают 16,8 i медленно кристаллизующегося маслянистогс вещества. После двух рекристаллизации - первой в 44 см смесп цнклогексанбепзол (со отнощение объемов 3: 1) и второй-в 260 смсмеси циклогексан-эфир (соотнощение объе .мов 1:1) получают 10,7 г (З-метил-5-хлорпИ ридил-2) - 2-(4-метилпиперазино)-3-карбонилоксиизоиндолинона-1, растворенного 10,4% пым циклогексаном с т. пл. 105-106°С.
(5-Хлор-3-метилпиридил-2)-2,3 - оксиизоип долинон-1 с т. пл. 185-186°С может быть получен путем воздействия борогидрида калия на 2-фталимидо-5-хлор-3-метилппридин в гид рометаполовой среде прп 20-30°С.
2-Фталимид-5-хлор-5-метилпиридин с т. пл
145°С получают воздействием фталевого ан
гидрида на 2-амино-5-хлор-3-метилпиридин г
окиси фенила при 200°С.
2-Амино-5-хлор-3-метилпиридин может быт1:
получен добавлением 134 см насыщенно)
19
кислородом воды в 55 об. ч. в раствор 64,8 г 2-амино-З-метилпиридина в 650 см концентрированной соляной кислоты (d 1,19), ноддерживая температуру около . Реакционную смесь затем выдерживают в течение 2 час при 25°С, доводят до рН 8 добавкой 615 см раствора гидроокиси натрия (d 1,33). Осажденное вещество отделяют фильтрованием, промывают в 300 см воды. После высушивания получают 70,5 г продукта с т. кип. 67°С. После рекристаллизации в смеси окись изопропил-гексан (соотношение объемов 2:1) получают 59,6 г 2-амино-5-хлор-3-метилпиридина с т. пл. 68°С.
Пример 28. Действуя так же, как и в примере 10, из 10 г смешанного карбоната фенила, 1-окси- (3,5-дихлорпиридил-2) -2-изоиндолинила-3 и 4,8 г 1-метилпиперазина получают 5,1 г (3,5-дихлорпиридил-2)-2-(4-метилпиперазиио) -З-карбонилоксиизоипдолинона-1, растворенного 8,9%-ным циклогексаном, с т. пл. 96- 97°С после рекристаллизации в смеси циклогексан-эфир (соотношение объемов 3:2).
Смешанный карбонат фенила и 1-окси-(3,5дихлорпиридил-2)-2 - изоиндолинила-3 с т. пл. 134°С может быть получен путем воздействия (3,5-дихлорпиридил - 2)-2,3-оксиизоиндолинона-1 на хлороформиат фенила при 5°С.
(3,5-Дихлорпиридил-2)-2,3 - оксиизоиндолинон-1 с т. нл. 180°С может быть получен путем воздействия борогидрида калия на 2-фталимидо-3,5-дихлорпиридин в гидрометаноловой среде при 20-30°С.
2-Фталимидо-3,5-дихлорпиридин с т. пл. 160-162°С может быть получен воздействием фталевого ангидрида на 2-амино-3,5-дихлорпиридин в уксусной кислоте в противотоке.
Пример 29. Перемешивают при 20°С в течение 24 час смесь 13,5 г окиси-(1-окси-Зфенилоксикарбонилоксиизоиндолинил - 2) - 2пиридина с 7,5 г 1-метилпиперазина в 500 см ацетонитрила. Реакционную смесь выпаривают досуха при попи кенном давлении. Таким образом получают маслянистый осадок, который растворяется в 250 см хлороформа. Полученный раствор пропускают через 200 г силикагеля, помещенного в колонке диаметром 5 см. Затем последовательно обрабатывают 600 см хлороформа, 300 см смеси хлороформ-этилацетат (соотношение объемов 1:1) и 1500 см чистого этилацетата. Все эти элюаты отделяют. Обрабатывают 1500 см смеси этилацетат-метанол (соотношение объемов 1:1). Полученный раствор выпаривают досуха при пониженном давлении. Таким образом получают 11,1 г бледно-желтого масла, медленно кристаллизующегося. Рекристаллизацией в смеси метанол-окись изопропила (соотнощение объемов 1 :4) получают 5,7 г окиси (4-метилпиперазино)-3 - карбонилокси - (1-оксиизоиндолинил-2)-2-пиридипа с т. пл. 168°С.
Окись (1-окси-З-фенилоксикарбонилоксиизоиндолинил-2)-2-пиридина можно получать добавкой 9,7 г хлорформиата фенила к суспенЗИИ 14,3 г (1-окси-3-гидроксиизоиндолинил-2)20
2-ниридииокись в 150 см безводного пиридина, поддерживая температуру около 4°С. Реакционную смесь выдерживают при 20°С в течение 18 час, затем сливают в 1000 см ледяной воды. Продукт, который кристаллизуется, отделяют фильтрованием, промывают в 60 см воды. После высушивания получают 9,2 г (окси-1-фенилоксикарбонилокси - 3 - изоиндолинил-2)-ниридинокиси с т. нл. 142°С.
Окись (1-окси-3-гидроксиизоиндолинил-2)2-пиридина можно нолучить путем добавки 113 см насыщенной кислородом воды со 110 об. ч. Оа в раствор 113 г (пиридил-2)-2-3гидроксиизоиндолинона-1 в 250 см уксусной
кислоты, поддерживая температуру 75°С. Реакционную смесь выдерживают при 75°С в течение 18 час, затем сливают в смесь 2000 см хлороформа, 100 см насыщенного водного раствора хлорида натрия и 500 г карбоната
калия. Перастворимые минеральные соли отделяют фильтрованием, промывают 200 см хлороформа. Полученный хлороформный раствор промывают 100 см насыщенного водного раствора натрия, высушивают карбонатом
калия в нрисутствии обесцвечивающего угля, фильтруют, затем выпаривают досуха при пониженном давлении. Полученный остаток обрабатывают в 400 см воды при 60°С и нерарастворимый продукт отделяют фильтрованием, промывают в 50 см воды. Охлажденный фильтр насыщают 300 г хлорида натрия, затем экстрагируют в 450 см хлороформа. Полученный хлороформный раствор высушивают сульфатом натрия, концентрируют до объема 100 см. Закристаллизованный путем охлаждения в ванне ледяной воды продукт отделяют фильтрованием, промывают в 50 см ацетонитрила. После высушивания получают первую порЦию 7,7 г окиси (1-окси-З-гидроксиизоиндолицил-2)-2-пиридина с т. пл. 203°С. Маточные растворы выпаривают досуха при пониженном давлении, остаток обрабатывают при 50°С в 50 см ацетонитрила. После охлаждеНИН в ванне с ледяной водою нерастворимый продукт отделяют фильтрованием, затем промывают в 20 см ацетонитрила. После высушивания получают вторую порцию 6,6 г окиси (1-окси-Д-гидроксиизоиндолинил-2()- 2-пиридина с т. пл. 203°С.
Пример 30. В суспензию 2,29 г гидрида натрия (покрытого на 50% минеральным маслом) в 25 см безводного диметилформамида добавляют раствор 9,8 г (пиридил-2)-2,3-гидроксиизоиндолинона-1 в 50 см безводного диметилформамида, поддерживая температуру около 20°С. Когда прекращается выделение газов, добавляют раствор 8,7 г 1-хлортиокарбонил-4-метилпиперазина в 10 см безводного
диметилформамида. Перемешивают еще в течение 2,5 час после окончания добавки, затем сливают реакционную смесь в 600 см воды. Продукт, который кристаллизуется, отделяют фильтрованием, промывают в 200 см
воды. После высушивания получают 15,6 i
21
продукта с т. пл. 177°С. Путем рекристаллизации в 240 см ацетонитрила и после промывки в 80 см окиси изопропила получают 12,15 т (пиридил-2)-2-(4-метилпиперазино)-3тиокарбонилоксиизоиндолинона-1 с т. пл. 182-183°С.
Предмет изобретения
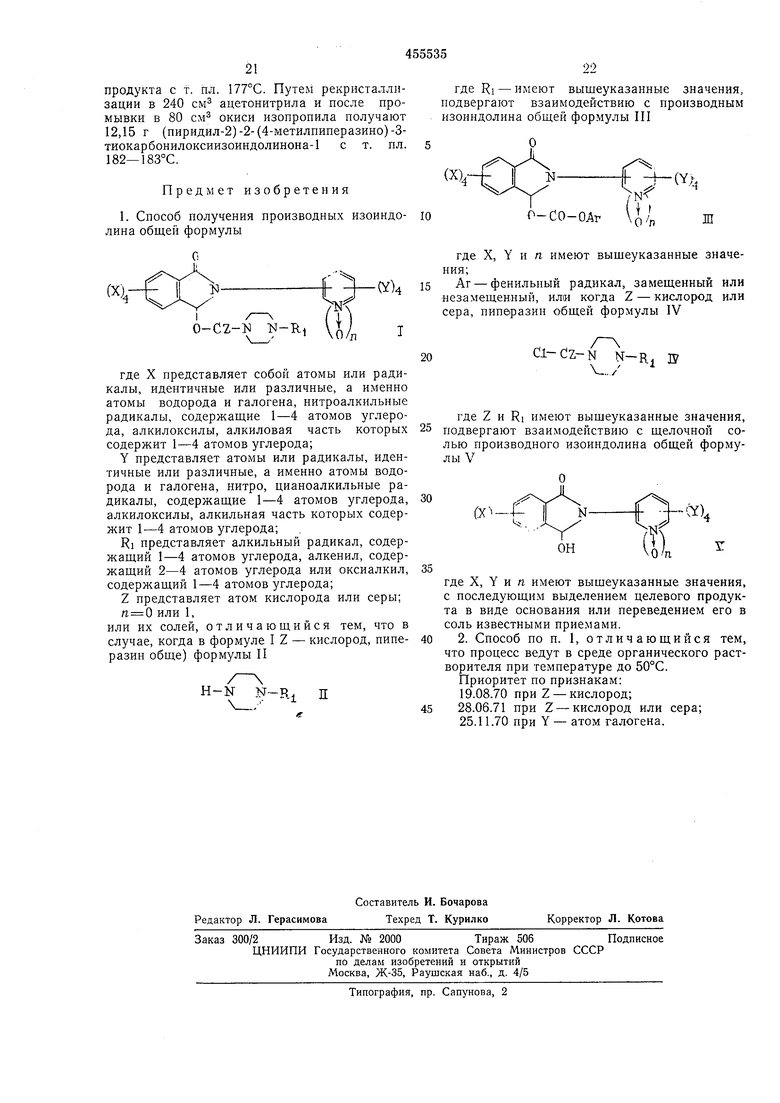
1. Способ получепия производпых изоиндолипа общей формулы 0-C2-1SI где X представляет собой атомы или радикалы, идептичные или различпые, а имеппо атомы водорода и галогена, питроалкильные радикалы, содержащие 1-4 атомов углерода, алкилоксилы, алкиловая часть которых содержит 1-4 атомов углерода; Y представляет атомы или радикалы, идентичные или различные, а именно атомы водорода и галогена, нитро, цианоалкильные радикалы, содержащие 1-4 атомов углерода, алкилоксилы, алкильная часть которых содержит -4 атомов углерода; RI представляет алкильный радикал, содержащий 1-4 атомов углерода, алкенил, содержащий 2-4 атомов углерода или оксиалкил, содержащий 1-4 атомов углерода; Z представляет атом кислорода или серы; tt 0 или 1, или их солей, отличающийся тем, что в случае, когда в формуле I Z - кислород, пиперазин обще) формулы П H-N N-Rj П
где RI - имеют выщеуказанные значения, подвергают взаимодействию с производным изоиндолина общей формулы П1
-СО-ОАг
10 где X, Y и п имеют вышеуказанные значения;Аг - фенильпый радикал, замещенный или незамещенный, или когда Z - кислород или сера, пиперазин общей формулы IV CI-CZ-N N-R. то V.,./ где Z и RI имеют выщеуказанные значения, подвергают взаимодействию с щелочной солью производного изоиндолина общей формулы V где X, Y и п имеют вышеуказанные значения, с последующим выделением целевого продукта в виде основания или переведением его в соль известными приемами. 2. Способ по п. 1, отличающийся тем, что процесс ведут в среде органического растворителя при температуре до 50°С. Приоритет по признакам: 19.08.70при Z - кислород; 28.06.71при Z -кислород или сера; 25.11.70 при Y - атом галогена.









| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных изоиндолина или их солей | 1974 |
|
SU505359A3 |
| Способ получения производных изоиндолина или их солей | 1975 |
|
SU568364A3 |
| Способ получения производных изоиндолина или их солей | 1973 |
|
SU488409A3 |
| Способ получения производных нафтиридина или их солей | 1974 |
|
SU583757A3 |
| Способ получения гетероциклических соединений | 1976 |
|
SU604496A3 |
| Способ получения производных изоиндолина или их солей | 1974 |
|
SU496730A3 |
| Способ получения производных изоиндолина или их солей | 1973 |
|
SU507233A3 |
| Способ получения гетероциклических соединений | 1975 |
|
SU673173A3 |
| Способ получения гетероциклических соединений | 1976 |
|
SU645582A3 |
| Способ получения производных пирроло/3,4-в/ пиразина | 1974 |
|
SU504484A3 |


Авторы
Даты
1974-12-30—Публикация
1971-08-19—Подача