(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИМИДАЗОЛА





1
Изобретение относится к способу иолучения ироизводных имидазола, обладающих физиологической активностью.
Осиованный на известной реакции взаимодействия дикетоиов с аминами предлагаемый сиособ нолучения производных имидазола оби1ей формулы
к.,-с о
I Я.-- С С
или «-оксикетон оби1,ей формулы
температуре кипения реакционной смеси в присутствии растворителя, например диметнлформанида, при атмосферном или повышенном давлении или в токе инертного газа.
В качестве аммониевой соли органической карбоновой кислоты можно применять ацетат и формиат аммония, а в качестве амида карбсповой кислоты - формамид. Аммониевую соль применяют обычно в большом избытке н в присутствии кислоты, нанрнмер низшей алканкарбоновой кислоты, такой, как муравьиная, уксусная или кислота обш,ей формулы R.iCOOH, где R4 - алифатический остаток, которая может одновременно служить растворителем.
Пример 1. 2-трег-Бутил-4(5)-(п-метокснфенил)-5(4)-(3-.г1иридил)-имидазол.
К смеси 56,6 г (0,375 моль) этилового эфира никотиновой кислоты и 75,6 г {0,39 моль) этилового эфира п-метокеифенилуксусной кислоты при 20-25°С в атмосфере азота прибавляют цорциями 3,6 г (0,585 МОЛь) метилата натрия, перемешивают 20 час при 60- 70°С, отдувая образуюш,ийся спирт слабым током азота, К твердой массе прикапывают 118 мл Концентрированной соляной кислоты, кипятят 3 час с обратным холодильником, охлаждают, промывают кислый раствор простым эфиром, к кислой водиой фазе добавляют разбавленный раствор аммиака и лед до рН 5, а затем раствор бикарбоната натрия до щелочной реакции. Суснензию экстрагируют этилацетатом, высушенную над сульфатом натрия органическую фазу выпаривают и поПример 2. 2-Г;Е7ег-Бутил-4(5)-(о-хлорфенил) -5(4) - (3-пиридил) -имидазол.
Смесь 25,0 г (0,126 моль) этилового эа)ира о-хлорфенилуксусной кислоты и 19,0 г (0,126 моль) этилового эфира никотиновой кислоты обрабатывают 10,2 г (0,196 моль) метилата натрия, как в примере 1, после перемещиваиия прибавляют по ка-плям 40 мл коицеитрироваиной соляной кислоты, кипятят 18 час с обратным холодильником, охлаждают и экстрагируют простым эфиром. К кислой водной фазе добавляют разбавленный раствор
лучают Г1-метоксибензил-(3-пиридил) - «етон, желтые кристаллы, т. нл. 86-87°С.
6,8 г (0,03 моль) /г-метоксибензил-(3--пиридил)-кетона, 3,32 г (0,03 моль) двуокиси селена и 80 мл ледяной уксусной кислоты кинятят 6 час с обратным холодильником, фильтруют в горячем состоянии, вьшаривают фильтрат в вакууме, растворяют остаток в этилацетате и фильтруют через колонку, наполненную 240 г силикагеля. Фильтрат выпаривают, церекристаллизовывают остаток из циклогексана и получают 1-(/г-метоксифенил)-2(З-пиридил)-глиоксаль, т. пл. 70-72°С. 10,0 г (0,0415 моль) 1-(/г-метоксифенил)-2(З-циридил)-глиоксаля, 3,58 г (0,0415 моль) пивалинового альдегида, 20 г ацетата аммония и 100 мл ледяной уксусной кислоты кипятят 22 час с обратным холодильником, при сильном неремешивании вводят смесь 350 г
льда и 250 мл концентрированного водного раствора аммиака, экстрагируют кристалличеекую маесу этилацетатом, промывают органическую фазу насыщенным раствором хлорида натрия до нейтрализации, высушивают над сульфатом натрия и выпаривают. Остаток нерекристаллизовывают из толуола, высушивают в высоком вакууме при 120°С и получают целевой продукт, белые кристаллы, т. пл. 202-204°С; выход 63%.
11спользуя 10 г соответствующего дикетона и различные количества альдегидов, аналогичным образом получают производные 2-Ri-4 (5) -R2-5 (4) -Нз - имидазола, перечисленные в табл. 1.
Таблица I
аммиака и лед до рП 5, а затем раствор бикарбоната натрия до щелочной реакции. Полученную суснензию экстрагируют этилацетатом, высушивают органическую фазу над сульфатом натрия, выпаривают и получают
о-хлорбензил-(3-пиридил)-кетон, желтые кристаллы, т. пл. 64-67°С.
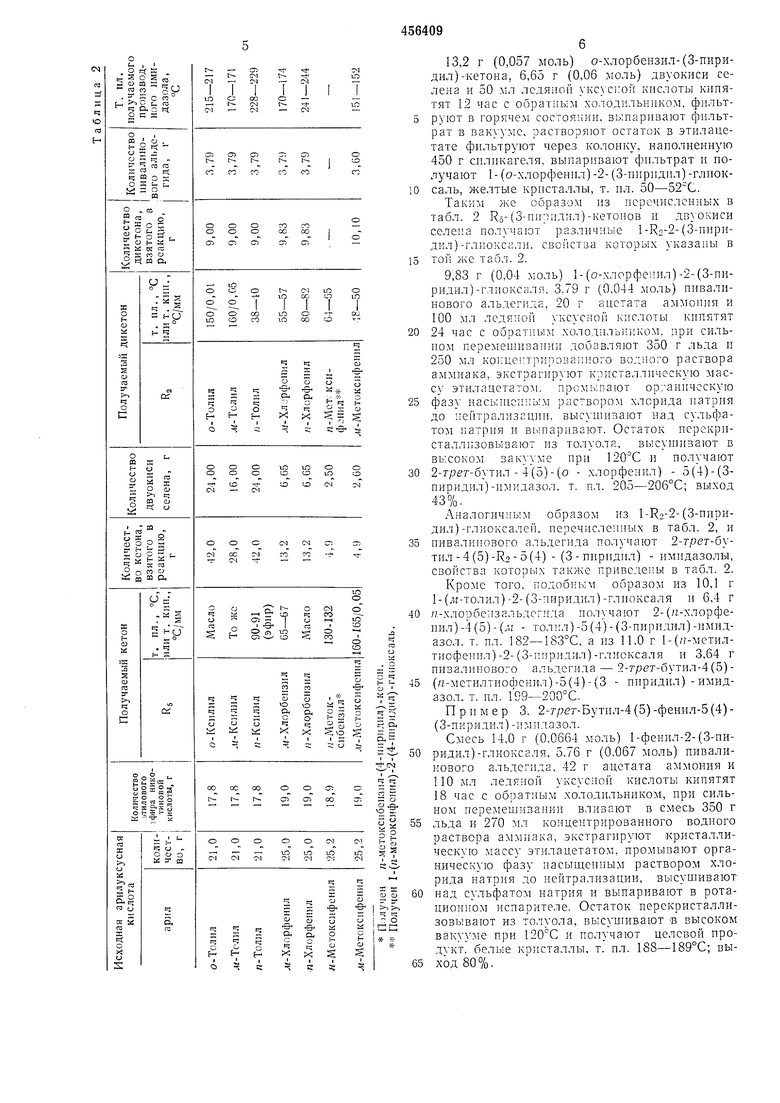
Аналогичным образом из этиловых эфиров арилуксусной и никотиновой кислот получают R5-(3-пиридил) -кетоны, перечисленные в табл. 2.
13,2 г (0,057 моль) о-хлорбензил-(3-пиридил)-кетона, 6,65 г (0,06 моль) двуокиси селена и 50 мл ледяной уксусной кислоты кипятят 12 час с обратным холодильником, фильтруют в горячем состоянии, выпаривают фильтрат в вакууме, растворяют остаток в этилацетате фильтруют через колонку, наиолнениую 450 г силикагеля, выпаривают фильтрат и получают 1- (о-хлорфеиил) -2- (3-пиридил) -глиоксаль, желтые кристаллы, т. пл. 50-52 С.
Таким же образом из перечисленных в табл. 2 К5-(3-пирпдил)-кетонов и двуокиси селена получают различные 1-R2-2-(3-пиридил)-глиоксали. свойства которых указаны в
той же табл. 2.
9,83 г (0,04 моль) 1-(о-хлорфенил)-2-(3-пиридил)-глиокеаля, 3.79 г (0.044 моль) пивалинового альдегида, 20 г аистата аммония и 100 мл ледяной уксусной кнслоты кипятят
24 час с обратным холодильником, при сильном перемеп1ивании добавляют 350 г льда и 250 мл ко1;центр1 рова1П ого водного раствора аммиака, экстрагируют кристаллическую массу этилацетатом. промывают органическую
фазу паеьпиенным рас вором хлорида натрия до нейтрализации, высушивают над сульфатом натрия и выпаривают. Остаток перскристаллнзовывают из толуола, высушивают в высоком вакууме при 120С и получают
2-г/ ет-бутил - 4(5)-(о - хлорфенил) - 5(4)-(3пиридил)-имидазол. т. нл. 205-206°С; выход 43%.
Аналогичным образом из 1-R2-2-(3-пиридил)-глиоксалей, перечисленных в табл. 2, и
иивалинового альдегида получают 2-трет-б тил-4(5)-R2 - 5(4) - (3-пиридил) - имидазолы,
свойства которых также приведе1;ы в табл. 2.
Кроме того, подобным образом из 10, г
1-(.и-толил)-2-(3-пиридил)-глиоксаля и 6,4 г
д-хлорбензальдегида нолучают 2-(/г--хлорфенил) -4 (5) - (м - толнл) -5 (4) - (3-пиридил) -имидазол. т. нл. 182-183°С, а из 11.0 г 1-(/г-метилтиофепнл)-2-(3-пиридил)-глиоксаля и 3,64 г пивалинового альдегида - 2-тре7--бутил-4(5)(/г-метилтиофенил)-5(4)-(3 - ииридил) - имидазол, т. ил. 199-200°С.
Пример 3. 2-7/; г-Бутил-4(5)-фенил-5(4)(З-ниридил)-импдазол. Смесь 14,0 г (0,0664 моль) 1-феиил-2-(3-ИИридил)-глиоксаля, 5,76 г (0,067 моль) пивалииового альдегида, 42 г ацетата аммония и 110 мл ледяной уксусной кислоты кипятят 18 чае с обратным холодильником, при сильном перемешивапии вливают в смесь 350 г
льда и 270 мл концентрированного водного раствора аммиака, экстрагируют кристаллическую массу этилацетатом, промывают органическую фазу насыш,еиным раствором хлорида натрия до нейтрализации, высушивают
над сульфатом натрия и выпаривают в ротационном испарителе. Остаток иерекристаллизовывают из толуола, высушивают в высоком вакууме ири 120°С и получают целевой продукт, белые кристаллы, т. ил. 188-189°С; выход 80 %. Для синтеза исходного вещества к 27,4 г (0,2 моль) метилового эфира никотиновой кислоты и 30 г (0,2 моль) метилового эфира фенилуксусной кислоты при 20-25°С в атмосфере азота прибавляют порциями 16,2 г (0,3 моль) метилата натрия, перемешивают 20 час при 60-70°С, отдувая образующийся спирт слабым током азота. К твердой массе прибавляют по а аплям 60 мл концентрированной соляной кислоты, кипятят 3 час с обратным холодильником, :к горячему еще желтому раствору прибавляют 30 мл воды, охлаждают до 50°С, добавляют 60 мл хлороформа, охлаждают до 5°С, отделяют белые кристаллы на нутче, промывают их хлороформом и получают гидрохлорид бензил-(З-пиридил)-кетона, т. пл. 225°С (этанол). К раствору 23,4 г (0,1 моль) гидрохлорида бензил-(З-пиридил)-кетона в 180 мл диметилсульфоксида прибавляют 20 мл 48%-ной бромистоводородной кислоты, иеремешивают 18 ча€ при 80-85°С, на смесь 800 г льда и 1000 мл воды, экстрагируют желтую Э мульсию 2X200 мл этилацетата, органические фазы объединяют, промывают водой и высушивают над сульфатом натрия. Красный раствор концентрируют в ротационном испарителе, остающееся масло перегоняют в трубке с щаровым расширением при 140- 150°С/0,1 мм и выделяют 1-фенил-2-(3-пиридил)-глиоксаль, т. лл. 56-57°С. Пример 4. 1-т/7ет-Бутил-4(5)-(я-метоксифенил) -5 (4) - (4-пиридил) -имидазол. 8,7 г (0,015 моль) 1-(л-метоКСифенил)-2-(4пиридил)-глиоксаля, 1,32 г (0,015 моль) пивалинового альдегида, 12 г ацетата аммония и 40 мл ледяной уксусной кислоты кипятят 13 час с обратным холодильником, при сильном перемешивании вливают в смесь 120 г льда и 100 мл Концентрированного водного раствора аммиака, обрабатывают кристаллическую массу, как в примере 3, и получают целевой продукт, белые кристаллы, т. пл. /258-260°С; выход 43%. Аналогичным образом из 3,2 г 1-фенил-2(4-пиридил)-1глиоксаля и 1,3 г пивалинового альдегида получают 2-г/7ег-|бутил-4(5)-фенил5(4)-(4-пиридил)-имидазол, т. пл. 266-268°С, а из 7,0 г 1-(«-метоксифенил)-2-(4-пиридил)глиоксаля и 4,2 г п-хлорбензальдегида - 2(п-хлорфенил)-4(5)-(я - метоксифенил)-5(4)(4-пиридил)-имидазол, т. пл. 286-288°С. ПрИ1мер 5. 2-грет-Бутил-4(5)-(«-метоксифенил) -5 (4) - (2-пиридил) -имидазол. К 30 г (0,142 моль) 2-(4-метоксистирил)пиридина в течение 30 мин при 200°С прибавляют 34,5 г (0,31 моль) двуокиси селена, выдерживают 30 мин при 200°С, охлаждают до 50°С, растворяют в 250 мл метиленхлорида, фильтруют через колонку, наполненную 1000 г силикагеля, упаривают фильтрат и получают 1-(л - метоксифенил)-2 - (2-пиридил)глиожсаль, желтые кристаллы, т. пл. 97-98°С. 7,2 г (0,03 моль) -(.ьметоксифенил)-2-(2:1иридил)-глиоксаля, 2,6 г (0,03 моль) пивалинового альдегида, 16 г ацетата аммония и 70 мл ледяной уксусной кислоты кипятят 18 час с обратным холодильником, при сильном перемешивании вливают IB смесь 220 г льда и 190 мл концентрированного раствора гпьмиака, экстрагируют кристаллическую массу этилацетатом, промывают органическую насыщенным раствором хлорида натрия до нейтрализации, высушивают над с льфатом натрия, выпаривают в ротационном испарителе, перекристаллизовывают остаток из цнклогексана, высушивают в высоком вакууме при 110°С и получают 2-грет-бутил-4(5)(л-метоксифенил) - 5(4)-(2 - пиридил)-имидазол, белые кристаллы, т. пл. 139-140°С; выход 55%. Аналогичным образом из 2,5 г вышеуказанного дикетона и 1,1 г беизальдегида получают 2-фенил-4(5)-(« - метоксифенил) - 5(4)-(2-пиридил)-имидазол, т. пл. 207-208°С; из 6,0 г вышеуказанного дикетона и 3,5 г /г-хлорбензальдегида - 2-(п - хлорфенил) - 4(5)-(я - метоксифенил)-5(4)-(2-ииридил)-и.мидазол, т. пл. 219-220°С; и из 12,0 г 1-фенил-2-(2-пиридил)глиоксаля и 4,9 г пивалинового альдегида - 2-т/ ег-бутил-4(5)-фенил - 5(4)-(2 - пиридил)имидазол, т. нл. 162-164°С. Пример 6. 2-т/7ег-Б}тил-4(5)(4)(3-пиридил)-имидазол. 38,4 г (0,18 моль) а-оксибензил-(З-пиридил)кетона растворяют при нагревании в 750 мл метанола, -при 30-35°С прибавляют 36,6 г (0,18 моль) моногидрата ацетата двухвалентной меди и 17,2 г (0,20 моль) пивалинового альдегида, за 10 мин прибавляют по каплям 375 мл концентрированного водного раствора аммиака, кипятят 3 час с обратным холодильником и фильтруют в горячем состоянии. Полученную медную соль промывают 2X50 мл горячего метанола, суспендируют в 1000 мл 80%-ного этанола, при 80°С насыщают суспензию сероводородом, перемешивают 3 чао при 80°С, фильтруют горячую суспензию на нутче для удаления сульфида меди, выпаривают фильтрат, перекристаллизовывают остаток из толуола, высушивают в высоком вакууме при 120°С и получают целевой продукт, т. пл. 188-189°С; выход 15%. Пример 7. 9,8 г (0,05 моль) бензил-(3пиридил)-кетона растворяют в 250 мл этанола и 88 мл 2 н. соляной кислоты, в течение 20 МИН при 20-25°С прибавляют раствор 7,0 г нитрита натрия в 100 мл воды, пергмешивают 15 час при 20-25°С, подщелачивают 2 н. раcTiBopoM бикарбоната натрия, прибавляют 1000 мл воды, фильтруют на нутче, перекристаллизовывают остаток из спирта и получают а-оксиминобензил-(3-пиридил)-кетон, т. пл. 169-172С. Таким же образом из 11,3 г (я-метоксибензил)-(3-пиридил)-кетона получают (а-оксими 1ю-л-метоксибензил)-(3-пиридил)-кетон, т. пл 183-186°С. Смесь 11,3 г (0,05 моль) а-оксиминобензил(З-пиридил)-кетона, 5,3 г (0,05 моль) пивалинового альдегида, 10 г ацетата аммония и 50 мл ледяной уксусной кислоты кипятят 3 час с обратныМ холодильником, наливают горячий раствор на лед, подщелачивают концентрированным водным раствором аммиака, кристаллическую массу экстрагируют этнлащетатом, промывают до нейтрализации, высушивают над сульфатом натрия, выпаривают органическую фазу, перекристаллизовывают остаток из этилацетата, высушивают в высоком вакууме при 150°С и получают 2-третбутил-4-фенил-5 - (3 - пиридил) - имидазол-3Окись, т. пл. 247-24в°С; выход 26%.
Аналогичным образом из 12,8 г (а-оксимино-п-метоксибензил) - (3 - пиридил) -кетона получают 2-т/5ег-бутил-4- (п-метоксифенил) -5- (3пиридил)-имидазол-3-окись, т. пл. 245-247°С.
К раствору 5,0 г 2-трег- бутил-4-фенил-5-(3пиридил)-имидазол-3-окиси в 30 мл хлороформа при охлаждении льдом прикапывают 6,5 мл треххлористого фосфора, перемешивают 2 час при 100°С, охлаждают, прибавляют 20 мл ВОДЫ, добавляют разбавленный раствор аммиака до рН 7,5, Экстрагируют смесь этилацетатом, промывают экстракт насьвденным раствором хлорида натрия, высушивают над сульфатом натрия, выпаривают в вакууме (М мм), высушивают в высоком вакууме при 120°С, кристаллизуют остаток из толуола и выделяют 2-т/зег-бутил-4(5) - фенил-5(4) - (3пиридил)-имидазол, т. пл. 188-189°С, выход 50%.
Аналогичным образом из 2-т/7ег-бутил-4{п-метоксифенил)-5-(3 - циридил) - имидазол3-окиси получают 2-третчбутил-4-(д-мето«сифеннл)-5-(3-пиридил)-имидазол, т. пл. 202- 204°С.
Пример 8. К смеси 31,2 г (0,19 моль) М-окиси этилового эфира никотиновой кислоты и 31 мл (0,195 моль) этилового эфира фенилуксусной кислоты в ат мосфере азота прибавляют 15,8 г (0,291 моль) метилата натрия, перемешивают I час при 20°С и 20 час при 60-70°С, отдувая образуюш.ийся спирт азотом. Смесь охлаждают до комнатной температуры, прибавляют 60 мл концентрированной соляной кислоты, кипятят 3 час с обратным холодильником, охлаждают до комнатной температуры, прибавляют 40 мл воды, темный раствор экстрагируют 2X50 мл хлороформа, добавляют разбавленный раствор аммиака и лед до рН 5, подщелачивают 2 н. раствором карбоната натрия, экстрагируют водный раствор этилацетатом, промывают экстракт насыщенным раствором хлорида натрия, высушивают над сульфатом натрия выпаривают при 40°С/11 мм и получают бензил- 3(пиридил-1-окись) -кетон, т. пл. 123-125°С.
Смесь 8,2 г (0,0385 моль) бензил- 3-(пиридил-1-окись)-кетона, 5,0 г двуокиси селена и 50 мл ледяной уксусной кислоты кипятят 6 час с обратным холодильником, фильтруют в горячем состоянии и прибавляют 500 мл воды. Смесь экстрагируют этилацетатом, промывают экстракт насыщенным раствором
.клорида натрия, высушивают над сульфатом натрия, выпаривают прп 40°С/11 мм и выделяют 1-фенил-2- 3-(пиридил-1-окись) -глиоксаль в виде масла.
Смесь 9,5 г (0.042 моль) 1-фенил-2- 3-(пиридил-1-окись) -глисксаля, 4.6 мл пивалинового альдегида, 20,0 г ацетата аммония и 150 мл ледяной уксусной кислоты кипятят 5 час с обратным холодильником, охлаждают
и вливают в смесь 300 г льда и 200 Мл концентрированного водного раствора аммиака. Смесь экстрагируют этиладетатом, промывают экстракт 1 асыщенным раствором хлорида натрия, высушивают над сульфатом натрия,
выпаривают в вакууме (11 мм) получают 2-г/7ет - бутил-4(5) - фенил-5(4)-3-(пиридил-1окись)-имидазол в виде масла, выход 15%.
Аналогично из 2-7рег-бутил-4(5)-фенил-5
(4) - (пиридил-1-окись) -имидазола получают 2-грег-бутил - 4 (5) -фенил-5 (4) - (3-пиридил)-имидазол, т. пл. 188-189°С.
Пример 9. К раствору 27,8 г (0,10моль) 2-трет-бутил - 4(5)-фенил - 5(4)-(3 - пиридил)имидазола в 900 мл ацетона при 20-25°С прибавляют 9,61 г (6,5 мл, 0,10 моль) метилсульфокислоты, перемешивают 15 час, отделяют белые кристаллы на нутче, перекристаллизовывают из смеси этанол - простой эфир и
получают метансульфонат 2-7 9ег-бутил-4(5)фенил-5(4)-(3 - пиридил) - имидазола, т. пл. 238-240°С; выход 66%.
Пример 10. К раствору амида натрия, полученному из 9,2 г (0,4 моль) натрия, 0,1 г
хлорида железа и 300 мл й идкого аммиака, в течение 20 мин при -40°С прикапывают 37,6 г (0,4 моль) 2-метилпиразина, красный раствор перемешивают 2 час при -40°С, при -40°С в течение 20 мин прибавляют раствор
27,2 г (0,2 моль) метилового эфира бензойной кислоты в 30 мл абсолютного простого эфира, перемешивают 1 час при -40°С, прибавляют порциями 25,0 г хлорида аммония и 250 мл абсолютного простого эфира, при -20°С выпаривают аммиак, через 2 час прибавляют 150 мл абсолютного простого эфира, перемешивают I час при комнатной температуре, кристаллизуют фенил-(пиразинил - 2-метил)кетон из простого эфира, перекристаллизовывают из этанола и получают фенил-(пиразинил-2-метил)-кетон, т. пл. 97-100°С.
Подобным образом из 27,6 г 2-метилпиразина и 34,2 г метилового эфира анисовой кислоты получают я-метокскфенил-(пиразинил-2метил)-кетон, т. пл. 77-85°С.
7,2 г фенил-(пиразинил - 2-метил) - кетона, 6,1 г двуокиси селена и 80 мл абсолютного диоксана кипятят 6 час с обратным холодильником, фильтруют на нутче, промывают осадок диоксаном и объединенные фильтраты выпаривают в вакууме (11 мм). Остающееся масло растворяют в 100 мл хлороформа, встряхивают с флоризилом, фильтруют, концентрируют фильтрат в вакууме (И мм), перегоняют остаток в трубке с шаровым расшиII
рением и собирают 1-фенил-2-(2-пиразинил)глиоксаль, т. кип. 170-180°С/0,05 мм.
Аналогичным образом из 10,0 г «-метоксифенил - (пиразинил-2-метил)-кетона получают 1-(/г - метоксифенил)-2-(2 - пиразинил)-глиоксаль, т. кип. 190-210°С/0,011 мм.
4,7 г .1-фенил-2-(2 - пиразинил)-глиоксаля, 2,9 мл пивалинового альдегида, 15,0 г ацетата аммония и 50 мл ледяной уксусной кислоты кипятят 2 час с обратным холодильником, при хорошем перемешивании вливают в смесь 170 г льда и 120 мл концентрированного водного раствора аммиака, кристаллическую массу экстрагируют этиладетатом, промывают экстракт насьщенным раствором хлорида натрия, высушивают над сульфатом натрия, выпаривают при 40°С/11 мм, кристаллизуют остаток из толуола и выделяют 2-грег-бутил4(5)-(2-пиразинил-5(4)-фенилимидазол, т. пл. 153-156°С; выход 33%.
Подобным образом из 6,5 г 1-(«-метоксифенил)-2-(2-пиразинил) - глиоксаля получают 2-трвг-бутил-4(5)-(2 - пиразинил)-5(4)-(«-метоксифенил)-имидазол, т. пл. 161 - 163°С.
Пример 11. К смеси 14,6 г этилового эфира никотиновой кислоты и 19,5 г этилового эфира я-метилтиофенилуксусной кислоты прибавляют порциями в токе азота 9,4 г метилата натрия, перемешивают 1 час при 20°С и 4 час при 65°С, прибавляют 40 мл концентрированной соляной кислоты, кипятят 7 час с обратным холодильником, охлаждают, прибавляют 40 мл воды н обрабатывают этилацетатом. Этилацетатный раствор экстрагируют 2 н. соляной кислотой, подш.елачивают экстракт карбонатом натрия, экстрагируют суспензию этилацетатом, промывают экстракт насыщенным раствором хлорида натрия, высушивают над сульфатом натрия, выпаривают в вакууме (11 мм) и кристаллизуют остаток из смеси этила1цетат - петролойпый эфир, получая (/г-метилтиобензил)-(3-пиридил)-кетон, т. пл. 125-127°С.
5,0 г (и-метилтиобензил) - (3-пиридил) -кетона, 10 мл 30%-ной перекиси водорода и 100 Мл ледяной уксусной кислоты перемешивают 10 час при комнатной температуре, выливают на 4000 мл льда, экстрагируют этилацетатом, промывают экстракт насыщенным раствором хлорида натрия, высушивают над сульфатом натрия и выпаривают при 40°С/11 мм. Остаток кристаллизуют из этанола и выделяют (л - метилсульфонилбензил) - (3-пиридил)-кетон, т. цл. 146-148°С.
27,0 г («-метилсульфонилбензил) - (3-пиридил)-кетона, 11,1 г двуокиси селена и 500 мл ледяной уксусной кислоты кипятят 8 час с обратным холодильником, фильтруют через Гифло, разбавляют фильтрат 3000 мл воды, добавляют аммиак до рН 6-7, экстрагируют этилацетатом, промывают экстракт насыщенным раствором хлорида натрия, Быс шивают над сульфатом натрия и концентрируют при 40°С/11 мм. Желтый кристаллический остаток кристаллизуют из толуола и получают
12
1-(п-метилсульфонилфенил) - 2-(3-пиридил)глиоксаль, т. пл. 160-170°С.
9,0 г 1-(/г-метилсульфонилфенил)-2-(3-пиридил)-глиоксаля, 3,5 мл пивалинового альдегида, 20,0 г ацетата аммония и 200 мл ледяной уксусной кислоты кипятят 5 час с обратным холодильником, вливают в смесь 300 мл льда и 200 мл концентрированного водного раствора аммиака, экстрагируют суспензию этилацетатом, промывают экстракт насыщенным раствором хлорида натрия, высушивают над сульфатом натрия, выпаривают в вакууме (11 мм), хроматографируют остаток на 200 г силикагеля, фракции 5 и б элюируют каждую
250 мл этилацетата и выделяют из них 2-третбутил-4(5)-(« - метилсульфонилфенил)-5(4)(З-пиридил)-имидазол, т. пл. 120-125°С (толуол) ; выход 45%.
Предмет изобретения
I. Способ получения цроизводных имидазо25 ла общей формулы
Н
I
N г-Ц ))-R,
К
RS
N
где RI - ИЗШИЙ алкил, циклоалкил или феНИЛ, который может быть замещен на галоид, низший алкил или низшую алкоксигруппу; один из остатков R2 и Кз - фенил, который может быть замещен на галоид, низший алкил, ОКСИ-, низшую алкокси- или алкилтиогруппу или низший алкилсульфонил, а другой - шсстичленный гетероароматический остаток, содержащий атома азота, их N-окисей или солей, отличающийся тем, что замещенный дикетон общей, формулы
( 3-C 0
или а-оксикетон общей формулы
I KS-CH-OH
где Ra и Rs имеют вышеуказанные значения, соответствующий монооксим или N-oKHCb обрабатывают аммиаком и альдегидом общей формулы RiCHO, где Ri-как указано выще, с последующим выделением целевого продук13та в свободном виде или переводом его в N-OKHCb или соль известными нриемами. 2. Способ по п. 1, отличающийся тем, что аммиак используют в виде аммониевой И соли органической карбоновой кислоты или амида карбоновой кислоты. Приоритет по пунктам: 11.05.71 по п. 2; 22.03.72 по п. 1.

Авторы
Даты
1975-01-05—Публикация
1972-05-10—Подача