(54) СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННОЙ ТИОМОЧЕВИНЫ
X,
C-CCH lt-Y-lCHslm-NH
у
Xi
где Xi, Xa, A У, / и m имеют указанные значения;
с изотиоцианатами общей формулы RiNCE где RI и Е имеют указанные значения.
Пример 1. Ы-Метил-Ы- 2-/ (4-нмидазолил) -метилтио/-этил -тиомочевина
Стадия 1. А. Раствор 67 г гидрохлорида 4(5)-оксиметилимидазола и 56,8 г гидрохлорида цистеамина в 1 л 40%-иой водной бромистоводородной кислоты нагревают в течение ночи при температуре кипения с обратным холодильником. После охлаждения раствор выпаривают досуха и остаточное твердое вещество промывают смесью этанола и диэтилового эфира для получения 156 г 4(5)- {(2аминоэтил) -тиометил -имидазола в форме гидробромида, плавящегося при 178-179°С.
13. 2 г фталимидоэтантиола прибавляют порциями при перемещивании к раствору этилата натрия (приготовленному из 0,23 г натрия) в 20 мл этанола при 0°С в атмосфере азота. После перемешивания при 0°С еще в течение 2,5 ч полученный желтый раствор охлаждают в бане из льда с солью и к нему по каплям прибавляют раствор 0,76 г гидрохлорида 4 (5)-хлорметилимидазола в 5 мл этанола в течение 10 мин. Кончив прибавлять, смесь перемешивают при комнатной температуре в течение ночи, затем подкисляют раствором хлористого водорода в этаноле и выпаривают досуха. При прибавлении воды осаждается 0,6 г непрореагировавшего фталимидоэтаптиола, который отделяют фильтрованием. Фильтрат концентрируют и подщелачивают водным раствором бикарбоната натрия для получения белого осадка, который после иерекристаллизации из водного этанола образует 0,75 г 4(5)- 2-(фталимидоэтил)-тиометил -имидазола, илавящегося при 136- 137°С. Перемешиваемую смесь 0,62 г фталимидопроизводного с 40 мл 48%-ной водной бромистоводородной кислоты выдерживают в течение ночи при температуре кипения с обратным холодильником. После охлаждения до 0°С полученный прозрачный раствор фильтруют и фильтрат выпаривают досуха. После перекристаллизации остатка из этанола получают 0,52 г дигидробромида 4(5)- 2- (2-амииоэтил) -тиометил -имидазола, плавящегося при 178-179С.
В. 118,8 г суспензии гидрохлорида цистеамина в 200 мл этанола высушивают над молекулярным ситом (прибавляют порциями при 0°С к раствору этилата натрия, приготовленному из 48 г натрия в 1 л этанола) в атмосфере азота. После перемешивания при ОС в течение дальнейших 2 ч прибавляют но каплям за период 45 мин ири температуре, поддерживаемой в интервале 1±2°С раствор 80 г
гидрохлорида 4(5) - хлорметилимидазола в 400 мл этанола. Кончив прибавлять, смесь перемешивают в течение ночи при комнатной температуре, фильтруют и фильтрат подкисляют концентрированной соляной кислотой. После этого раствор выпаривают досуха, остаток растворяют в 1 л этанола и прибавляют раствор избытка иикриновой кислоты в горячем этаноле. Полученный сырец-пикрат растворяют в 2,7 л воды и после декантации от нерастворимого масла раствору дают охладиться для образования дипикрата 4(5)- (2-аминоэтил) -тиометил -имидазола, плавящегося при 194-195°С. После обработки дипикрата водной бромистоводородной кислотой с последующей экстракцией толуолом получают дигидробромид, плавящийся при 178- 179°С после выпаривания досуха и перекристаллизации сырого остатка из этанола.
Стадия 2. Раствор 10 г дигидробромида 4(5)- |(2-аминоэтил) -тиометил -имидазола в 25 мл воды подщелачивают до рП 11, прибавляя раствор 8,7 г карбоната калия в 25 мл воды. Полученный раствор выпаривают досуха, экстрагируют изопропиловым спиртом и следы воды удаляют в форме азеотропной смеси с изопропиловым спиртом. Остаточный амии экстрагируют для отделения от неорганических материалов изонропиловым спиртом, экстракты концентрируют до объема около 70 мл и ирибавляют раствор 2,3 г метилизотиоциаиата в 5 мл изопропилового спирта. После этого реакционную смесь нагревают ири температуре кипения с обратным
холодильником в течение 1,5 ч и после охлаждения выпаривают досуха. Остаточное масло растворяют в ацетоне, раствор фильтруют для удаления следов неорганических материалов и фильтрат концентрируют для получения
4,1 г Ы-метил-Ы- 2-/(4-имидазолил)-метилтио/-этил -тиомочевиньт, нлавящейся при 96-
98°С. Проба этого материала после перекристаллизаци из ацетона имеет т. ил. 98-99°С.
Пайдено, %: С 41,8; П 6,4; N 24,4; S 27,6.
.
Вычислено, %; С 41,7; П 6,1; N 24,3; S 27,8. Пример 2. К-Метил-Ь - 2-/(5-метил-4-имидазолил) -метилтио/-этил - тиомочевина Стадия 1. А. Смесь 30,0 г гидрохлорида 4-оксиметил-5-метилимидазола и 23,0 г гидрохлорида цистеамина в 200 мл уксусной кислоты нагревают нри температуре кииения с обратиым холодильииком в течение 10 ч. После охлаждения до 15-20°С кристаллизующийся твердый продукт собирают и промывают изопропиловым спиртом для получения 45,5 г дигидрохлорида 4-метил-5- (2-аминоэтил)-тиометил -имидазола, плавящегося при 189- .
Б. Раствор 30,0 г гидрохлорида 4-оксиметил-5-метилимидазола и 23,0 г гидрохлорида цистеамина в 450 мл концентрированной водной соляной кислоты нагревают при температуре кинения с обратным холодильником в
течение 17 ч. После концентрирования и иовторного выпаривания с водой получают остаток, который растворяют в изопропиловом спирте, концентрируют до малого объема и охлаждают для получения 40,6 г дигидрохлорида 4-метил-5- (2-аминоэтил) -тиометил -имидазола, плавящегося при 185-19ГС.
В. Смесь 15,0 г гидрохлорида 4-оксиметил-5-метилимидазола и 11,5 г гидрохлорида цистеамина и 225 мл 48%-ного раствора бромистого водорода в уксусной кислоте нагревают при температуре кипения с обратным холодильником в течение 7 ч. После охлаждения получают 21,6 г дигидробромида 4-метил-5-(2-аминоэтил) -тиометил -имидазола, плавящегося при 208-21 ГС.
Стадия 2. 7,75 г карбоната калия прибавляют к раствору 14,6 г дигидрохлорида 4-метил-5- (2-амшюэтил) -тиометил -имидазола в 120 мл воды. Раствор выдерживают при комиатпой температуре в течение 15 мин и прибавляют 5,15 г мстилизотиоциапата. После пагревания при температуре кипепия с обратным холодильником в течение 30 мии раствор медленио охлаждают до 5°С.
Собирают 13,1 г продукта, перекристаллизовывают его из воды для получения N-метил-N- 2-/(5-метил-4-имидазолил) - метилтио/-этил -тиомочевипы, плавящейся при 150- 152°С.
Найдено %: С 44,5; Н 6,7; N 23,0; S 26,2.
C9Hi6N4S2.
Вычислено, %: С 44,2; П 6,6; N 22,9; S 26,2.
Примеры 3-27. Двухстадийными способами, сходными с описанными в примере 1, приготовлены тиомочевины формулы
Гет - -СНг-S-CHaCHsNH-C-NHCHs
S
в которой символ «Гет имеет значения, указанные в приведенной ниже табл. 1. В табл. 1
Гет-СН2-S-СНаСНгЫН-С-NHCHj
При-мер
Гет
CjHs
V-f
tJ30
Cf,H5H2C
HN.N
и 2 приведены также растворитель, из которого осуществляется перекристаллизация продукта, температура плавления продукта и данные элементарного анализа, а также температура плавления соответствующего полупродукта - соли амина формулы
Гет-СП2-S-CPbCHsNHa в которой AV представляет собой пикрат- или бромид-анионы, приведенные в той же таблице.
Исходные материалы, описываемые формулой Гет - CH2Q, в которой символ Q представляет собой гидроксильную группу, атом галоида или метоксильную группу, представляют собой все известные соединения, за исключением использованных в примерах 3 5, 14 и 26, нолучепие этих соединений описано после табл. 1 и 2. В каждом случае исходный материал вводят в реакцию с гидрохлоридом
цистеамина в водной бромнстоводородной кислоте, как это описано в примере 1, стадия 1. А. Там, где необходимо, полученный амин очищают, превращая в пикрат с последующей обработкой соляной или бромистоводороднон
кислотой и удалением пикриново кислоты, получают соответствующий гидрохлорид или гидробромид (как описано в нри.мере 1, стадия 1. В).
Гидрохлорид или гидробромид превращают в свободное основание, прибавляя карбопат калия с последующим концентрированием и экстракцией изопропанолом илн смесью диэтилового эфира и этанола (3:1); получают экстракт, который вводят в реакцию с метилизотиоцианатом в подходящем растворителе в условиях, сходных с описанными в примере 1, стадия 2. Полученные тиомочевины, в тех случаях, когда они способны к кристаллизации, перекристаллизовывают из раствор .теля, приведенного в табл. 1.
Таблица 1
S
Т. пл. проРастворительдукта, С
187-189
Водный этанол
Бромид
Изопропи л ацетатди этиловый
86-89
170эфир
131-133
Водный этанол
Бромид
Гет
Пример
Вг
HNv.V
сн.
H,c-.J
-N
т
10
H,C-N-jy
N
11
k/N
12 H,C-NTJ
c,i
13
kA
N
И
IS
m.
fl-
I .w
NH
16
Продолжение табл. 1
Т. пл. проРастворительдукта, °С
Бромид 180-
Лцетопитрил
152-153 182
Бромид 181 -
119-122
Вода 182
114-115
Мстилэтилкетон
Бромид 196- 198
76-78
Этм.-1ацетат - петролейный
195эфир
114-116
Пикрат 172Изоиропилацетат - этанол 174
105-107
Бромид
Изоироиилацетат
90-98
Вода
Бромид
97-99
Этанол - диэтиловый эфир
Бромид
154-155
Бромид 175Вода177
Бромид 153154
114-116
Изопронн л ацетат
Бромид 144147,5











17
S..T4
18
N
Изоиропилацетат - изопро78-80,5
197иапол
Бромид 191193
Гет
Пример
19
н,с
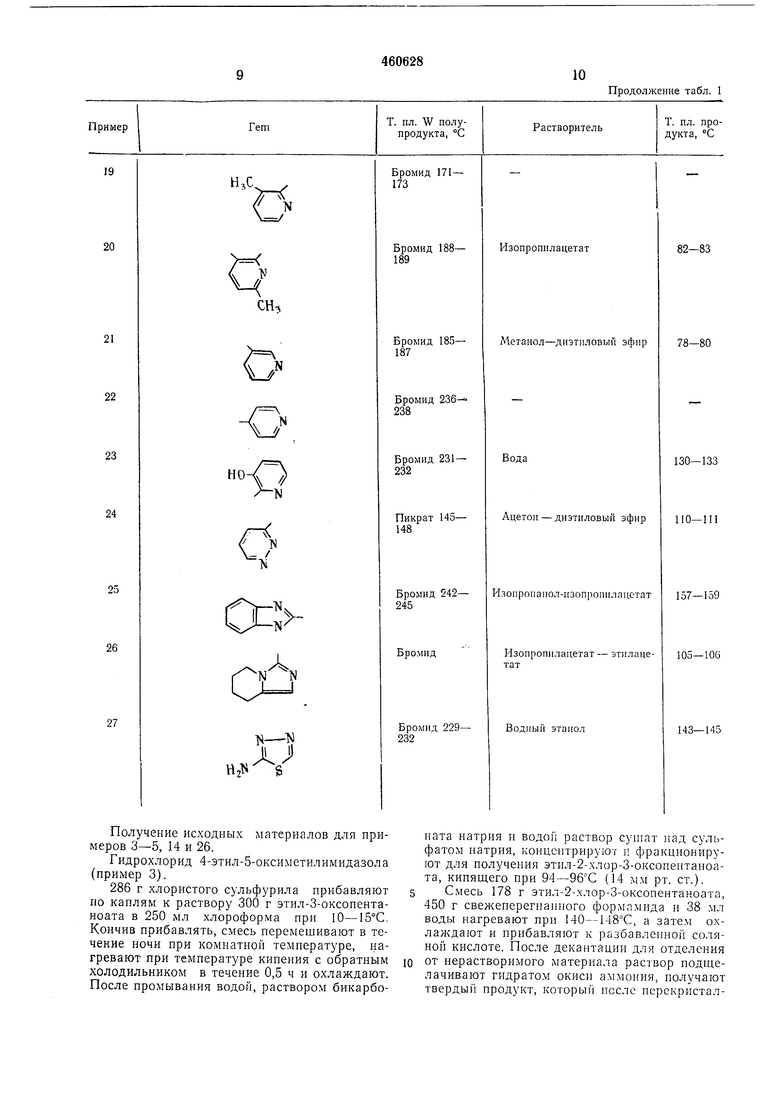
Продолжение табл. 1
Т. пл. проРастворительдукта, °С
Бромид 171 - 173
20
82-83
Изопропплацетат
Бромид 188189
21
22
N
//
23
о-О
-N
Метаиол-диэтлловыи эфир
Бромид 18578-80187
Бромид 236238
Вода
Бромид 231130-133232
24
Ацетон-диэтиловый эфир
Пикрат 145110-111148
25
.
26
27
-I
Получение исходных материалов для примеров 3-5, 14 и 26.
Гидрохлорид 4-этил-5-оксиметилимидазола (пример 3).
286 г хлористого сульфурила прибавляют по каплям к раствору 300 г этил-3-оксопентаноата в 250 мл хлороформа при 10-15°С. Кончив прибавлять, смесь перемешивают в течение ночи при комнатной температуре, нагревают при температуре кипения с обратным холодильником в течение 0,5 ч и охлаждают. После промывания водой, раствором бикарбоИзопропанол-изопропилацстат
Бромид 542-
157-159 245
Изопропилацетат - этилане
Бромид
105-10G тат
Бромид 229-
Водный этанол
143-145 232
ната натрия и водой раствор сушат ад сульфатом натрия, концентрируют фракционируют для получения этил-2-хлор-З-оксопентаноата, кипящего при 94-96°С (14 мм рт. ст.).
Смесь 178 г этил-2-хлор-З-оксопентаноата, 450 г свежеперегнанного формпмида и 38 мл воды нагревают при 140-148°С, а затем охлаждают и прибав.тяют к разбавленной соляной кислоте. После декантации для отделения от нерастворимого материала раствор подщелачивают гидратом окисп аммония, получают твердый продукт, который несло нерекристал11
N-Meтнл-N- 2- К-метилтио) -этил -тиомочевнна
лизации из водного этанола и смеси этанола и этилацетата образует 29 г 4-этил-5-карбэтоксиимидазола, плавящегося при 170-172°С. 14 г этого сложного эфира восстанавливают 4,6 г гидрида лития - алюминия в тетрагидрофуране и затем обрабатывают хлористым водородом для получения 10,6 г гидрохлорида 4-этил-5-оксиметилимидазола, плавящегося при 141 - 143°С (из изопроиилового спирта - диэтилового эфира).
Гидрохлорид-4-изопропил - 5 - оксиметилпмидазола (пример 4)
Раствор 43,8 г нитрата патрия в 92 мл воды прибавляют при иеремещивании к раствору 100,3 г этилизобутирилапетата в 80 мл уксусной кислоты прп 0°С. После перемешивания при 0°С в течение 30 мин, а затем при компатной температуре в течение 3 ч прибавляют 100 мл воды и смесь экстрагируют диэтиловым эфиром. Экстракты промывают водой, насыщенным раствором бикарбоната натрия
12
Таблица 2
и водой. После сущки над безводным сульфатом кальция раствор выпаривают для получения 112 г этил-2-оксимино-4-метил-3-оксопентаноата в форме масла-сырца.
Раствор 219 г этого оксиминокетона в 280 мл этанола прибавляют к суспензии предварительно восстановленного палладизированного древесного угля (10 г, 10%-ный) в 1 л этанола и насыщенному раствору хлористого водорода в этаноле (512 мл) и смесь гидрируют при комнатной температуре и давлении до поглощения теоретического количества водорода. Смесь фильтруют, фильтрат концентрируют и прибавляют этилацетат для получения 230,6 г гидрохлорида этил-2-амино-4-метил-З-оксопентаноата, плавящегося при 129-13ГС (с разложением). 50,5 г этого аминокетона растворяют в 180 мл повторно перегнанного формамида и раствор нагревают при 120°С в течеиие 2 ч, при 130°С в течение 1 ч при 140°С в течение 2 ч. После охлаждения смесь фильтруют и кристаллический продукт промывают водой для получения 22 г этил-4-изопропил-5-карбэтоксиимидазола, плавящегося при 177-178°С.
108 г этого сложного эфира помещают в аппарат Сокслета и восстанавливают 34,5 г гидрида лития-алюминия в тетрагидрофуране для получения 62,3 г 4-оксиметил-5-изопропилимидазола, плавящегося при 121 - 123°С.
Гидрохлорид 4-бензил-5-оксиметилимидазола (пример 5).
Проводят реакцию между 10,3 г этил-3-оксо-4-фенилбутирата и нитритом натрия с последующим восстановлением 10,8 г сырого этил-2-оксиамино-З-оксо - 4 - фенилбутирата, как это было описано для примера 4, для получения 8,5 г гидрохлорида этил-2-амино-З-оксо-4-фенилбутирата, нлавящегося при 150- 153°С. Температура плавления пробы, отобранной для анализа и перекристаллизованной из смеси этанола и этилацетата, 154- 155°С.
При реакции между 160 г этого аминокетона и 480 мл формамида, осуществляемой, как описано для примера 4, образуется 75 г 4-бензил-5-карбэтоксимидазола, плавящегося при 168,5-169,5°С. При восстановлении этого сложного эфира 6,4 г гидрида лития-алюминия в 600 мл тетрагидрофурана с последующим прибавлением воды, фильтрованием и подкислением фильтрата этанольным раствором хлористого водорода получают 22,9 г гидрохлорида 4-бензил-5-оксиметилимидазола, плавящегося при 149-15ГС после концентрирования и прабавления этилацетата.
4-Метил-З-оксиметил- 1,2,4 -триазол (пример 14)
57 г эпоксиацетилхлорида медленно прибавляют к перемешиваемому раствору 53,5 г 4-метилтиосемикарбазида в 500 мл безводного пиридина при О-5С. Смеси дают достигнуть комнатной температуры и перемещивают в течение 18 ч. После концентрирования при пониженном давлении остаток обрабатывают 21,4 г раствора натрия в 500 мл этанола и смесь нагревают при температуре кипения с обратным холодильником в течение 24 ч. После концентрирования и подкисления соляной кислотой получают твердое вещество. После частичного концентрирования твердое вещество собирают и перекристаллизовывают из этилацетата для получения 53 г 3-этоксиметил-4-метил-1,2,4-триазолин-5-тиона, плавящегося при 137-138°С.
44 г тиона десульфурируют, медленно прибавляя к раствору, приготовленному из 75 мл азотной кислоты, 150 мл воды и 1,5 г нитрита натрия при 15-20°С. После последующего подщелачивапия карбонатом натрия и концентрирования остаток экстрагируют смесью этанола и диэтилового эфира (1:1) и перегоняют для получения 30 г З-этоксиметил-4-метил-1,2,4-триазола, кипящего при 154-156°С (0,05 мм рт. ст.). 15 г указанного соединения растворяют в 150 мл 48%-ной водной бромистоводородной кислоты и нагревают при температуре кипения с обратным холодильником в течение 24 ч, концентрируют до получения сухого продукта и полученный продукт
непосредственно употребляют при реакции с гидрохлоридом цистеамина и бромистоводородной кислотой.
3-Оксиметил - 5,6,7,8 - тетрагидроимидазол-(1,5-а)-пиридин (пример 26)
Раствор 1,58 Al н-бутиллития в 49 мл н-гексана прибавляют в течение 0,5 ч к перемешиваемому раствору 8,9 г 5,6,7,8-тетрагидроимидазо-(1,5-а)-пиридина в безводном диэтиловом эфире при -60°С в атмосфере азота. Через 3 ч через раствор, приобретший красный цвет, пропускают газообразный формальдегид, образующийся при термической конденсации (разложении) параформа. Смеси дают нагреться до комнатной температуры в течение ночи, подкисляют соляной кислотой и экстрагируют хлороформом. Водный слой подщелачивают избытком насыщенного раствора карбоната натрия и экстрагируют хлороформом. После концентрирования и перекристаллизации остатка из смеси этанола, этилацетата и петролейного эфира получают 7,7 г 3-оксиметил-5,6,7,8-тетрагидроимидазо- (1,5-а) -пиридина, плавящегося при 188-189°С.
Примеры 28-30. Для получения соединений формулы используют двухстадийный
CH2S(CH2lmNHC-NHBi S
35
способ, описанный в примерах 3-27. В указанной формуле RI имеет значения, приведенные в табл. 3. В каждом случае полупродукт (амин) имеет формулу
(СН21;77Ш2-2НВг
В табл. 3 и 4 помещены величины т и Ri, растворитель, применяемый прп перекристаллизации, точка плавления и результаты элементарного анали а каждого продукта.
Пример 31. Дигидройодид Ы-.Метил-М- 2-/2- (4-имидазолил) -этил/-тиоэтил -тиомочевины
Стадия 1. Раствор 13,6 г гидрохлорида 4 (5)-(2-хлорэтил) -имидазола и 9,3 г гидрохлорида цистеамина в 100 мл дистиллированной воды прибавляют за 30 мин к перемещиваемому раствору 15,8 г 85%-ного гидрата окиси калия в 40 мл воды при комнатной температуре в атмосфере азота. Кончив прибавлять раствор, нагревают в течение 4 ч при 50°С. Периодически прибавляют по песколько капель растора гидрата окиси калия, чтобы величина рН реакционной смеси не опустилась ниже 11. После этого реакционную смесь подкисляют 2 п. раствором соляной кислоты.
15
N-K -N- K N-K V -(4-имидазолилмет11лтио)-К -тиомочевина
Найдено, %
выпаривают досуха при пониженном давлении и следы воды удаляют азеотроппой отгонкой с н-пропанолом. Остаток экстрагируют несколькими порциями изопропилового спирта и объединенные экстракты прибавляют к горячему раствору пикриновой кислоты в изопропиловом спирте. После охлаждения получают 42,3 г дипикрата 4(5)- 2- (2-амипоэтил)-тиоэтил -имидазола, плавящегося при 225-226°С.
Стадия 2. Указанный дипикрат превраш;ают в дигидрохлорид, прибавляя 200 мл концентрированиой соляной кислоты с последующей экстракцией толуолом (5 раз по 50 мл). Водный раствор выпаривают досуха, остаток растворяют в воде и раствор подщелачивают, прибавляя водный раствор карбоната калия.
Полученную смесь после этого выпаривают досуха и остаток экстрагируют н-пропанолом для получепия сырого основания 4(5)- 2- (2аминоэтил)-тиоэтил -имидазола после удаления н-пропанола. Раствор 3,3 г этого основания и 1,9 г метилизотиоцианата в 15 мл этанола нагревают при температуре кипения с обратным холодильником в течение 30 мин. После охлаждения раствор выпаривают досуха и остаток хроматографируют на силикагеле. После элюирования смесью этилацетата и метанола (3:2) и выпаривания соответствующих средних фракций получают маслянистый остаток, который подкисляют 64%-ной водной йодистоводородной кислотой. После проведения ряда декантаций при помощи диэтнлового эфира получают желтый осадок, который после промывания ацетонитрилом и затем диэтиловым эфиром образует дигидро460628
16
Таблица 3
-КПП
(4-имидазолилыетилтио) -тиомочевина
Т а б ли ц а 4
йодид Ы-метил-Ы- 2- (4-имидазолил) -этил)-тиоэтил -тиомочевины, плавящийся при 143- 145°С (не вполне белое вещество).
Найдено, %: С 21,6; Н 3,7; N 11,1; S 12,9; I 50,7.
C9HieN4S2 2НГ.
Вычислено, 7о: С 21,6; П 3,6; N 11,2; S 12,8; I 50,7.
Пример 32. N- 2- (4-Имидазолилметилтио) -этил- -тиомочевина.
Стадия 1. Раствор 6,0 г 4(5)- (2-аминоэтил) -тиометил -имидазола и 6,0 г бензоилизотиоцианата в 150 мл хлороформа нагревают при температуре кипения с обратным холодильником в течение 1 ч. После концентрирования и перекристаллизации из смеси этилацетата и изопропилацетата получают 7,5 г К-бензоил-Ы- 2- (4 - имидазолилметилтио)-этил - тиомочевины. Аналитически чистая проба (из водного изопропилового спирта)
имеет т. ил. 126-128°С.
Стадия 2. 6,0 г бензоилтиомочевины прибавляют к раствору 1,4 г карбоната калия в 80 мл воды при . Раствор выдерживают
при этой температуре в течение 1 ч, концентрируют для получения малого объема и подкисляют соляной кислотой. Бензойную кислоту отфильтровывают, фильтрат подщелачивают карбонатом калия и концентрируют при
пониженном давлении. После экстракции изопропиловым спиртом и концентрирования продукт кристаллизуют из изопропилацетата. Перекристаллизовывая из воды, получают 2,5 г N- 2- (4-имидазолилметилтио) -этил -тиомочевины, плавящейся при 135-137°С.
Найдено, %; С 38,9; Н 5,5; N 26,1; S 29,6.
C7H,2N4S2.
Вычислено, 7о: 38,9; Н 5,6; N 25,9; S 29,6.
Пример 33. N- 2-/(4-Метил-5-имидазолил)-метилтио/-этил -тиомочевина.
Стадия 1. При реакции 5,0 г 4-метил-5-(2-амипоэтил) -тиометил -имидазола и 23,8 г бензоилизотиоцианата, проводимой, как описано в примере 32, стадия 1, получают 24 г N-бензоил- N- 2- {4-метил-5-имидазолил)-ме.тилтиоэтил -тиомочевины, плавящейся при 138-140°С (из изонропилового спирта - этилацетата - диэтилового эфира). Аналитически чистая проба, полученная перекристаллизацией из водного изопропилового спирта, плавится при 165-166°С.
Стадия 2. 22 г сырой бензоилтиомочевины гидролизуют при помощи карбоната калия, как описало в примере 32, стадия 2, для получения 7,5 г N- 2- (4-метил-5-имидазолил)-метилтиоэтил - тиомочевины. Затем перекристаллизовывают из воды, потом из смеси изопропилового спирта и диэтилового эфира, получают 3,8 г чистого продукта, плавящегося при ПО-112°С.
Пайдено, %: С 41,9; П 6,3; N 24,5; S 28,0.
C8Hi4N4S2.
Вычислено, %: С 41,7; Н 6,1; N 24,3; S 27,8.
Пример 34. 4,5-бис- 4- (N-Метилтиоуреидо) -этилтиометил -имидазол
Стадия 1. При реакции 1,6 г гидрохлорида 4,5-диоксиметилимидазола и 2,2 г гидрохлорида цистеамина, проводимой, как описано в примере 1, стадия 1. А, получают 3,8 г тригидробромида 4,5-бис- (2-аминоэтил) -тиометил -имидазола), плавящегося при 233-236°С.
Стадия 2. При реакции 1,2 г 4,5-бис- {(2-аминоэтил) -тиометил -имидазола и 1,5 г метилизотиоцианата, проведенной как описано в примере 1, стадия 2, получают 1,1 г 4,5-бис- 2- (N-метилтиоуреидо) -этилтиометил -имидазола, плавящегося при 154-155°С (из изоиропилового спирта - изопропилацетата).
Найдено, %: С 39,8; И 6,2; N 21,5; S 32,5.
Сз1Н24Нб54.
Вычислено, %: С 39,8; II 6,2; N 21,4; S 32,7.
Пример 35. 3,5-бис- 2- (N-Метилтиоуреидо) -этилтиометил -1,2,4-триазол
Стадия 1. Реакцию между 9,0 г 3,5-диоксиметил-1,2,4-триазола (полученного из 1,2,4-триазола и избытка формальдегида при повыщенных температурах) и 17,3 г гидрохлорида цистеамина проводят, как описано в примере 1, стадия 1. А, и получают 4,7 г тригидробромида 3,5-бис- (2-аминоэтил) -тиометил -1,2,4- триазола, плавящегося при 214-215°С
Стадия 2. Проводя реакцию 3,5-бис- (2-аминоэтил)-тиометил -1,2,4-триазола (полученного из 6,5 г тригидробромида) с 1,93 г метилизотиоцианата, получают бистиомочевину, которую очищают, пропуская через колонку силикагеля и используя этанол в качестве элюента. После растирания с изопронилацетатом и нерекристаллизации из смеси этанола и диэтилового эфира получают 0,9 г 3,5-бис- 2- (N-метилтиоуреидо) - этилтиометил - 1,2,4-триазола, плавящегося при 133-135°С. Пайдено, %: С 35,7; Н 5,9; N 24,6.
Ci2H23N7S4-0,5H2O.
Вычислено, %: С 35,8; П 6,1; N 24,3.
Пример 36. N-Meтил-N- 3- (2-имидазолилтио) -нронил -тиомочевина
Стадия 1. Раствор 2 г 2-меркаптоимидазола и 1,14 мл 3-аминопропанола в 25 мл 487о-ной бромистоводородной кислоты нагревают при температуре кипения с обратным холодильником в течение 25 ч. Реакционную смесь выпаривают досуха и маслянистое остаточное твердое вещество дважды перекристаллизовывают из смеси этанола и диэтилового эфира для получения 3,55 г дигидробромида 2- (3-аминопропилмеркапто) -имидазола, плавящегося при 160-162°С.
Стадия 2. 7 г этого дигидробромида амина
переводят в свободное основание и вводят в реакцию с 1,75 г метилизотиоцианата способом, описанным в примере I, стадия 2, для получения сырого желтого твердого продукта после выпаривания реакционной смеси. Этот
продукт-сырец промывают смесью ацетона и изопропилацетата (1:1) и перекрнсталлизовывают из воды для получения 3,46 г N-метил-N- 3- (2-имидазолилтио) - пропил -тиомочевины, плавящейся при 139-14ГС.
Найдено, %: С 41,5; Н 6,1; N 24,1; S 27,7.
C8Hi4N4S2.
Вычислено, %: С 41,7; Н 6,1; N 24,9; S 27,8. Примеры 37-40. Двухстадийный способ, описанный в примере 36, используют для получения соединений тиомочевины формулы Гет-S-СП2СН2СН2-NHC-NHCHs
Ч
S в которой Гет имеет значения, ириведенные в
помещенной ниже табл. 5. Растворитель, из которого проводили кристаллизацию продукта, точка плавления продукта и результаты его элементарного анализа приведены в табл. 5 и 6 вместе с точкой плавления соответствующих полупродуктов - солей аминов формулы
Гет-S-CH2CH2CH2NH2 2НВг
19
S-CHaCHsCHj-NHC-NHCHs
К-Метил-К- () -пропил -тиомочевцна
Пример 41. М-Метил-Ы- 3- (2-оксазолил)-тиопропил -тиомочевина
Стадия 1. 90 мл соляной кислоты прибавляют к раствору тиоцианата калия в этаноле (1,8 л) при перемешивании. Отфильтровывают от неорганического материала, прибавляют 35,9 г гликолевого альдегида и полученный раствор нагревают при температуре кипения с обратным холодильником в течение 24 ч.
Концентрируют раствор, затем охлаждают. Образуется белый твердый продукт, который после перекристаллизации из этанола дает 30 г оксазол-2-тиола, плавящегося ири 143- 144°С.
Стадия 2. 13,4 г 3-бромпропилфталимида прибавляют к перемешиваемому раствору этилата натрия (полученному из 1,15 г натрия) и 5,1 г оксазол-2-тиола в 100 мл этанола. Полученный раствор нагревают при температуре кипения с обратиым холодильником в течение 2,5 ч и концентрируют ири понижен20
Таблица о
Ч
s
Таблица 6
ном давлении. Остаток растирают со 100 мл воды для получения 14 г 2- (3-фталимидопропилтио) -оксазола, плавящегося при 101°С. После перекристаллизации из этанола получают чистый оксазол, плавящийся при 102- .
Стадия 3. 5,3 г гидразингидрата осторожно прибавляют к раствору 10 г 2- (3-фталимидопроиилтио) -оксазола в 179 мл этанола при
перемешивании. Раствор после этого нагревают при температуре кипения с обратны.м холодильником в течение 25 мин. Охлаждают и отфильтровывают от фталгидразида, затем фильтрат концентрируют ири пониженном
давлении и остаток повторно выпаривают при добавлении этанола для получения сырого 2 - (3-аминопроиилтио) - оксазола, который дважды промывают диэтиловым эфиром и растворяют в 60 мл этанола. Прибавляют 2,54 г
метилизотиоцианата и раствор нагревают при температуре кипения с обратным холодильником в течение 30 мин. Охлаждают, фильт21
роваиием удаляют нерастворимый материал, фильтрат концентрируют до образования масла, которое хроматографируют на колонке силикагеля, используя в качестве элюента этилацетат. Образовавшийся нродукт кристаллизуют из смеси этанола, диэтилового эфира и н-гексана для нолучения 2,4 г N-метил-N 3- (2-оксазолил) -тиопропил -тиомочевины, плавящейся при 43-45°С.
Найдено, %: С 41,7; Н 5,9; N 18,3; S 27,5.
CsHisNaSs.
Вычислено, %: С 41,5; Н 5,7; N 18,2; S 27,7.
Пример 42. К-Метил-1 - 3- (4-метил-2-оксазолил) -тиопропил -тиомочевина
Стадия 1. Реакцию между 5,8 г 4-метилоксазол-2-тиола и 13,4 г 3-бромнропилфталимида проводят в условиях, описанных в примере 41, и получают 14 г 4-метил-2- (3-фталимидопропилтио)-оксазола, плавящегося при 92-93°С (этанол - диэтиловый эфир).
Стадия 2. При обработке 3,0 г фталнмидного соединения 1,53 г гидразина с последующим взаимодействием неносредственно с 0,73 г метилизотиоцианата в условиях, описанных в нримере 41, получают 1,0 г N-метил-N- 3- (4-метил-2-оксазолил) - тиопропил -тиомочевипы, плавящейся при 73-74°С (из этанола - диэтилового эфира - н-гексана).
Найдено, %: С 44,0; Н 6,2; N 17,1; S 25,9.
CgHisNsSa.
Вычислено, %: С 44,1; Н 6,2; N 17,1; 526,1.
Пример 43. К-Метил-Ы- 2- (4-имидазолилметокси) -этил -тиомочевина
Стадия 1. Перемешиваемую суспензию 14,7 г 4- (2-хлорэтоксиметил) -имидазола в форме гидрохлорида и 9,8 г азида натрия в 103 мл безводного днметилформамида выдерживают при 95°С 5 ч, азид осаждается при выдержке в течение ночи при комнатной темнературе. Разбавляют водой, фильтруют, фильтрат концентрируют и остаток очищают методом хроматографии на безводной колонке окиси алюминия, применяя этанол. Продукт выщелачивают 6,5 г карбоната калия в 3 мл воды и безводный остаток экстрагируют изопропиловым спиртом (три раза по 50 мл). При концентрировании экстракта получают 7,2 г 4- (2-азидоэтоксиметил)-имидазола. При гидрирова 1ии 7,2 г азидного соединения в среде 142 мл изопронилового спирта на катализаторе - 3,0 г окиси платины - получают 6,48 г 4- (2-амнноэтоксиметил) -имидазола. Проба монопикрата моногидрохлорида плавится при 139-140 С (из нитрометана).
Найдено, %: С 35,4; Н 3,8; N 20,6; С1 8,8.
С,2Н,5Нб08 НС1.
Вычислено, %: С 35,4; Н 3,7; N 20,7; С1 8,7.
Стадия 2. 2,24 г 4- (2-аминоэтоксиметил)-имидазола вводят в реакцию с 1,21 г метилизотиоцианата в 25 мл изопропилового спирта обычным способом. Сырой продукт очищают методом хроматографии на бумаге на колонке силикагеля, используя в качестве элюента этилацетат, а затем на колонке безводной окиси алюминия, используя в качестве элю460628
22
ента хлороформ. Конечный продукт перекристаллизовывают из этилацетата для получения 0,80 г М-метил-Ы- 2- (4-имидазолилме токси) -этил -тиомочевины, плавящейся прм
gg98°С
Найдено, %: С 44,6; Н 6,5; N 26,0; S 14,7.
C8Hi4N4OS.
Вычислено, %: С 44,8; Н 6,6; N 26,2; S 15,0.
Пример 44. Ы-Метил-М- 3- (2-пиридиламино) -пропил -тиомочевина
Раствор 2,74 г 2-(3-аминоиропиламино)-пиридина и 1,46 г метилизотиоцианата в 50 мл изопропилового спирта перемешивают при комнатной температуре в течение 16 ч. Концентрируют, затем растирают остаток с метилэтилкетоном, получают сырой продукт, который перекристаллизовывают из водного этанола, образуется 2,45 г М-метил-М- 3- (2-пиридиламино) -пропил -тиомочевины, плавящейся при 134-135°С.
Найдено, %: С 53,4; Н 7,2; N 25,0; S 14,3.
CioHieN S.
Вычислено, %: С 53,5; Н 7,2; N 25,0; S 14,3.
Пример 45. N-Метил- N- 2-/(4-метил-5-имидазолил -метилтио/-этил -тиомочевина
Смесь 5,1 г 4-метил-5- (2-аминоэтил) -тиометил -имидазола и 2,0 г метилизоцианата в ацетоиитриле нагревают при 100°С в автоклаве в течение 18 ч. После охлаждения полученный твердый продукт собирают и перекристаллизовывают из смеси изопропилового спирта и ацетонитрила для получения 4,0 г 1 -метил-К- .2-/(4-метил-5-имидазолил)-метилтио/-этил -тиомочевипы, плавяп1ейся при 158-159°С.
Найдено, %: С 47,5; Н 7,1; N 21,5; S 14,1.
CgHieNiOS.
Вычислено, %: С 47,3; Н 7,1; N 24,5; S 14,0.
Пример 46. Ы-Метил-К- /2- (5-тиазолил) -метилтиоДэтил -тиомочевнна
Стадия 1. Реакцию между 2,01 г 5-оксиметилтиазола и 1,99 г гидрохлорида цистеамина в водной бромистоводородпой кислоте проводят аналогично описанному в примере 1, стадия 1, для получения 4,85 г 5- (2-аминоэтил) -тиометил -тиазола в форме дигидробромида, плавящегося при 191 - 194°С (из метанола).
Стадия 2. При реакции между 2,2 г 5- (2-аминоэтил) -тиометил -тиазола и 0,94 г метилизотиоцианата в сред 10 мл этанола получают тиомочевииу, которую очищают методом хроматографии на колонке силикагеля, используя в качестве элюента этилацетат. После перекристаллизации из смеси изопропилацетата, метилэтилкетоиа и диэтилового эфира получают 2,1 г N-MeTPM-N- /2- (5-тиазолил)-метилтио/-этил -тиомочевины, плавяп ейся при 86-88°С.
Найдено, %: С 38,6; П 5,4; N 16,19; S 38,6. CeHisNsSa.
Вычислено, %: С 38,8; Н 5,3; N 17,0; S 38,9. Пример 47. М-Метил-К - /2- (2-пиридил) -метилтио/-этил -мочевина
При взаимодействии 7,0 г 2- (2-аминоэтил) -тиометил -пиридина и 2,7 г метилизоцианата, проведенном, как описано в примере 45, получают N-мeтил-N- /2- (2-пиридил)-метилтио/-этпл -мочевину, плавящуюся при 63-66°С (из ацетонитрила-диэтилового эфира).
Пример 48. N- /2- (4-метил-5-имидазолил) -метилтио/-этил -мочевина
Раствор 3,33 г дигидробромида 4-метил-5-(2-аминоэтил)-тиометил -имидазола, 0,811 г цианата калия и 0,69 г карбоната калия в 30 мл воды нагревают при 80-90°С в течение 3 ч. Концентрируют при пониженном давлении и экстрагируют остаток к-пропанолом, получают сырой продукт, который хроматографируют на колонке с силикагелем, используя смесь этилацетата и этанола (5:1) в качестве элюента. Перекристаллизацией из смеси эфира и изоиропилового спирта и затем из ацетонитрила получают 0,8 г N- /2- (4-метил-5-имидазолил) - метилтио/-этил - мочевины, т. пл. 148-ИЭ-С.
Пайдено, %: С 44,6; Н 6,5; N 25,7; S 15,0.
CsHuNiO.
Вычислено, %: С 44,8; Н 6,6; N 26,1; S 15,0.
Предмет изобретения
Способ получения замещенной тиомочевины общей фор.мулы
(CH,v-Y-leHA,NH-c4
где А имеет такое значение, что образует вместе с атомом углерода ненасыщенное гетероциклическое ядро, которое включает, по меньщей мере, один атом азота и может содержать кроме того другие гетероатомы, такие как атом серы и кислорода;
Xi и Х2 (одинаковые или разные) - водород, низший алкил, трифторметил, гидроксил, бензил, галоид, аминогруппа, группа
(CH2)i-Y-(ab,i,-Mi-cf
NHEi
или Xi и Xz могут образовывать вместе, по меиьшей мере, с двумя атомами, входящими в А, следующее кольцо, например бензольное, пиридиновое или частично ненасыщенное кольцо;
/ и m - от О до 4, причем сумма их не должна превыщать 3 или 4;
У - атом серы, кислорода или группа NH;
Е - атом кислорода или серы;
RI - водород, низщий алкил, ацил или диалкиламиноалкил, отличающийся тем, что амин общей формулы
X,
C-CCHglt-Y-lCHs fn-NH, ,-Xi
где Хь Х2, А, У, / и т имеют указаиные значения,
подвергают взаимодействию с изотиоцианатами общей формулы RiNCE где RI и Е имеют указанные значения,
с последующим выделением целевого продукта известными приемами.
Приоритет по признакам;
,Е
(CH2U-W-cf ШВ,
или Х и Х2 могут образовывать вместе, по меньшей мере, с двумя атомами, входящими в А, следующее кольцо; Ri - диалкиламиноалкил.

Авторы
Даты
1975-02-15—Публикация
1972-02-25—Подача