трифеиилфосфин. метил пиперидин, диметилапилнн; азометипы, например гидробензамид, бензилидендиапилип; четвертичные соли аммония, нанример тeтpa eГ Iлa :л1oннйбpoмид (.хлорид); фосфоииевые соли, нанример тетраэтилфосфонийхлорид, азотсодержащие гетероциклы, например пиридин, хииолин, изохинолии и их алкильиые производные; амиды кислот, например диметилформа.мид, диметилбензамид; окиси фосфи 1ов и амииов, например ниридиноксид, триметилфосфиноксид; амиды кислот фосфора, например диэтиламид этилфосфоновой кислоты, гексаметилтриамид фосфорной кислоты. Катализаторы нримеыяют в количестве 0,01-5 вес. %, предпочтительно 0,05-2 вес. %.
Процесс желательно проводить в среде инертного органического растворителя, например трихлорэтана, толуола, хлорбензола, предпочтительным раствори ге-ле,м является целевой продукт.
Реакцию можно проводить прн повышенном давлении, ио лучше при атмосферном.
Данный способ особенно пригоден для нолучения дихлорангидрида 2-хлорэтилфосфоновой кислоты из сырого бис-2-хлорэтилового эфира 2-хлорэтилфосфоиовой кислоты, получаемого реакцией треххлористого фосфора с окисью этилена с последующей термической перегруппировкой трис-(2-хлорэтил)-фосфита.
Все три стадии этого процесса могут быть проведены в одном реакторе без выделения промежуточных соединений; выход целевого продукта превышает 70% (в зависимости от катализатора). Наряду с целевым продуктом при этом образуется дихлорангидрид винилфосфоновой кислоты, выделяемый дистилляцией. Целевые продукты по предлагаемому способу образуются с выходом до 99% и выделяются известными приемами.
Пример 1. Дихлорапгидрмд этилфосфоновой кислоты из дпметилового эфира этилфосфоновой кислоты.
В цилиндрический сосуд диаихетром 4 см и длиной 25 см помещают 125 г диметилового эфира этилфосфоновой кислоты и 0,5 г трифенилфосфина. Через впаянную в нижпюю часть реактора пористую пластинку из спеченного стеклянного порошка медленно пропускают фосген при интенсивном перемеитивании и температуре .
Через 6 час пропускание фосгена прекращают и избыток фосгена выдувают азотом при комнатной температуре. Продукг реакции отгоняют при уменьшенном данлепип. Получают 125 г чистого (по данным газохром атографичес кого исс.тед.ованпя) дихлорангидрида этилфосфоповой кислоты (т. кип. 7ГС при 15 мм рт. ст.). Это соответствует выходу 96% от теоретического.
Пример 2. Дихлорапгидрид этплфосфоновой кислоты из метилового э({)ира этилпирофосфоновой кислоты.
Как описано в примере 1, в 56 г диметилового эфира этилпирофосфоновой кислоты пропускают в присутствии 0,5 г трифенилфосфина при 100-120°С в течение 6 час фосген.
Раствор, полученный после реакции, продувают азотом при комнатной температуре для удаления избыточного количества фосгена и затем перегоняют при уменьшенном давлении. При остаточном давлении 9 мм рт. ст.
и температуре 58°С отгопяется 67 г дихлорангидрида этилфосфоновой кислоты. Это соответствует выходу 94% от теоретического. Пример 3. Дихлорангидрид этилфосфоповой кислоты из ангидрида этилфосфоновой
кислоты.
В раствор 71 г ангидрида этилфосфоновой кислоты и 0,7 г пиридина в 71 j- дихлорапгидрида этилфосфоново кислоты пропускают, как указано в примере 1, фосген при 100 -
120°С в течение 4 час. После продувания реакционного раствора азотом с последующей перегонкой при уменьшенном давлении получают 183 г дихлорсшгцдрнда этилфосфоиовой кислоты (т. кип. 58°С при 9 мм рт. ст.). За
вычетом 71 г днхлорангидрида этилфосфоновой кислоты, примененного в качестве растворителя, получают выход, равный 112 г. Это соответствует выходу 99% от теоретического. П р и м еры 4-46. Проводя опыты, как
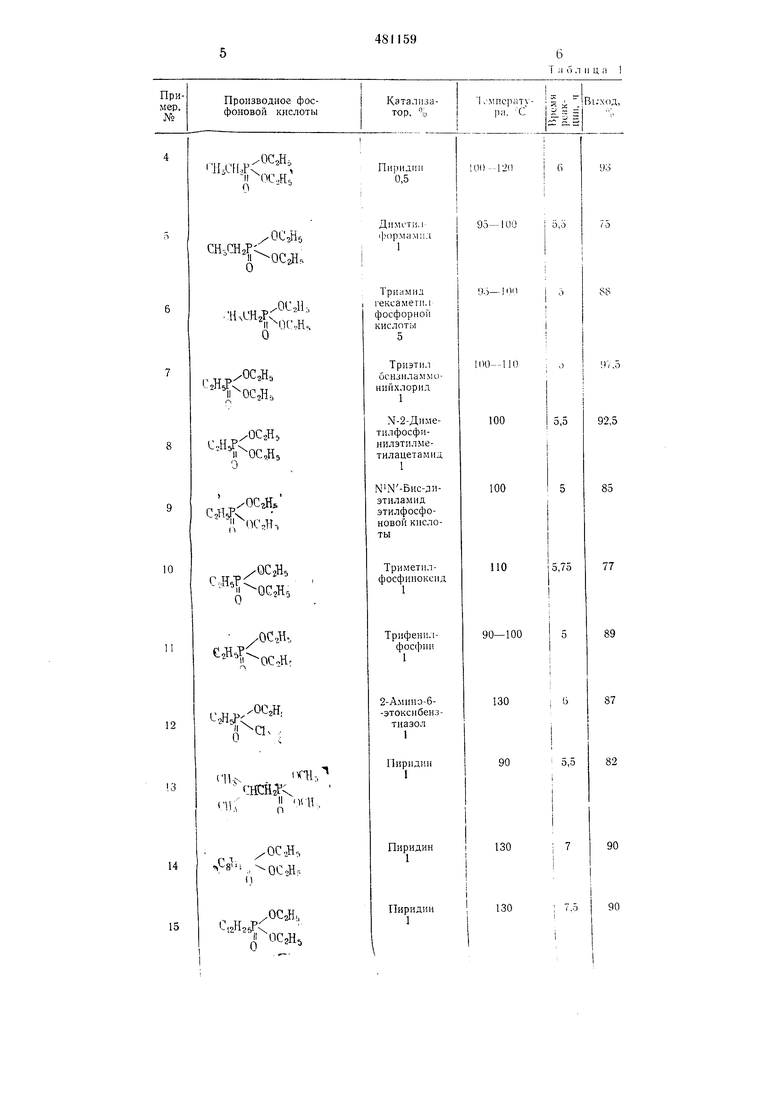
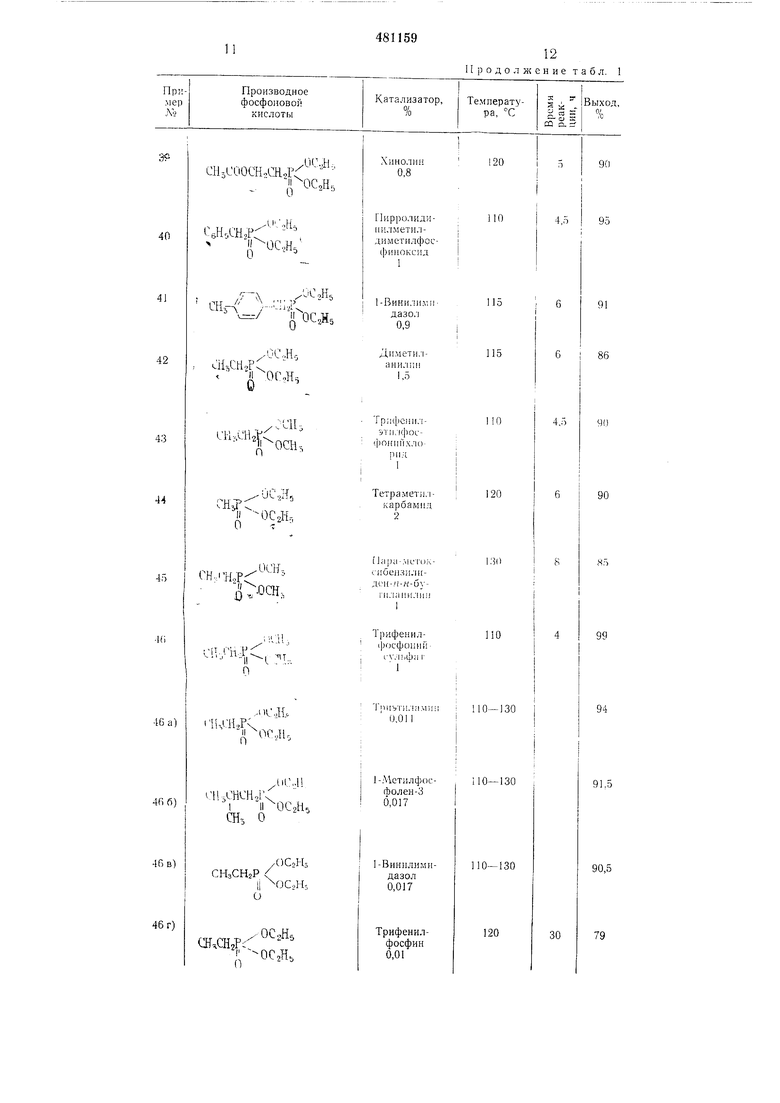
указано в примере 1, с применением различных производных фосфоновой кислоты и различных катализаторов, получают данные, обобщенные в приводимой ниже табл. 1. Пример 47. Дихлорангидрид хлорэтилфосфоновой кислоты из бис-(2-хлорэтилового) эфира хлорэтилфосфоновой кислоты.
Цилиндрический стеклянный сосуд диаметром 7 см и высотой 20 см, снабженный щтуцером для термометра и в нижней части-пластинкой из пористого стекла, ниже которой расположена трубка, подающая газ, погружают до половины высоты в обогревающую ванну. Реактор имеет в верхней части вертикально расположенную стеклянную
трубку, к которой присоединен опускающийся вниз холодильпик, охлаждаемый до 20-40°С, с приемником в виде двухгорлой колбы емкостью 500 см. К этой колбе присоединена (ко второму ее горлу) трубка для отвода
газа.
В цилиндрический сосуд помещают 600 г (2,2 моль) бис-2-хлорэтилового эфира 2-хлорэтилфосфоновой кислоты и 3 г трифенилфосфина.
Через расположенную внизу реактора пооистую пластипку пропускают интенсивную струю фосгена с таким расчетом, чтобы за срок около 4 ч прошло 300 г (8 моль фосгена) при температуре обогревающей ванны порядка 120-130°С. Температура реакции поддерживается па уровне температуры обогревающей ванны или несколько превышает ее за счет тепла, выделяющегося в результате реакции.
Продол ж с и II е т а б л. 1
10
Г1 n о д о л ж с II II с т а б л.
11
481159
12 Продолжение т а б ,i. 1






| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения дихлорангидрида 2-хлорэтилфосфоновой кислоты | 1971 |
|
SU519137A3 |
| Способ получения 2-хлорэтилфосфоновой кислоты | 1973 |
|
SU475782A3 |
| Способ получения диалкиловых эфиров алкилфосфоновых кислот | 1970 |
|
SU511013A3 |
| Способ получения ариловых эфиров хлоругольной кислоты или циклических карбонатов | 1972 |
|
SU527132A3 |
| Способ получения олигомеров гексафторпропилена | 1974 |
|
SU522787A3 |
| Способ получения фосфорсодержащих сложных эфиров | 1975 |
|
SU633485A3 |
| Способ получения 2-фенилэтиленфосфоновой кислоты | 1974 |
|
SU524520A3 |
| Способ получения триизоцианатов | 1976 |
|
SU637081A3 |
| Способ получения 2-хлорэтанфосфоновой кислоты | 1971 |
|
SU528036A3 |
| Способ получения 2-хлорэтанфосфоновой кислоты | 1971 |
|
SU482948A3 |

И-ЛИгР
46 а)
,11,
IH- CHCHoJ
466)
1 inOCzHs
сн, о
/ОСоНз
СНзСНгР
У ОС.Нз О
46 г)
..-ос .На
ат.сн2Р
-ос,н,
0,01
ЬМстилфос110-130фолен-3 0,017
110-130
90,5
120
30
CHsCH.P
ОСН-,
О
к концу реакции температура, развивающаяся в ходе реакции, понижается на 10 - - 15°С при температуре обогревающей ванпы, остающейся па одинаковом уровне.
В результате фракционированной перегонки реакционной смеси получают 23 г дихлорангидрида винилфосфоповой кислоты, имеющего температуру кипения 48-49°С при остаточном давлении 6 мм рт. ст. (выход 7% от теоретического), и 375 г дихлорангидрида 2-хлорэтилфосфоновой кислоты, имеющего температуру кипения 93-94°С при остаточном давлении 6 мм рт. ст. (89% от теоретического) .
1,2-Дихлорэтан, поступающий в сборник с первыми погонами, освобождают от растворенного фосгена промыванием разбавленным аммиачным раствором.
Получают 420 г 1,2-дихлорэтана, что соответствует выходу 92% от теоретического.
Пример 48. Дихлорангидрид хлорэтилфосфоновой кислоты из трех.хлористого фосфора и окиси этилена по одностадийному способу, осуществляемому в одном аппарате.
В цилиндрический стеклянный сосуд для проведения реакции емкостью 1 л, снабженный мешалкой, обратным холодильником термометром и трубкой для подачи газа, достигающей дна реактора, концевая часть которой снабжена пористой пластинкой, пропускают в течение 3-4 ч при охлаждении 500 г окиси этилена при 30-40°С в смесь 500 г треххлористого фосфора и 200 г хлорбензола. По окончании 1 юпускания газа присоединяют посредством стеклянной переходной трубки «обратный холодильник, соединенный, в свою очередь, с двухгорлой колбой и вертикальным холодильником.
Полученную указанным образом реакционную смесь, состоящую главным образом из трис-(2-хлорэтил)-фосфита нагревают с целью перегруппировки до 155-160°С. Дихлорэтан, образующийся в результате перегруппировки, время от времени отгоняют посредством повышения температуры охлаждающей воды в «обратном холодильнике до
0,05
90-ЮО С. Прп этом получают 60 г ди.хлорэтана.
Через 6-7 ч после опорожнения «обратного холодильника отгоняют (при вакууме 20-120 мм рт. ст.) остаток дихлорэтана и хлорбензол, примененный в качестве растворителя. Полученный остаток (906 г) после добавлепия 9 г хиполнна в качестве катализатора обрабатывают газообразным фосгеном через описанную выше трубку для подвода газа при 120-140°С до тех пор, пока (через 6 ч) из отходящих газов не будет более конденсироваться дихлорэтан. После выдувания из состава реакционной смеси путем продувания сухим азотом избыточного количества фосгена отгоняют из реактора в вакууме продукт реакции.
Получают 570 г «сырого но степени чистоты продукта перегонки, имеюп;его т. кип. 40-80°С при остаточном давлении 2 мм. рт. ст.
«Сырой продукт перегонки содержит (по данным газо-хроматографического анализа) 89,8% днхлоранпщрпда 2-хлорэтилфосфоновой кислоты наряду с 6,6% дихлорангидрида винилфосфоновой кислоты, что соответствует выходу дихлорапгидрида 2-хлорэтилфосфопопой кислоты - 77,5 от теоретического, и выходу дпхлора11Г дрида винилфосфоповой кислоты - 7,7% от теоретического, считая на прпмепенное чол 1чесгпп треххлорнстого фосфора.
«Сырой продукт перегонки может Оып. р;1зделе11 перегонкой is ко.попнс.
Пример 49, Дихлорангидрид хлорэтп; фосфоновой кислоты из продукта коидепсацип 500 г остатка после перегонки, образовавшегося в результате реакции перегруппировки трис-хлорэтплфосфита .а,о бис-2-хлорэтилового эфира 2-хлорэтилфосфоновой кислоты после добавления 5 г пиридина в цилиндрическом стеклянном сосуде емкостью 500 мл обрабатывают газообразным фосгеном, подаваемым в нижнюю часть реактора через впаянную пористую пластинку из спеченного тонкоизмельчепного стекла. При этом температура реакционно смеси повышается от 140°С, соответствующих ванне для обогрева, до 145°С. Отходящие газы с целью конденсации образующегося дихлорэтана пропускают через холодильиик. Через 3 ч температура реакционной смеси ири сохраняемом обогреве с помощью ванны понижается до 120°С. В общей сложности пропущено 550 г фосгена. Реакционную смесь освобождают от избыточного количества фосгена посредством получасового пропускания азота при 90 - - 120°С, после чего перегоняют смесь в вакууме.
Наряду с 45 г остатка после перегонки получают 302 г «сырого по степени чистоты продукта перегонки, который по данным газо-хроматографического анализа содержит 85% дихлорангидрида 2-хлорэтилфосфоновой кислоты и 6% дихлорангидрида винилфосфоиовой кислоты. В результате повторной иерегонки в колонне «сырого дистиллата получают 240 г дихлорангидрида 2-хлорэтилфосфоновой кислоты, имеющего температуру кинеиия 88-89°С и 15 г дихлорангидрида вииилфосфоновой кислоты, имеющего температуру кипения 47-49°С при остаточном давлении, в обоих случаях равном 6 мм рт. ст.
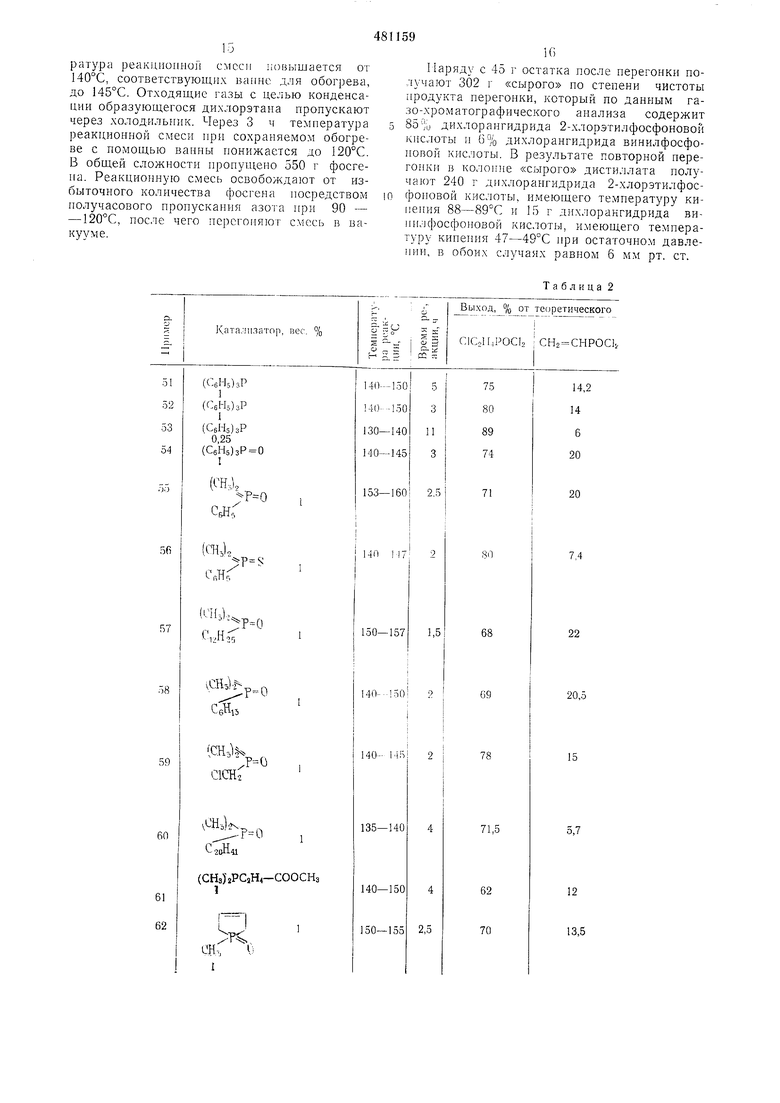
Таблица 2
17
18
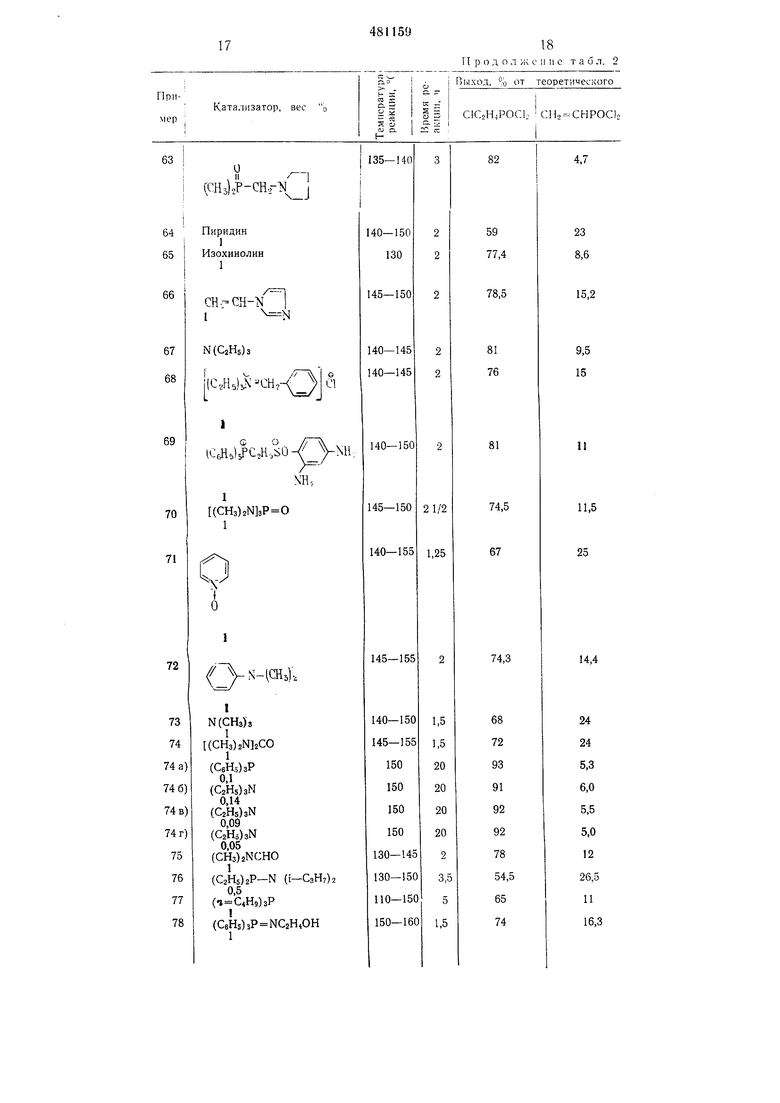
П р о д о л ж с и и с таи л. 2
Пример 50. В реактор, описанный в примере 49, помещают 700 г «сырого по степени чистоты бис- (2-хлорэтилового) -эфира 2-хлорэтилфосфоновой кислоты, содержащего 30% не поддающегося перегонке остатка и при 130-135°С обрабатывают смесь газообразным фосгеном в присутствии 5 г оксида трифенилфосфина в качестве катализатора в течение 4 ч или до тех пор, пока в составе отходящих газов не будет содержаться более дихлорэтана.
Обработку продукта реакции производят, как описано в примере 49. Получают 429 «сырого продукта перегонки наряду с 25 г остатка. По данным газо-хроматографического анализа этот продукт содержит 90% дихлорангидрида 2-хлорэтилфосфоновой кислоты и 7% дихлорангидрида винилфосфоновой кислоты.
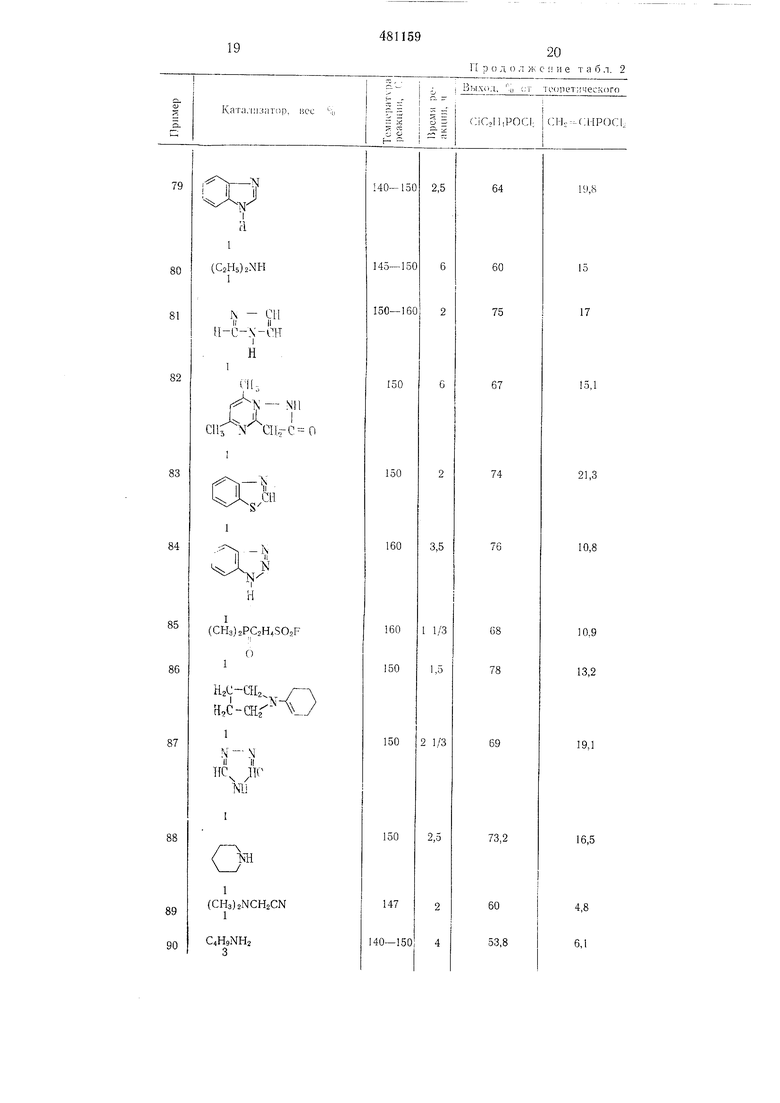
Примеры 51-90. По способу, аналогии.ному описанному в примере 1, получают из бис-2-хлорэтилового эфира 2-хлорэтилфосфоповой кислоты при приводимых ниже условиях дихлорангидрид 2-хлорэтилфосфоновой кислоты и дихлорангидрид винилфосфоновой кислоты. Полученные результаты приведены в табл. 2.
Пример 91. Через смесь 239 г этилфосфоновой кислоты и 4 г пиридина при 130 - 140°С в течение 20 час пропускают фосген. Затем из состава реакционной смеси путем создания разрежения водоструйным насосом при ЮОС удаляют растворенный фосген, после чего перегоняют смесь. Получают 293 г дихлорангидрида этилфосфоновой кислоты, что соответствует выходу 92% от теоретического.
Пример 92. Через смесь 150 г октилфосфоновой кислоты и 1,5 г триэтиламина пропускают при 135-140°С в течение, примерно 6,5 ч фосген. Затем растворенный фосген удаляют из состава реакционной смеси путем создания разрежения водоструйным насосом при 100°С, носле чего перегоняют смесь. Получают 163,5 г дихлорангидрида октилфосфоновой кислоты, имеющего т. кип. 98°С при остаточном давлении С,4 мм рт. ст., что соответствует выходу 91,5% от теоретического.
Пример 93. Через смесь 43,5 г бензилфосфоновой кислоты и 0,2 г пиридина, нагретую до 170°С, пропускают фосген в течение примерно 5 ч. Затем из состава реакционной смеси путем создания разрежения водоструйным насосом при 100°С удаляют растворенный фосген, после чего перегоняют смесь. Получают 163,5 г дихлорангидрида октилфосфоновой кислоты, имеющего т. кип. 103°С при остаточном давлении 0,3 мм рт. ст. Температура плавления 60-62°С, это соответствует выходу 91,5% от теоретического.
Пример 94. 50 г мононатриевой соли октилфосфоновой кислоты суспендируют в 200 мл хлорбензола, добавляют 0,5 г пиридина и нагревают до 120°С. При этой температуре при интенсивном персмещивании в течение 8 час пропускают фосген. Затем охлаждают и отсасывают от выпавщего в виде осадка хлористого натрия, фильтрат освобождают путем создания разрежения водоструйным насосом от растворенного фосгена 1 хлорбензола. Остаток перегоняют, получают 45 г дпхлорангидрида октилфосфоновой кислоты, что соответствует выходу 84% от
теоретического.
Пример 95. 14 г фенилфосфоновой кислоты п 0,1 г пиридина растворяют в 50 мл хлорбензола и нагревают до . При этой температуре в течение 6 час пропускают фосген. Затем реакционную смесь продувают азотом и перегоняют при уменьшенном давлении. Получают 13,5 г дихлорангидрида фенилфосфоновой кислоты, имеющего т. кип. 88°С при остаточном давлении 0,6 мм рт. ст.,
что соответствует выходу 78% от теоретического.
П р и м е р 96. Через смесь 60 г хлорметилфосфоновой кислоты, 16 г дихлорангидрида хлорметилфосфоновой кислоты п 0,5 г пиридина при 130-140°С пропускают фосген в течение 25 ч и после добавления 1 г триэтиламина дополнительно 3 ч при 150°С. Реакционную смесь продувают азотом и перегоняют при уменьшенном давлении. Получают
83 г дихлорангидрида хлорметилфосфоновой кислоты, имеющего т. кип. 82°С при остаточном давлении 11 мм рт. ст. Это соответствует выходу 86% от теоретического.
Предмет изобретения
С1
II
О
где R - С -Cjs-алкил, С -Св-циклоалкил, Cz-С18-алкенил, фенил, CG-Сз-фенилалкил или Сб-Cs-алкилфенил, причем R может
содержать в качестве функциональных групп
хлор, бром, циан, пли низшую ацилоксигруппу; взаимодействием фосгена с производными
фосфоновых кислот общей формулы
TOR
где R имеет указанные выше значения, а R и R - водород, солеобразующий катион, Ci-С12-алкил, (в качестве заместителя может содержать галоген), C -Сз-циклоалкил R и R вместе €2-Ст-алкилен, в том числе один из R и R может быть хлором, или с соответствующими эфирами пирофосфоновых кислот и ангидридами фосфоновых кислот при нагревании с последующим выделением целевого продукта известными прие23мами, отличающийся тем, что, с целью упрощения процесса и повышения выхода продукта, процесс проводят в присутствии каталитических количеств фосфорорганических или азоторганических соединепий или полных5 33 дизамещеиных амидов кислот трех- или пятивалентного фосфора. 2. Способ по п. 1, отличающийся тем, что процесс проводят в среде инертного органического растворителя.
Авторы
Даты
1975-08-15—Публикация
1972-06-14—Подача