(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ АМИНОПИРАЗОЛПИРИМИДИНА
этил-, окси-н-пропил- или оксиизопропилгруппа. Если R4 означает низший алкенилостаток, то им является винил-, аллил- или кротонилостаток, и если R4 означает низший алкоксиалкилостаток, то им является метоксиметил-, метоксиэтил-, метокси-н-пропил-, метоксиизопропил-, этоксиметил-, этоксиэтил-, этокси-нпропил-, этоксиизопропил-, к-пропоксиметил-, н-пропоксиэтил-, н-пропокси-н-пропил-, к-пропоксиизопропил-, изопропоксиметил-, изопроПОКСИЭТИЛ-, изопропокси-н-пропил- или изопропоксиизопропилостаток.
Соединения общей формулы I могут образовывать соли в неорганическими кислотами, например соляной, бромистоводородной, серной, фосфорной, азотной или хлорной, или с органическими кислотами, такими как алифатические, циклоалифатнческие, циклоалифатически - алифатические, ароматические, аралифатические, гетероциклические или гетероциклически-алифатические карбоновые или сульфокислоты, например муравьиная, уксусПредпочтительно эта реакция проводится при условии, когда соединение, соответствующее формуле II вводят в реакцию с водноспиртовым раствором амина общей формулы 1П при температуре, в интервале от комнатной до кипения растворителя.
Желаемое превращение соединений, соответствующих общей формуле I в 5-Ы-оксид происходит благодаря тому, что соединение, соответствующее общей формуле I, окисляют перекисью. Например, превращение может происходить при применении перекиси водорода в пригодном растворителе, например ледяная уксусная кислота, или при применении органической надкислоты, например надуксусная кислота, которая может одновременно применяться также в качестве растная, пропионовая, янтарная, гликолевая, молочная, яблочная, винная, лимонная аскорбиновая, малеиновая, оксималеиновая, пировиноградная, фенилуксусная, бензойная,
5 4 - аминобензойная, антраниловая, 4 - оксибензойная, салициловая, 4 - аминосалициловая, эмбоновая, метансульфо-, этансульфо-, 2 - оксиэтансульфо-, этиленсульфо-, галогенбеизолсульфо-, толуолсуль0 фо-, нафталинсульфосульфаниловая или N - циклогексилсульфаминовая кислоты. Соли с вышеуказанными кислотами приготовляются обычным образом, например путем обработки свободного соединения с помощью
5 кислоты или пригодного ионита.
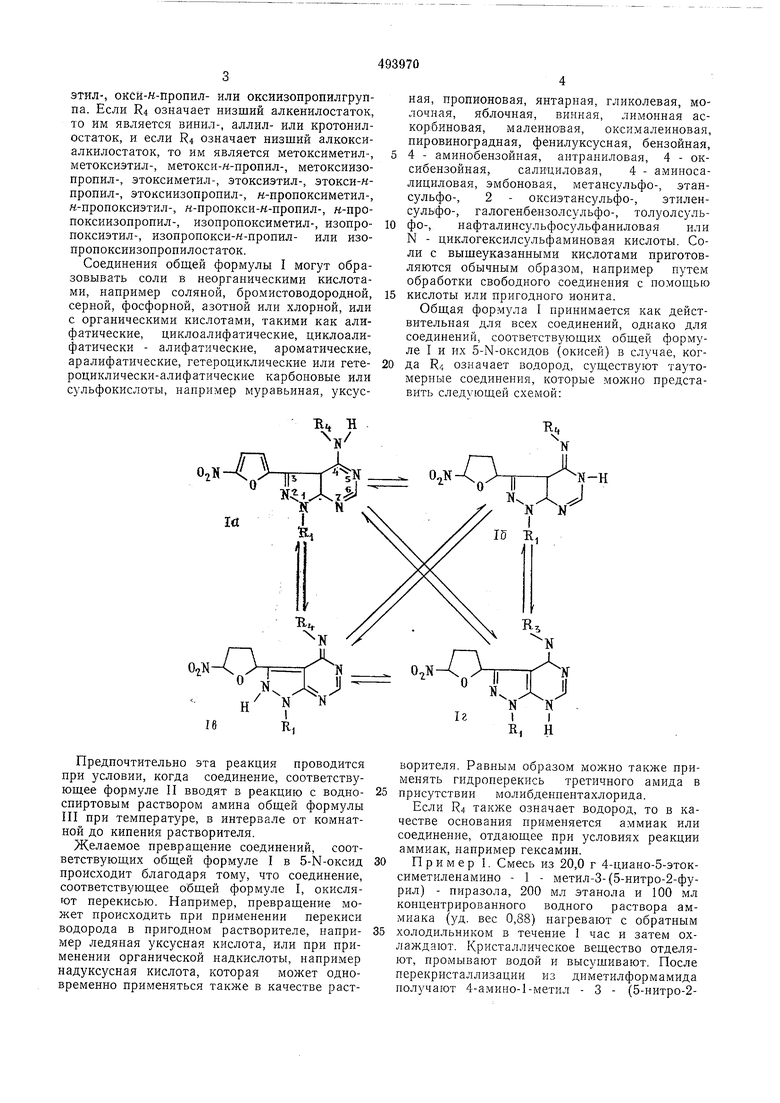
Общая формула I принимается как действительная для всех соединений, однако для соединений, соответствующих общей формуле I и их 5-М-оксидов (окисей) в случае, когда R/, означает водород, существуют таутомерные соединения, которые можно представить следующей схемой:
и.
N
Л
N-H
II
х А
N К
ворителя. Равным образом можио также применять гидроперекись третичного амида в
присутствии молибденпептахлорида.
Если R4 также означает водород, то в качестве основания применяется аммиак или соединение, отдающее при условиях реакции аммиак, например гексамин.
Пример 1. Смесь из 20,0 г 4-циано-5-этоксиметиленамино - 1 - метил-3-(5-нитро-2-фурил) - пиразола, 200 мл этанола и 100 мл концентрированного водного раствора аммиака (уд., вес 0,88) нагревают с обратным
холодильником в течение 1 час и затем охлаждают. Кристаллическое вещество отделяют, промывают водой и высушивают. После перекристаллизации из диметилформамида получают 4-амино-1-метил - 3 - (5-нитро-2фурил) - IH - пиразол - 3,4-rf - пиримидин; т. разл. 305°С. Выход 80%.
На основании характеристических определений спектра ядерного резонанса (трифторуксусная кислота) можно дать следующие значения б, ррш: 8,75 (2Н, S, обмениваемые); 8,70 (1Н, S); 7,60 (1Н); 7,44 (1Н, d); 4,26 (ЗН, S).
Пример 2. Путем, описанным в примере 1, вместо 4 - циано-5-этоксиметиленамино-1метил-3-(5-нитро-2-фурил) - пиразола при тех же реакционных условиях применяют 4- - циано-5-(1 - этоксиэтилиденамино)-1-метил-3-(5-нитро-2-фурил) - пиразол в качестве исходного материала.
Получают 4 - амино-1,6-диметил-3-(5-нитро2-фурил) - 1Н - пиразол- 3,4-(i -пиримидин с точкой разложения 300°С. Выход 30%.
Характеристическими полосами ЯМР-спектра (трифторуксусная кислота) являются J, ррш: 8,51 (2Н, S, обмениваемые); 7,65 (1Н, d)- 7,45 (1Н, d); 4,23 (ЗН, S); 2,83 (ЗН, S).
Пример 3. Смесь из 10,0 г 4-циано-5-этоксиметиленамино-1-метил-3-(5 - нитро - 2 - фурил)-пиразола и 100 мл 33%-ного этанольного раствора метиламина нагревают 30 мин с обратным холодильником, затем охлаждают. Кристаллическое вещество отделяют, промывают эфиром (простым) и затем высущивают. После перекристаллизации из диметилформамида получают 4 - метиламино-1-метил3-(5 - нитро - 2 - фурил)-1Н-пиразол- 3,4- пиримидин; т пл. 280°С. Выход 85%.
Пример 4. При проведении такого же процесса, как описано в примере 3, с применением 4-циано-5-этоксиметиленамино - 1 метил - 3 - (5-нитро-2-фурил),4- -пиримидина и эквивалентного количества этаноламина вместо метиламина при тех же реакционных условиях получают 4-(2-гидроксиэтиламино)-1-метил-3-(5-нитро - 2 - фурил)-1Нпиразол- 3,4-с -пиримидин; т. нл. 212°С. Выход 90%.
Пример 5. При проведении такого же процесса, как описано в примере 3, с применением 4-циано-5-этоксиметиламино - 1 - метил - 3 - (5-нитро-2-фурил)-пиразол - 3,4-d пиримидина и эквивалентного количества
3- метоксипропиламина вместо метиламина при тех же реакционных условиях получают
4- (3 - метоксипропиламин)-1-метил - 3 - (5нитро-2-фурил)-1Н-пиразол - 3,4-й - пиримидин; т. пл. 173°С. Выход 85%.
Пример 6. При проведении такого же процесса, как описано в примере 3, с применением 4 - циано-5-этоксиметиленамино-1-метил-3-(5-нитро-2-фурил) - пиразол - 3,4-(i пиримидина и эквивалентного количества аллиламина вместо метиламина при тех же реакционных условиях получают 4-аллиламино1-метил-3-(5-нитро-2-фурил) - 1Н - пиразол 3,4-(i -пиримидин; т. .пл. 177°С. Выход 70%.
Пример 7. Смесь из раствора 2,0 г 4-амино-1-метил-3-(5 - нитро - 2 - фурил)-1Н-пиразол- 3,4-й -пиримидина в 100 мл ледяной уксусной кислоты и 10 мл 30%-ного (вес. %) раствора перекиси водорода оставляют стоять три дня при комнатной температуре. Реакционную смесь выпаривают досуха, полученное вещество отделяют, промывают уксусной кислотой и высушивают. После перекристаллизации из воды получают 4- амино-1-метил-З(5-нитро-2-фурил) - 1Н - пиразол 3,4-й -пиримидин-5-оксид; т. пл. 285°С. Выход 45%.
Характеристическими полосами спектра ядерного резонанса (трифторуксусная кислота) являются:
б, ррш: 8,53 (1Н, S, обмениваемый); 8,25 (Ш, S);
8,00 (1Н, S, обмениваемый); 7,17 (Ш, d); 6,95 (Ш, d); 3,70 (ЗН, S). ИК-спектр показывает полосы 3490, 1640, 1572 см-Ч
Пример 8. При проведении такого же процесса, как описано в примере 3, с применением 4 - циано-5-этоксиметиленамино - 1 метил-3-(5 - нитро - 2 - фурил) - пиразола и эквивалентного количества диэтиламина вместо диметиламина при тех же реакционных условиях получают 4 - этиламино-1-метил-3-(5-нитро-2-фурил)-1Н-пиразол - 3,4-d пиримидин; т. пл. 240°С. Выход 90%.
30
Предмет изобретения
1. Способ получения производных аминопиразолпиримидина общей формулы I
35
0-,-М
40
где RI - низший алкил,
R4-атом водорода, низший алкил, низший оксиалкил, низший алкенил, низший алкоксинизщий алкил,
или их 5-Ы-оксидов, или их солей, отличающийся тем, что соединение общей формулы II
CN
1
И
,OR
К Н RI
60
где R - низший алкил,
RI имеет выщеуказанные вергают взаимодействию с формулы П1 65R4-NH,
где имеет вышеуказанные вначения, с последующим окислением, в случае необходимости, полученного соединения общей формулы I при известных условиях з соответствующий 5-Ы-оксид и выделением целевого продукта в свободном виде или в виде 5-N-oкcида или в виде соли, известным приемом.
2. Способ по п. 1, отличающийся тем, что в качестве окислителя соединения общей формулы I используют перекись водорода.
надуксусную кислоту, гидроперекись третичного амида.
Приоритет по признакам:
27.04.71:
RI - метил, этил;
R4 - атом водорода;
02.02.72:
R4 - низший алкил, низший оксиалкил, низший алкенил, низший алкоксиалкил;
03.03.72: касается 5-Ы-оксидов соединения общей формулы I и их солей.




Авторы
Даты
1975-11-30—Публикация
1973-11-05—Подача