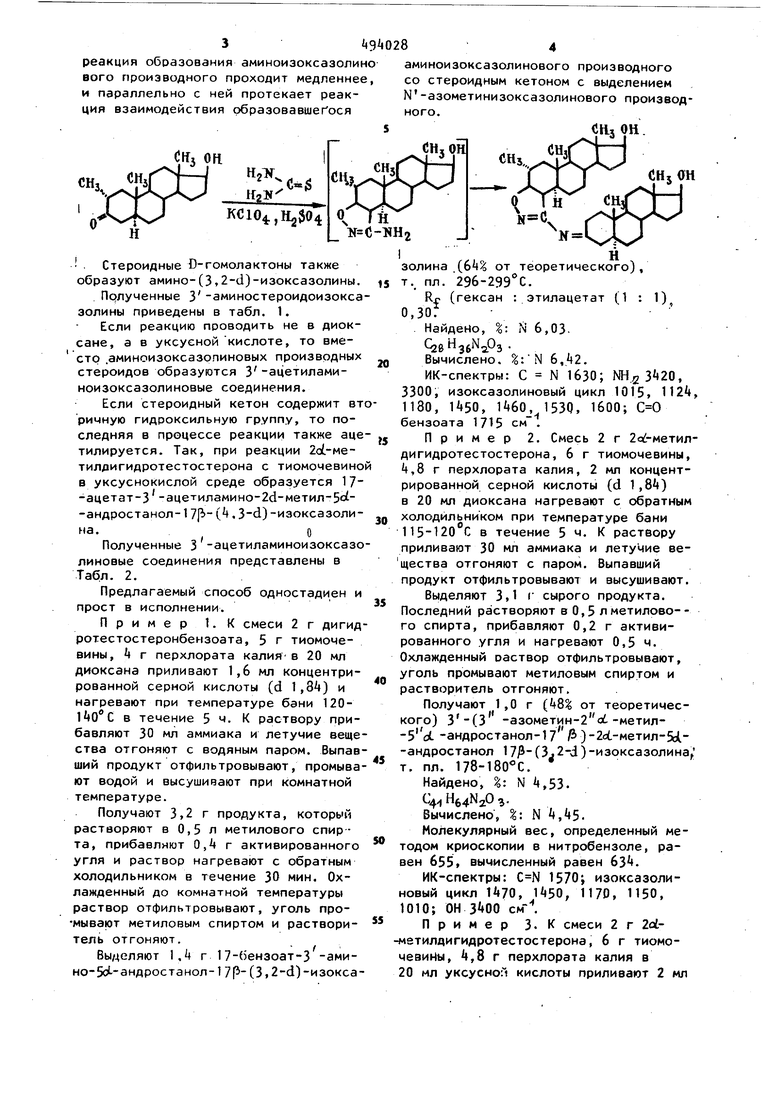
3i«9 028 реакция образования аминоизоксазолино вого производного проходит медленнее, и параллельно с ней протекает реакция взаимодействия образовавшегося % «н сн, «. ..-fVU О ЧхМКС10,Н2304 №С-ИН2 Стероидные D-гомолактоны также образуют aминo-(3,2-d)-изoкcaзoлины. Прлученные 3-аминостероидоизокса золины приведены в табл. 1. Если реакцию проводить не в диоксане, а в уксусной кислоте, то вместо .аминоизоксазопиновых производных стероидов образуются 3-ацетиламиноизоксазолиновые соединения. Если стероидный кетон содержит вт ричную гидроксильную группу, то последняя в процессе реакции также аце тилируется. Так, при реакции 2о -метилдигидротестостерона с тиомочевино в уксуснокислой среде образуется 17 -ацетат-3 -aцeтилaминo-2d-мeтил-5ot-андростанол-1 С, 3-d) -изоксазолина.О Полученные 3 -ацетиламиноизоксазо линовые соединения представлены в Табл. 2. Предлагаемый способ одностадиен и прост в исполнении. Пример 1. К смеси 2 г дигид ротестостеронбензоата, 5 г тиомочевины, i г перхлората калия-в 20 мл диоксана приливают 1,6 мл концентрированной серной кислоты (d 1,8) и нагревают при температуре бани 120l jQ C в течение 5 ч. К раствору прибавляют 30 мл аммиака и летучие веще ства отгоняют с водяным паром. Выпав ший продукт отфильтровывают, промыва ют водой и высушивают при комнатной температуре. Получают 3,2 г продукта, который растворяют в 0,5 л метилового спирта, прибавляют 0, г активированного угля и раствор нагревают с обратным холодильником в течение 30 мин. Охлажденный до комнатной температуры раствор отфильтровывают, уголь промывают метиловым спиртом и растворитель отгоняют. Выделяют 1,4 г 17-бензоат-З -амино-5о--андростанол-1 7p-(3,2-d)-изoкca ами со Nногноизоксазолинового производного стероидным кетоном с выделением азометинизоксазолинового производо. 1113 ОН. НзОН .„ СНл1 Н5.. CHj он (п золина (6А% от теоретического), т.. пл. 29б-299С. Rn (гексан : этилацетат (1 : . Найдено, %: N 6,03СзвНзб аОзВычислено. : N 6,42. ИК-спектры: С N 1бЗО; МН23«20, 3300, изоксазолиновый цикл 1015, 112, 1180, U50, , 1330, 1600; бензоата 1715 см. Пример 2. Смесь 2 г 2с| -метилдигидротестостерона, 6 г тиомочевины, t,8 г перхлората калия, 2 мл концентрированной серной кислоты (d 1,8) в 20 мл диоксана нагревают с обратным холодильником при температуре бани 115-120 С в течение 5 ч. К раствору приливают 30 мл аммиака и летучие вещества отгоняют с паром. Выпавший продукт отфильтровывают и высушивают. Выделяют 3,1 с сырого продукта. Последний растворяют в 0,5 лметилово-го спирта, прибавляют 0,2 г активированного угля и нагревают 0,5 ч. Охлажденный раствор отфильтровывают, уголь промывают метиловым спиртом и растворитель отгоняют. Получают 1,0 г (k8% от теоретического) 3-(3 -азометин-2 о6-метил-5oL -андростанол-17 Э)-2с(.-метил-5Ь1.-андростанол (3.2-d ) -изоксазолина, т. пл. 178-180°С. Найдено, %: N i,53. C4 Hfc4N203Вычислено, %: N ,. Молекулярный вес, определенный методом криоскопии в нитробензоле, равен б55, вычисленный равен бЗ ИК-спектры: 1570; изоксазолиновый цикл U70, 1«50, 117D, 1150, 1010; О см-. Пример 3. К смеси 2 г 2с1метилдигидротестостерона, 6 г тиомочевины, 4,8 г перхлората калия в 20 мл уксусной кислоты приливают 2 мл
концентрированной серной кислоты и нагревают до кипения в течение 5 ч. Затем к раствору приливают 50 мл водного раствора аммиака и летучие вещества отгоняют с паром. Охлажденный раствор отфильтровывают, промывают водой и высушивают.
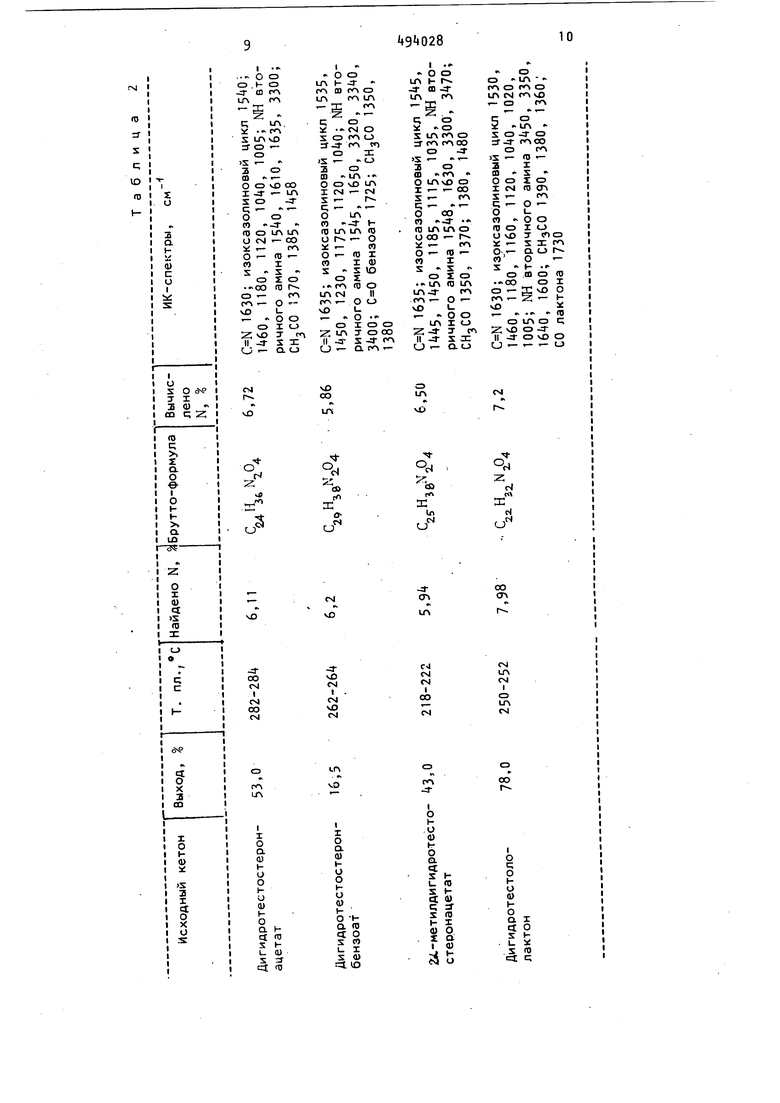
Выделяют 2,2 г сырого продукта, который перекристаллизовывают из 11 мл этилацетата.
Выделяют 1,2 г («3% от теоретического) 17 ацетат-3 -ацетиламино-2л1-метил-5о -андростанол-1 7/ 1, З-с) -изоксазолина; т. пл. 218-222 €.
Найдено, I: N 5,9.
C2 H3eN2p4Выч ислено, N 6,50.
ИК-спектры; 1635; изоксазолиновый цикл 15«5. , П83, 1115, 1035, NH вторичного амина , 3300, 1630, 15«8, 1350, 1370, 1380, см-1
1 elozs12
Формула изобретениявзаимодействию с тиомочевиной в растСпособ получения 3 -аминоизоксазо- ворах диоксана или уксусной кислоты линовых производных стероидов, от- в присутствии перхлората калия и серличающийся тем, что соот- ной кислоты и целевой продукт выделяветствующий кетостероид подвергают5 ют известными приемами.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения изоксазолиновых производных стериодных кетонов | 1973 |
|
SU447402A1 |
| Способ получения хинолиновых или изохинолиновых производных 3-кетостероидов | 1974 |
|
SU521282A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ХОЛЕСТАНА | 1971 |
|
SU423294A3 |
| Способ получения 2-(6"-метилурацил-2")стероидов | 1974 |
|
SU514849A1 |
| Способ получения перхлоратов демитиламинометиленовых производных стероидных кетонов | 1972 |
|
SU448713A1 |
| ВПТБ | 1973 |
|
SU399133A1 |
| Способ определения дигидротестостерона и его производных в масляной смеси | 1981 |
|
SU1083116A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЬ1Х ИНДОЛА | 1970 |
|
SU262906A1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНДОЛИЛ-3-АЛКАНКАРБОНОВЫХКИСЛОТ | 1968 |
|
SU218770A1 |
| СПОСОБ ПОЛУЧЕНИЯ 17-АЗАСТЕРОИДОВ | 1973 |
|
SU399138A1 |


Авторы
Даты
1982-06-23—Публикация
1974-01-14—Подача