(54)
: СПОСОБ ПОЛУЧЕНИЯ КОНДЕНСИРОВАННЫХ АЗАГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
« Г J 5 r-flTfi
.: и1:пШ

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 1-алкокси-2,6диоксифосфоринан-1-онов | 1975 |
|
SU568651A1 |
| Способ получения 2-замещенных 5,5-диметил-4-оксо-1-пирролин-1-оксидов | 1985 |
|
SU1356400A1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-ОКСО-19-НОР-А4-СТЕРОИДОВ | 1974 |
|
SU439089A3 |
| Способ получения производных дипептиданилида | 1990 |
|
SU1773917A1 |
| НОВОЕ АНТИТРОМБОТИЧЕСКОЕ И АНТИАТЕРОСКЛЕРОТИЧЕСКОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2011 |
|
RU2483066C1 |
| Способ получения производных 1-ацилгомопиримидазола или их солей | 1973 |
|
SU584781A3 |
| Способ получения 2-замещенных перимидина | 1973 |
|
SU504770A1 |
| Способ получения 4-кето-10а-окси1,2,3,4,5,6,7,8,8а,10а-декагидроксантенов | 1972 |
|
SU445656A1 |
| Способ получения производных бензо (с) хинолинов или их фармацевтически приемлемых солей с кислотами | 1978 |
|
SU953981A3 |
| Способ получения 11-дезокси-16арилокси- -тетранорпростагландинов или их солей | 1976 |
|
SU679134A3 |

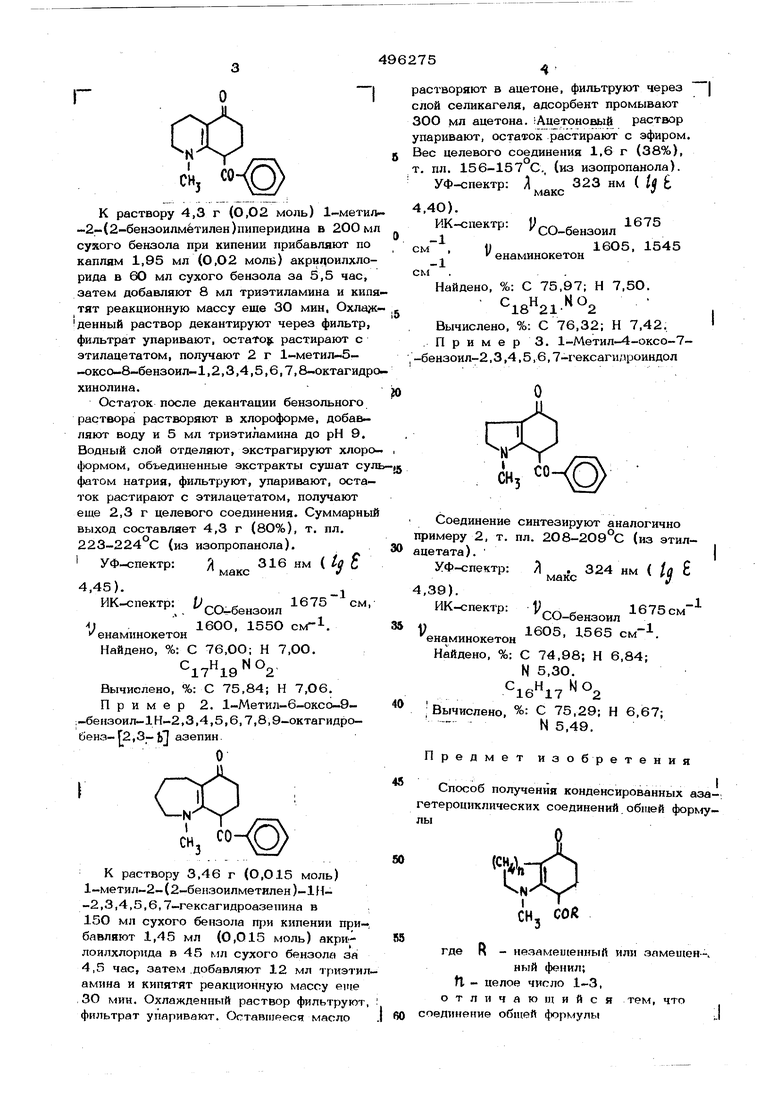
Предлагается способ получения новых производных индола, хинолшш, и бензазе.пина, которые могут найти применение в качестве биологически активных веществ, а также промежуточных соединений в органическом синтезе. Известна реакция 1-метил-2-этиленпирролидина и 1-метил.-2.-этилиденпиперидина с акролеином, протекающая с образованием гидрированных производных индола и хино- лина. Однако соединения, полученные этим способом, не содержат функциональных груп пировок, на основе которых было бы возмо но дальнейшее структурное изменение веществ. Предлагается способ получения конденсированных азагетероциклических соединений общей формулы CHj (ох R - незамещенный или замещенный фенил; fl - целое число 1-3. Способ получения предлагаемых соединений заключается в том, что соединение общей формулы CU N CHCOR где R и fj, имеют указанные значения, подвергают взаимодействию с акрилоилхлоридом с последующими обработкой реак..ционной массы органическим основанием, например триэтиламином, и выделением целевого продукта известными приемами. г Строение полученных целевых соединений доказано ИК- и ПМР-спектрами. Пример 1. 1-Метил-5-оксо-б....бензоил-1,2,3,4,5,6,7,8-октагидрохинолин К раствору 4,3 г (О,О2 моль) 1-метил -2-{2-бенэоипметилен) пиперидина в 200м сухого бензола при кипении прибавляют по каплям 1,95 мл (0,О2 моль) акрицоилхлорида в 60 мл сухого бензола за 5,5 час, затем добавляют 8 мл триэтиламина и кип тят реакционную массу еше 30 мин, Охла данный раствор декантируют через фильтр, фильтрат упаривают, остато| растирают с этилацетатом, получают 2 г 1-метил-5-оксо-8-бензоил-1,2,3,4,5,6,7,8-октагидр хинолина. Остаток после декантации бензольного раствора растворяют в хлороформе, добавляют воду и 5 мл триэтиламина до рН 9. Водный слой отделяют, экстрагируют хлоро формом, объединенные экстракты сушат су фатом натрия, фильтруют, упаривают, остаток растирают с этилацетатом, получают еще 2,3 г целевого соединения. Суммарны выход составляет 4,3 г (80%), т. пл. 223-224 С (из изопропанола). Я316 нм ( to Е УФ-спектр: макс/ 4,45). i; 1675 см, ИК-спектр: СО-бензоил И)16ОО, 155О см-1. енаминокетон Найдено, %: С 76,ОО; Н 7,ОО. Вычислено, %: С 75,84; Н 7,О6. Пример 2. 1-Метил-6-оксо-9;-бензоил-1Н-2,3,4,5,6,7,8,9-октагидробенз-Г2,3-ЬТ азепин. К раствору 3,46 г (0,015 моль) 1-метил-2-(2-бензоилметнлен )-1Н-2,3,4,5,6,7-гексагидроазепина в 15О мл сухого бензола при кипении при-, бавляют 1,45 мл (0,015 моль) акрилоилхлорида в 45 мл сухого бензола за 4,5 час, затем .добавляют 12 мл триэтиламина и кипятят реакционную массу еще ЗО мин. Охлажденный раствор фильтруют, фильтрат упаривают. Оставшееся масло створяют в ацетоне, фильтруют через ой селикагеля, адсорбент промывают 0 мл ацетона. ;Ацетоновь1й раствор аривают, остаток растирают с эфиром. с целевого соединения 1,6 г (38%), пл. 156-157 С., (из изопропанола). УФ-спектр: Д323 нм ( 1§ i максJ 4О). ИК-спектр: J 1675 СО-бензоил 1605, 1545 енаминокетон Найдено, %: С 75,97; Н 7,5О. Вычислено, %: С 76,32; Н 7,42, П р и м е р 3. 1-Метил-4-оксо-7ензоил-2,3,4,5,6,7-1ексагилроиндол Соединение синтезируют аналогично имеру 2, т. пл. 2О8-2О9°С (из этилетата). УФ-спектр: Я . 324 нм 39). ИК-спектр: V1675см СО-бензоил СО-ЙРНЯПМП енаминокетон - см . Найдено, %: С 74,98; Н 6,84; N 5,30. .Вычислено, %: С 75,29; Н 6,67; N 5,49, редмет изо б р е т е н и Способ получения конденсированных азатероциклических соединений общей формуCHj COR где R - незамещенный или замешен- ный фенил; Н - целое число 1-3, отличающийся тем, что оединение общеЛ фюрмулы К1 CHCOR Ig vHj -I где R и ft имеют указанные значения, подвергают взаимодействию с акрилоил- хлоридом с последующими обработкой реакционной .массы органическим основанием, например триэтиламином, и выделением целевого продукта известными приемами.
Авторы
Даты
1975-12-25—Публикация
1974-03-05—Подача