(54) СПОСОБ ПОЛУЧЕНИЯ ВОДОНЕРАСТВОРИМОГО ФЕРМЕНТНОГО ПРЕПАРАТА



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 6-аминопенициллановой кислоты | 1974 |
|
SU654170A3 |
| Способ получения иммобилизованных ферментов | 1977 |
|
SU744002A1 |
| Препарат фермента | 1977 |
|
SU687080A1 |
| Способ проведения ферментативныхРЕАКций | 1975 |
|
SU847926A3 |
| Способ получения носителя для иммобилизации белков | 1977 |
|
SU897770A1 |
| ИММОБИЛИЗОВАННАЯ КАТАЛАЗА | 1991 |
|
RU2016901C1 |
| Способ иммобилизации микробных клеток | 1975 |
|
SU608479A3 |
| Способ получения иммобилизованной рибозофосфатизомеразы | 1985 |
|
SU1326616A1 |
| Способ получения препарата для определения моноаминов на основе иммобилизованной моноаминооксидазы | 1987 |
|
SU1495378A1 |
| БИОКАТАЛИЗАТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2233327C2 |

1
Изобретение относится к области микробиологии, в частности к получению ферментных препаратов повышенной активности из ненициллинов.
Водонерастворимые ферментные препараты получают из фермента пенициллин-ацилазы; водонерастворимого абсорбирующего материала, предпочтительно из структурированного полиакрилата, содержащего свободные карбоксильные группы; водорастворимого диальдегида, например глутарового; алифатического диамина, предпочтительно а, ы-диаминоалкана с 2-10 углеродными атомами. Указанные ферментные препараты обл.адают повышенной активностью при получении 6-аминопенициллиновой кислоты.
Известен способ получения водонерастворимого ферментного препарата путем смещения в водном растворе водонерастворимого абсорбирующего материала с пенипиллин-ацилазой и диальдегидом, отделения твердого осадка и его промывки. Однако в известном способе выделение фермента из реакционной смеси затруднено: Способ пе обеспечивает также высокого выхода 6-аминопенициллиновой к: слоты и имеет невысокую степень новторного использования ферментного препарата при последующих (периодических) реакциях получения этой кислоты. Для повышения стабильности и эффективности действия препарата предлагается абсорбирующий материал, пепипиллпн-ацилазу и диальдегид дополнительно смешивать с алифатическим диамином, предпочтительно а, мдиаминоалканом с 2-10 атомами углерода.
Абсорбирующий материал смешивают с ферментом ацилазой, а затем к смеси последовательно добавляют диальдегид и диамин; абсорбирующий материал смешивают с ферментом ацилазой и диамином, а затем к смеси
добавляют диальдегид; абсорбирующий материал смешивают с диамином и диальдегидом, а затем к смеси добавляют пенициллин-ацилазу.
Каждое из веществ, диамин и диальдегид,
добавляют в количестве 0,01-20 ммоль/г абсорбирующего материала в молярном соотношении диамина и диальдегида от 1 : 0,1 до 1 : : 40, предпочтительно в интервале от 1:1 до 1 : 10. При этом диамип добавляют в количестве 0,1-5,0, предпочтительпо 0,2-2 ммоль/г абсорбирующего материала. Диальдегид добавляют в количестве ОД-10, предпочтительно 2,5-5,0 ммоль/г абсорбирующего материала. Способ осуществляют следующим образом Фермент ацилазу получают предпочтительно от бактерий, нанример штаммов Эшерихиа коли, для использования при расщеплении бензилпенициллина до 6-аминопенициллиновой кислоты или, например, из грибков и акцитомицетов для расщепления феноксиметилпенициллина. Предпочтительным водорастворимым диальдегидом являются глиоксаль или глутаровый альдегид. В качестве абсорбирующего материала используют порошкообразную целлюлозу и ее производные, ионообменные смолы, силикагель и другие полимерные материалы. Предпочтительно использовать структурированные полиакрилатные или полиметакрилатные смолы, например, в макросетчатой форме, то есть при высоком соотношении удельной поверхности к весу. В качестве водонерастворимого адсорбента применяют тонкоизмельченный полимерный материал с достаточной поверхностью для получения водонерастворимых ферментных препаратов высокой удельной активности, при этом поверхность возрастает по мере уменьшения размеров частиц абсорбента. В случае структурированных поли-(мет)-акрилатов частицы смолы могут иметь средний размер 0,6 мм, а удельная поверхность смолы достигает 450 . По мере уменьшения размеров частиц повышается эффективность реакции сочетания, а также удельная активность целевого водонерастворимого ферментного препарата. Из алифатических аминов предпочтительно использовать а,(й-алифатический диамин с прямой цепью из 2-10 углеродных атомов, например 1,3-диаминопропан или 1,6диаминогексан. Ферментный препарат получают в водном растворе при рН 5-9. Водонерастворимый абсорбент сначала контактирует с ацилазой в присутствии диамина, а затем - противоточно с диальдегидом и алифатическим диамином. В этом случае фермент абсорбируют в присутствии диамина в количестве 0,1-5, нредпочтительно 0,2-2 ммоль/г абсорбента, и диальдегида в количестве 0,25-10,0, предпочтительно 2,5-5,0 ммоль/г абсорбирующего материала. Для исключения реакции избыточного альдегида по окончании реакции копуляции смолу с ферментом промывают раствором метабисульфита натрия, алифатического диамина, мочевины или глицина. Стабильность фермента - смолы определяют инкубацией водонерастворимых ферментных препаратов, увлажненных буферным раствором при рН 7,8 и 37°С. При отсутствии стабилизирующего действия субстрата или продуктов быстро увеличивается потеря активности фермента. Ферментные препараты более высокой стабильности получают путем предварительной обработки абсорбента смесью диамина и диальдегида с последующей абсорбцией фермента ацилазы. При этом диамин и диальдегид используют в количестве 0,, предпочтительно 0,1 -10 ммоль/г абсорбента, а молярное соотношение диамина и альдегида должно быть от 1 : 0,1 до 1 : 40, предпочтительно от 1 : 1 до 1 : 10, при рН 4-9. При оптимальных условиях стабильность ферментного препарата достаточна для проведения 50 или более последовательных расщеплений пенициллина. Активность фермента после абсорбции на субстрате повышается, например, при использовании в качестве последнего структурированной поли-(мет)-акрилатной смолы, если фермент предварительно обрабатывают моноили диальдегидом, например формальдегидом или глутаровым альдегидом при концентрации 0,5-5% и рН 5-8 в течение 2-24 ч з случае формальдегида и при концентрации 0,01-0,5% и рН 5-8 в течение 2-24 ч в случае глутарового альдегида. Такую обработку проводят до или после выделения фермента из его природного источника, например из целых клеток Е. коли. Чистота фермента (препарата) колеблется от 0,15 до 50 ммоль/ мин/мг протеина и обычно лежит в интервале 1,5-15 ммоль/мин/мг протеина. Эффективность реакции копуляции и удельная активность водонерастворимого ферментного препарата повышаются при повышении степени чистоты используемого при реакции копуляции фермента. Температура реакций копуляции колеблется от 1 до , предпочтительно 15-25°С. Возможна также обработка бензилпенициллина или феноксиметилпенициллина водонерастворимьш ферментным препаратом в водной среде с рН 6,0-9,0, предпочтительно 7,0- 8,5, для получения 6-аминопенициллиновой кислоты. При этом рН влажной смеси поддерживают периодическим или непрерывным добавлением щелочи (так -как в процессе дезацилирования от пенициллина отрывается боковая цепь) в емкости с мешалкой или в реакторе типа колонки. Используемая смола амберлит ХАД-7 представляет собой структурированный полиметакрилат в макрорешетчатой форме. Частично очищенный препарат фермента цилазы получают выделением фермента из леток ацилазы нродуцирующего штамма .КОЛИ № С1В8743 механическим путем в гоогенизаторе. Обломки клеток удаляют фильрацией после доведения рН до 5,0. Фермент саждают общепринятым способом, например ульфатом аммония, насыщением до 75% бором осадка, повторным растворением в вое, диализом раствора, используемого непоредственно для копуляции с водонераствориым абсорбентом, либо подвергают сублимаии (сушке вымораживанием), а затем расворению по мере необходимости.
Пример 1. Некоторое количество диамина растворяют в 1500 мл 0,5 М цитратно-фосфатного буфера при рН 5,0. Далее доводят рН до 5,0, вносят заданное количество пенициллин-ацилазы и 100 г амберлита ХАД-7, перемешивают в течение 18 ч при комнатной температуре. Затем приливают 100 мл 50%ного водного раствора глутарового альдегида и доводят рН до 5,0. После дополнительного перемешивания в течение 18 ч твердое веш,ество отфильтровывают, промывают чодой.
Пример 2. Способ осуш,ествляют, как в примере 1, используя 300 мл буферного раствора и 50 мл фермента амилазы в 250 мл воды при перемешивании фермента и смолы в течение 18 ч до добавления 200 мл 25%-ного водного раствора глутарового альдегида. Активность препарата 20,6 мкм/мин/г.
При использовании 103 г указанного веш,ества для дезацилирования бензилпенициллина (как в примере 1) 91% пенициллина конверсируется в 6-аминопенициллиновую кислоту в течение 6 ч после 18 последовательных повторных использований вешества.
Пример 3. Заданное количество 1,3-диамииопропана растворяют в 1500 мл 0,25 М фосфатного буфера при рН 7,0. При рН 7,0 вносят 25 мл раствора пенициллин ацилазы и 100 г амберлита ХАД-7, перемешивают в течение 18 ч, добавляют 200 мл 25%-пого раствора глутарового альдегида, доводят рН до 7,0 и перемешивают еше 18 ч. Затем фильтруют, промывают, как в примере 1, и получают препарат установленной активности.
При использовании указанного вещества для дезацилирования 1 л 6%-ного бензилпенициллин-калия при рН 7,8 и 37°С получают конверсию после 5 ч при десяти последовательных экспериментах.
Результаты дезацилировання приведены в табл. 2.
Пример 4. В 300 мл 0,5 М фосфатного буфера при рН 7,0 вводят 60 мл раствора пенициллин-ацилазы, затем 240 мл дистиллированной воды и 100 г амберлита ХАД-7. Фер5%-ным раствором метабисуль|)ита натрия, 1 М раствором хлористого натрия и 0,5 М фосфатным буфером при рН 7,8. Далее определяют активность препарата. Некоторое количество полученных препаратов используют для проведения ряда последовательных дезацилирований бензилпенициллина калия - 6% в литровом реакторе с мешалкой при рН 7,8 и 37°С. Выход конверсии з каждом эксперименте определяют через 5 ч. Результаты опытов приведены в табл. 1.
Таблица 1
Таблица 2
мент абсорбируют на см )ле в течение 18 ч при перемешивании.
Затем вносят И мл 1,3-диаминопропана и 200 мл 25%-ного водного раствора глутарового альдегида так, чтобы поддерживать рН 8,0. Далее раствор доводят до рН 7,0, перемешивают еш,е 18 ч, фильтруют и твердое веш,ество промывают, как в примере 1.
Получают 107 г нерастворимого фермента с активностью, установленной на Ьензилпенициллин-калий и равной 11,92 мкм/мин/г.
Пример 5. В 500 мл раствора пенициллин-ацилазы, приготовленного на 0,2 М фосфатном буфере при рН 7,0, вносят 100 г амберлита ХАД-7. Смесь перемешивают в течение 16 ч. Твердое вепхество отфильтровывают, вносят в 500 мл 5%-ного раствора глутарового альдегида в 0,1 М фосфатном буфере при рН 7,0 и перемешивают еше 16 ч.
Твердое вешество снова отфильтровывают, вносят в 500 мл 0,2%-ного растзора 1,3-диаминопропана в 0,1 М фосфатном буфере при рН 7,0 и перемешивают еш,е 16 ч. ОтфильтроБывают твердое вещество, промывают 5%-ным водным раствором хлористого натрия, 2,5%-ным раствором метабисульфита натрия и 0,2 М фосфатным буфером при рН 7,0. Активность препарата 30,8 rviKM/мин/г.
Пример 6. В 600 мл воды вносят 100 г амберлита ХАД-7 и 200 мл 25%-кого водного раствора глутарового альдегида, рН доводят до 7,0 и перемешивают в течение 2 ч. Далее приливают 2 мл 1,3-диаминопропана и перемешивают еще 18ч. Твердое вещество отфильтровывают, промывают водой и суспендируют в 575 мл 0,2 М фосфатного буфера при рН 7,0. Затем приливают 25 мл раствора пенидиллинацилазы и перемешивают еще 18 ч. Твердое отфильтрованное вещество промывают 1 М раствором хлористого натрия и 0,2 М фосфатным буфером при рН 7,8. Активность препарата 42 мкм/мин/г.
120 г препарата используют для дезацилирования 1 л 8%-ного раствора бензилпенициллин-калия при рН 7,8 и 37°С; при этом за 5 ч при щести последовательных экспериментах конверсируется больще 80% субстрата.
Пример 7. К 1 мл диаминопропана и 4 мл 25%-ного (объем/объем) глутарового альдегида в 0,2 М при рН 4,5-8,5 добавляют раствор фермента (77 мкм/мин/г) и 20 г структурированной полиметакрилатной смолы - амберлита ХАД-7.
Доводят объем до 100 мл, перемешивают его в течение 16 ч при комнатной температуре, отфильтровывают смолу и тщательно промывают фосфатным буфером при рН 7,8. Удельную активность смолы определяют еразу же и после хранения последней при 37°С в течение 1,4 и 5 дней.
Результаты испытаний приведены в табл. 3.
Таблица 3
Пример 8. В 0,2 М фосфатный буферный раствор вносят 16 мл 25%-ного раствора глутарового альдегида и 1 мл диаминопропана при рН 5-9, доводят объем до 100 мл, вносят 25 г амберлита ХАД-7, перемешивают в течение 16 ч при 25°С и промывают буферным раствором при рН 6,0.
Смолу переносят в раствор фермента в 0,2 М фосфатном буферном растворе при рН 6,0, перемешивают в течение 16 ч при 25°С,
отфильтровывают и промывают 0,2 М буферным раствором при рН 7,8.
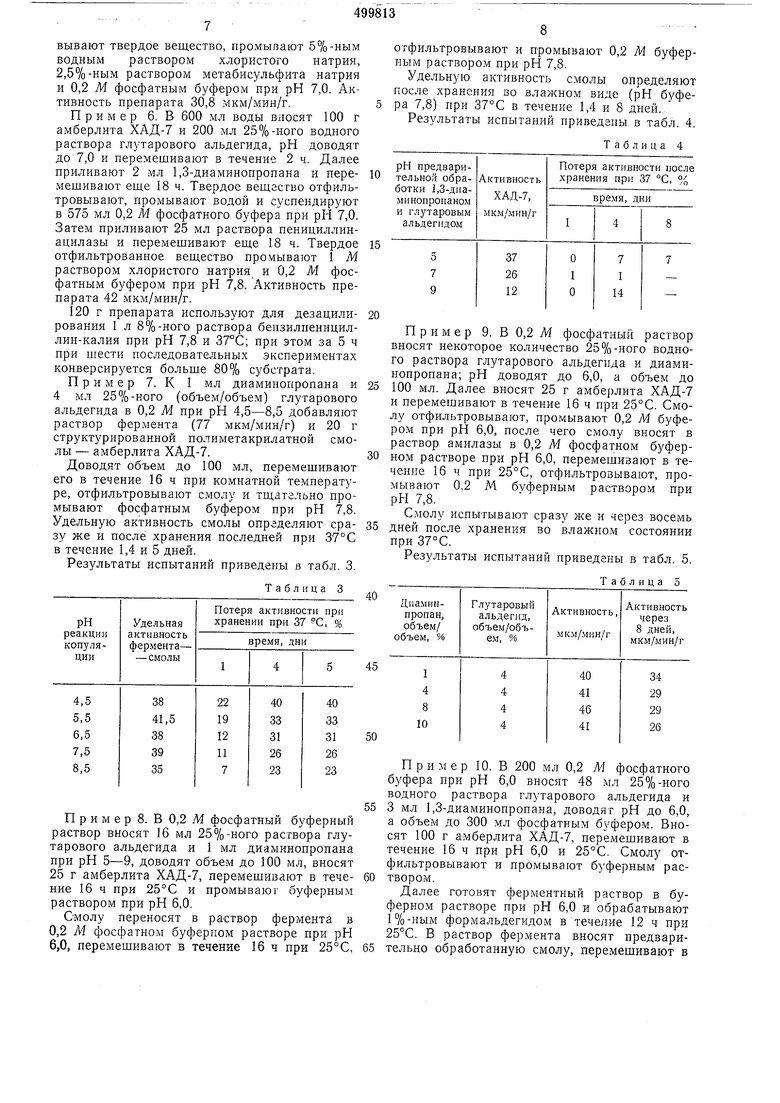
Удельную активность смолы определяют после хранения во влажном виде (рН буфера 7,8) при 37°С в течение 1,4 и 8 дней.
Результаты испытаний приведены в табл. 4.
Таблица 4
Пример 9. В 0,2 Af фосфатный раствор вносят некоторое количество 25%-ного водного раствора глутарового альдегида и диамипопропана; рН доводят до 6,0, а объем до 100 мл. Далее вносят 25 г амберлита ХАД-7 и перемешивают в течение 16 ч при 25°С. Смолу отфильтровывают, промывают 0,2 М буфером при рН 6,0, после чего смолу вносят в раствор амилазы в 0,2 М фосфатном буферном растворе при рН 6,0, перемешивают в течение 16 ч при 25°С, отфильтровывают, промывают 0,2 М буферным раствором при рН 7,8.
Смолу испытывают сразу же и через восемь дней после хранения во влажном состоянии при 37°С.
Результаты испытаний приведены в табл. 5.
Таблица 5
Пример 10. В 200 мл 0,2 М фосфатного буфера при рН 6,0 вносят 48 мл 25%-ного водного раствора глутарового альдегида и 3 мл 1,3-диаминопропана, доводят рН до 6,0, а объем до 300 мл фосфатным буфером. Вносят 100 г амберлита ХАД-7, перемешивают в течение 16 ч при рН 6,0 и 25°С. Смолу отфильтровывают и промывают буферным раствором.
Далее готовят ферментный раствор в буферном растворе при рН 6,0 и обрабатывают 1%-ным формальдегидом в течение 12 ч при 25°С. В раствор фермента вносят предварительно обработанную смолу, перемешивают в
Авторы
Даты
1976-01-15—Публикация
1973-07-20—Подача