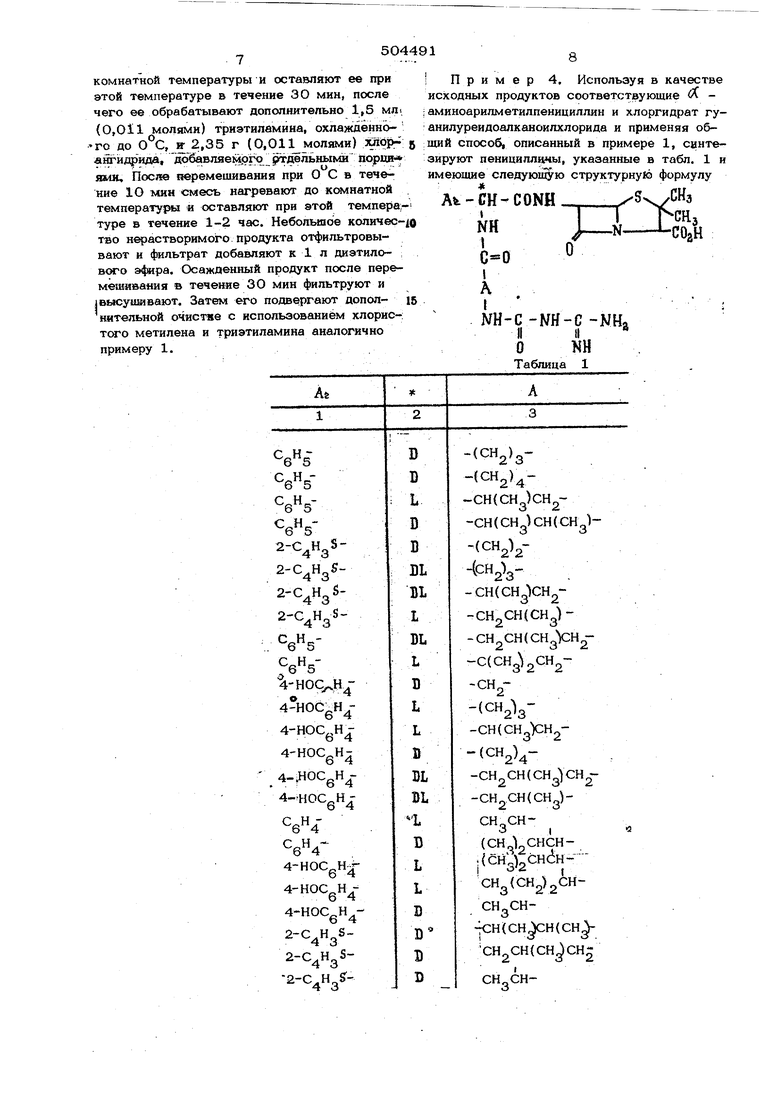
(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗЕЮДНЫХ ПГ:НИ111)/1ЛИИ.Л или их солей, где л - фенил, 4-оксифвнил, 2-тиенип или 3-тиенил; 1 - целое число, равное 1-3; А - алкилен, содержащий 1-4 ато углерода или алкилидеи, содержащий 2-4 атома углерода; каждый из радикалов R- - Б . -атом водорода или алкил, содержащий 1-4 атом углерода; К„ (совместно) - алкирадикалы R и яен, содержащий 2-4 атома углерода; радикалы R. л (совместно) - алки.ленд содержащий 2-4 атома углерода; радикалы R и R (совместно) - алкилен, содержащий 4-5 атома углерода. Сущность способа заключается во взаимодействии соединения общей фо|)мулы AI - СН CONH 5х/ ,. П I -N -СОаН где . имеет указанные значения, с соединением общей формулы О II / P Rjl -C-N-C-X где RJ - F „ имеют указанные значени а X - радикалы формулы -NH-A-cocje-HW или ГЫНАСО -0-N, I-JK где А и Ki имехгг указанные значения. Если X пр)едставляет собой-ЖЯ-А-СО НС1,реакцию обычно проводят в среде инертн го апротонного растворителя в присхтстви галоидводородной противогарной присадки, например третичного амина, при температуре ледяно бани. Обычно используются эквимолярные количества реагентов с избыточным количеством хлорангидрида (до 10-1ОО%). Как правило на 1 моль кажд го из используемых реагентов использует ся 3 моля третичного амина, преимущест венно триэтиламииа. При введении дополн тельного количества хлорангидрида исполь зуется соответствующее молярное колнчес 1тво амина. « Наиболее предночтител ;ные растворители должны быть i безводными алротонкыми полярными растворителями, такими как диметилформамид или гексаметилформамид. После завершения реакции все получаемые нерастворим 1е вещества «{ ьтруют и продукт осаждают путем добавления фильтрата к больщому объему диэтилового эфира. Сырой продукт отделяют посредством отсасывающей фильтрации и сущки. Суспензию сырого продукта в хлористом метилене освобождают от минимальных количеств исходкого Л -аминоарилметилпенициллина путем добавления небольшого количества триэтил амина, который превращает исходный пенициллин в растворимую в хлористом метилене триэтиламиновую соль. .Чистый продукт затем подвергают фильтрации и сущке. Если X представляет собой NHA.. ,где А и и. имеют указанные значения, обб1ч:но эквимолекулярные количества 3-гуанил-1-уреидоалкановой кислоты, N - гидроксисукцинимида и дициклогексилкарбодиимида плюс избыточное количество указанных двух последних реагентов вплоть до 5О% :контактируют друг с другом.в среде инертного к реакции растворителя, например :упомянутого растворителя, при комнатной температуре. Спустя 1-3 часа промежуточный продукт реакции сложный эфир ii -сукцинимида, образующийся непосредственно ja зоне протекания реакции, подвергают обработке эквимолярным количеством плюс избыточным количеством вплоть до 50% соответствующего оС -аминоарилметилпенициллина, преимущественно в виде его основной соли. Продолжительность реакции 1-6 час в зависимости от температуры, концентрации и реакционной способности используемых реагентов. Продукт реакции отделяют после фильтрации реакционной смеси путем введения полу:чаемо1х фильтрата эгой реакционной смеси в в большой объем диэтиловогок эфира. При необходимости продукт может быть очищен путем использования триэтиламина. Особе нностью кислотных соединений,соответствующих настоящему изобретению, является способность их образовыватьЬсновные соли. Производные кислот превращаются в Лхзновные соли в результате химического взаимодействия указанных кислот с основаниями в водной либо в неводной среде. Основания, используемые при получении упомя нутых основных солей, могут различаться |по своей природе. В качестве таких основа 1НИЙ можно использовать, например, |органй{ческие амины, аммиак, гидроокиси щелочны металлов, карбонаты, бикарбонаты, гидриды и алкоксиды щелочных металлов, а также ;гидроксилы, гидриды, алкоксиды и карбона(ты щелочноземельных металлов. I Соединения, имеющие асимметрический 1-углеродный атом и II -конфигурацию, явля ются более активными, чем соединения, им кшше L -конфигурацию, Прим е.р 1. -2-фенил-2-{3-гуанил-1-уреидоацетамидо)-ац тамидо}шен циллановая кислота. 1А. К суспензии 12,7 г (0,0325 моля) тригидрата- D - Л -аминобензилпенициллина в 200 мл диметилформамида при комнатной : температуре и в атмосфере азота добавля|ют 9,15 мл триэтиламина и полученный в результате раствор охлаждают до О С в ледяной бане. К этой реакционной смеси в течение 2 мин при тщательном перемещивании добав ляют две порции по 3,5 г (О,О325 моля) хлоргйдрата гуанилуреидоацетилхлорида. Смесь перемешивают при О С в течение 5 мин и при комнатной температуре в течение 50 мин. Эту смесь снова охлаждают в ледяной бане и в течение 2 мин добавляют к ней 4,55 мл триэтиламина и дополнительно две порции по 3,5 г хлорангидрида. После перемешивания при в течение 10 мин и при комнатной температуре в течение 1 часа смесь фильтруют и фильтрат добавляют к 3 л диэтилового эфира. Получаемый сырой продукт (19,5 г) суспензируют в 2ОО мл хлорида метилена, содержащего 5 мл триэтиламина, и осуществляют перемеши- вание в течение 2 час. Получаемое веществ представл-яющее собой белый порошок, фильтруют и высушивают, в результате чего получают продукт в количестве 14,0 г (выход 88%). Пики 1К-спектра : (мкм; КВг ) 3,О; 3,3; 5,6; 5,75 - 6,3 ( Ь ) ; 6,3 - 6,75 ;(Ь ); 7,2; 7,6 и 8,1. Пики спектра ЯМР : ;( г. /млн; DMSO-De) 1,5 (tf ); 6Н; 3,9 (с ), :2Н; 4,0 ( S ), 1Н; 5,4 ( с ) ; 2Н; .5,8 (С), 1Н; 7,5 (с), 7Н; 8,4-9,2 (с), 5 Н. Б. К раствору 345 мг (3 ммоля) N -гидроксисукцинимчда и 62О мг (3 ммоля) дициклогексилкар15одиимидав 15 мл высушенного диметилформамида добавляют 587 мг (3 ммоля) хлоргйдрата 3-гулн11Л-1-уреидоуксусной кислоты и эту смесь перемешивают при комнатной темлературе в течение .К смеси добавляют трлэтиламнновую соль I D - (X -аминобенаялпенициллнна в количестве 1,35 мг (3 ммоля) и продолжают пере мешивание еще в течение 3 час. К получе1Г ной реакционной смеси добавляют диэтилформамид (20 мл), после чего осуществляют фильтрацию и чистый фильтрат добавляют к 1,2 л диэтилового эфира. Высущенный белый осадок (947 мг) отделяют посредством фильтрации с отсосом, суспензируют в 50 мл хлористого метилена и обрабатывыют 1 мл триэтиламина. После перемеши|вания в течение 1 часа очищенный продукт собирают и высущивают,:В результате чего получают 537 мг продукта (выход 36,5%). |Этот продукт во всех Ьтношениях идентичен 1продукту,,получаемому по способу с применением хлорангидрида. Пример 2. 6- В-2-фенил-2:-( /i -3-гуанил-1-уреидопропионамидо)аци тамидопенициллановая кислота. ; Хлоргидрат - - (3-гуанил- 1-уреидо) ;пропионовой кислоты в количестве 840 мг (4 ммоля) добавляют к раствору 785 мг (3,8 ммоля) дицнклогексилкарбо.диимида и 44О мг (3,8 ммоля) N -гидрокснсукцинимида в 15 мл высушенного диметилформамида при комнатной температуре и в атмос; фере азота и смесь перемешивают в течение 2 час. Затем добавляют триэтиламиновую соль В - -аминобензилпе1/щиллинп в количестве 1,71 г (3,- ммоля)и эту реак- I ционную смесь перемешивают в течение 1,5 час. Эту смесь фильтруют и фильтрат добавляют к 400 мл диэтилового эфлр.ч. Полученный материал, представляющий собой белый порошок, после очистки с псполь;зованием способа, описанного в примере 1, фильтруют и высушивают, получая 1,4 г конечного продукта (выход 73%). I Пики ИК-спектра: (мкм; КВ) 3,0; (3,35; 5,6 ; ,5,75-6,3 (Ь) ; 6,3-6,8 ( Ь) ; 7,15 ; 7,85 и 8,0. Пики спектра ЯМР : (ч./млн. ; DMSO-Be) i,5(f ),6Н; 2,5 (С ), 3,3 (с ), 4,0 ( 5, 1Н; 5,4 ( с ), 2Н; 5,75 (с ), 1Н; 7,1|7,8 (С), 7Н; 8,3-9,3 (С), 5Н, Пример 3.. -2-(2-тиеиил)-2-(гуаыилуреидоаиетамидо) -ацетамидо пенициллановая кислота. Колбу (150 мл), снабженную отводом для азота, заполняют 3,55 г (0,01 моля) Д оС -амино-2-тиенилметилпеницилли11а, суспензированного в 7О мл сысушеиного диметилформамида и иолученяую суспензию Обрабатывают 3,О6 мл (0,022 молями) триэтиламина. Полученную реакшюннуюсмесь охлаждаютдоО С и обрабатывают 2,35 г (0,011 молями) хлоргйдрата гуанилуреидолцетилхлорида, добавляемого отдельн)1ми ио)ииями B течение 2 мин, Сусггеизию и.-1Греппют до комнатной температуры и оставляют ее при этой температуре в течение ЗО мин, после чего ее обрабатывают дополнительно 1,5 МЛ1 (0,011 молями) триэтиламина, охлажденного до , и; 2,35 г (0,011 молями) xnojp-; 5 ангид1)1ада/д6ёавляемрго ртдель№1мн шля. После перемешивания при О С в течение 1О мии смесь нагревают до комнатной температурьл « оставляют при этой темпера;туре в течение 1-2 час. Небольшое количес-/ о тво нерастворимого продукта отфильтровывают и фильтрат добавляют к 1 л диэтило- вого эфира. Осажденный продукт после перемешивания в течение 30 мин фильтруют и 1 высушивают. Затем его подвергают допол- is нательной очистве с использовешиём хлорис-: тсхго метилена и триэтиламина аналогично примеру 1. ; Пример 4. Используя в качестве исходных продуктов соответствующие Х аминоарилметилпенициллин и хлоргидрат гуанилуреидоалканоилхлорида и применяя обЩий способ, описанный в примере 1, синтезируют пенициллнчы, указанные в табл. 1 и имеющие следующую структурную формулу Afe. - СН- CONH д- хСНз WU I I ГСНз NHJ N J. о NH-C -NH-C -NHa IIII О т Таблица 1
1 Продолжение таблицы 1







| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 6-/ -(имидоиламиноалкиллоиламино)арацициламино -пенициллановых кислот или их солей | 1975 |
|
SU576945A3 |
| Способ получения 6-/ -(аминоаминоалканоиламино)-арациламино/пенициллановых кислот или их солей | 1973 |
|
SU576944A3 |
| Способ получения производных пенициллановой кислоты или их солей | 1976 |
|
SU633482A3 |
| Способ получения 1,1-диоксидов пенициллановой кислоты или ее эфиров или ее солей | 1978 |
|
SU860706A1 |
| Способ получения производных 6-( -2ациламидо-2-фенил-ацетамидо) пеницилановой кислоты или их солей | 1976 |
|
SU622407A3 |
| Способ получения проивзодных пенициллановой кислоты или их солей | 1974 |
|
SU609468A3 |
| Способ получения пенициллиновых производных или их солей | 1974 |
|
SU578888A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНИЦИЛЛИНОВ | 1973 |
|
SU367605A1 |
| Способ получения производных пенициллина или их фармацевтически приемлемых солей (его варианты) | 1979 |
|
SU1151212A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ЦЕФАЛОСПОРАНОВЫХ КИСЛОТ | 1972 |
|
SU343438A1 |

а табл. 1 и в последующих таблицах группа А, ; представляющая собой алкилен, написана так, что I левая связь этой группы присоедина к группе
- С -, а правая - к группе-NH. Пример 5. 6- В-2-фени7г-2г (З-метилгуанил- 1 -уреидоацетами до) -ацетамидо леннциллановая кислота. Суспензию 2,25 г (5 ммолей триэтиламиновой соли D - Л -аминобензилпенициллй на в 25 мл высушенного диметилформамида, поддерживаемую в атмосфере азота, обрабатывают 0,7 мл {5 ммолями) триэтйламина и эту реакционную смесь охлаждают до температуры -30 С. К тщательно перемешанной реакционной смеси в течение 3 мин в виде разделенных порций добавляют хлоргидрат 3-( N -метилгуанил)-1-уреидоацетил хлорида в количестве 2,28 г (О,О1 моля) при температуре ледяной бани. После перемещивания в течение 2 час при температуре ледяной бани ч смесь подвергают фильтрованию при использовании вакуума и фильтрат :добавляют к смеси, состоящей из хлороформа (5ОО мл) и ацетона (5ОО мл). После |перемещивания в течение ночи при комнат- 1ной температуре полученный осадок собирают и высущивают в вакууме, в результате
Таблица 2 чего получают конечный продукт в колнчес1тве 1,5 г с т.пл. 195 С (плавящийся с разложением). Пример 6. Повторяют процедуру, описанную в примере 5, кспользуя в качестве исходных продуктов С -аминоарилметил |пенициллины и соответствующие хлориды ;Гуанилуреидоацетила, получая при этом сле|дующие производные указанных соединений (см. табл. 2). At-CH-CONH. Ss./CHj I pcHj NH -WLpQ,-, NH-C-N-C-N
11
504491
12 Продолжение
таблицы 2 i Пример. Повторяя процедуру, описаин ную в примере 5, используют в качестве исход-: :ных продуктов соответствуюшие DL - (ЗС I -11 t)
I «II /Ха
NH-C-N-C-N/
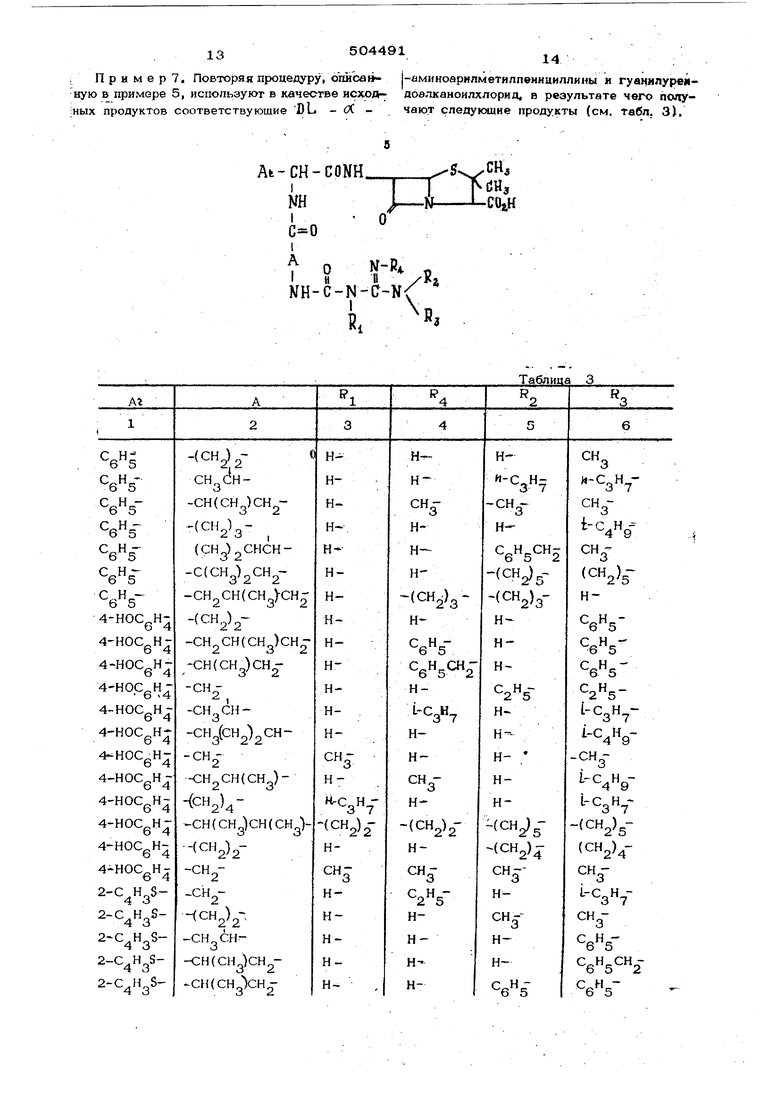
Таблиц {-амнноарнлметилпеннциллины и гуацилуремдоалканоилхлорид, в результате чего получают следующие продукты (см. табл. 31,
Пример 8. -2-фенил-2{3- , - уанил-1-уреидоацетилглицинамидо)-ацетамидсДпенициллановая кислота.
к 175 мл диметилформамида, поддер-т живаемого в атмосфере ааота добавляют 4,3 г (17 ммолей) хлоргидрата 3-гуанил-1-уреидоацетилглицидина, после чего добавляют 2,42 г (21 ммолей) ti -гидроЧ i ксисукцинимида и 4,35 г (21 ммопя)Ы,И дициклогекеилкарбодиимида. Полученную суспензию перемешивают в течение 2,5 час и затем ее фильтруют. К фильтру добавляют триэтиламиновую соль D - -аминобен- зилпенициллина (9,45 г; 21 ммоля), после чего смесь перемешивают при комнатной температуре в течение 2 час. Далее эту смесь фильтруют и фильтрат добавляют по каплям а течёние20 мин к 2,5 л диэтилового эфира. Полученный осадок взбалтывают в течение 20 мин, фильтруют и суспензируют в хлористом метилене, в который добавляют 4,5 мл триэтиламина. Спустя 25 мин: полученный продукт в виде задубленного твердого вещества фильтруют и высушивают в вакууме, получая при этом конечный продукт в количестве 8,Э г. Пики ИЧ-спектра:. (мкмг KBt) 3,О5; 5„в5; 6,04 6,58; 7,2О; 7; 6О и 8,1О. Пики спектра ЯМР ; (ч./млн.; ВаО) 1,3 6Н; 3,85; 6,35 (2Н); 7,32 (5Н).
Продолжение таблицы 3
.д
П р и м е р 9. 6-LD-2-феиил-2-(3-гуанил-1 -уреидоацетилглицидилглицинамидо) -ацетамидо}пениииллановая кислота. ; К раствору 310 мг (1 ммоля) хлоргидрата З-гуанилуреидоацетилглицилглицина в 8мл высушенного диметилформамида в атмосфере азота добавляют 115 мг (1 ммоль) N.-иидроксисукцинимида и затем 206 мг(1 ммоль) N,A/ -дициклогекеилкарбодиимида и полученный раствор перемешивают при комнатной температуре в течение 2 час. К этому раствору за один прием добавляют триэтиламиновую соль -Б - -аминобензилпенициллина (45О мг, 1 ммоль) и смесь дополнительно
перемешивают в течение 3 час. Полученные твердьхе продукты фильтруют, промывают небольшим количеством диметилформамида, фильтрат и промывание воды соединяют и добавляют ПО каплям к 4ОО мл диэтилового эфира. Полученный .осадок фильтруют и :Сусйендируют в хлористом метилене, к которому добавляют шесть капель триэтиламина. После перемешивания в течение 30 мин продукт фильтруют и высушивают в вакууме, .подучая 310 мг целевого продукта. Пики ИК-спектра: (мкм; КВ,) 3,05 ; 5,65; 6,О5; 6,55; 7,2О и 8,1О. Пики спектра ЯМР: (ч./млн.; flWSO-D p) 1,40 (6Н); 3,20-4,1 (Ь); 3,38 (1Н); 5,7 (1Н) и 7,34 (5Н).
.
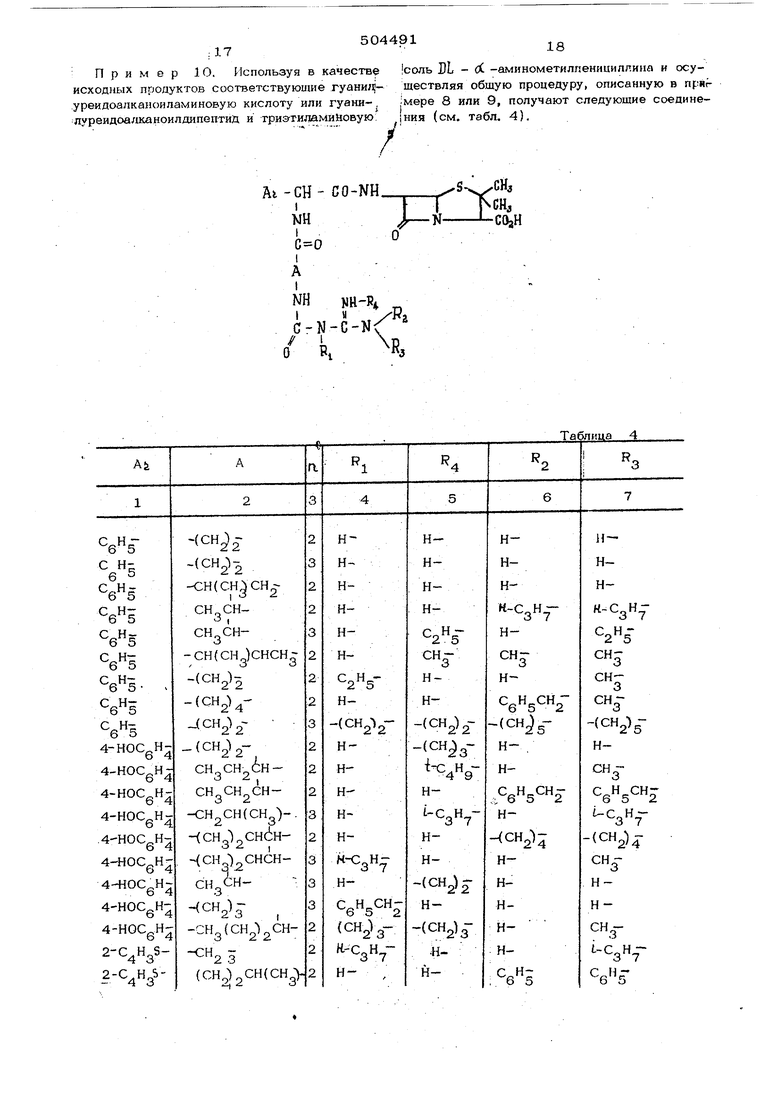
Пример Ю. Используя в качеству соль БЬ - (X -аминометилпенициллниа и осуисходных продуктов соответствующие гуанил -ществляя обшую процедуру, описанную в прнг
уреидоапканоиламиновую кислоту или гуани-.|мере 8 или 9, получают следующие соединелуреидоалканоилдипептиа и гриэтиламиновую|ния (см. табл. 4).
AI -СН- CO-NH.
Ш
I
А NH
NH «i
IЧ /R,
i;-N-c-N ;
0 BI
СНз
Ьсн,
W--СОаН
NH-Ri R,
Таблица 4 Пример 12. Натриевая содь 6-tl -2-фенил-2-(3-гуанил-1-уреидоацета- gQ омидо)-ацетамидо)пенициллановой кислоты. К суспеюии 30 г (0,061 моля) 2-фенил-2-( З-гуанил-1 -уреидоацетамидо) -йцвтамидо пенициллановой кислоты в ЮОмЛ диоксана и 50 мл водь ирлодной) до- 95 ёавляют 5,2 г (О,О61 моля) бикарбоната натрия, растворенного в 75 мл воды. Раствор перемешивают в течение 15 мин, нерастворимые вещества отфильтровывают и фильтрат подвергают сушке при температу- М ре ниже О С. Получаемый твердый продукт суспендируют в 2 л хлороформа, фильтруют и высушивают в вакууме. Получают 29,2 г очищенного продукта (выход 93%). Аналогичным образом получают соответ- 45 ствующие калиевую, кальциевую, магниевую и другие пригодные для фармацевтическоср использования соли 6- D-2-фeнил-2-(3-гy ани л- 1 -уреидоацетамидо) -ацетами до пенициллановой кислоты и упомянутые пеницил- SO Пример 13. Триэтиламиновая соль 6- TD -2-фенил-2-(3-гуанил-1-уреидоацетамидо) -ацетамидо1пенициллановой кислоты.85 Суспензию 2,0 г (3,8 ммолей) 6- D-2-фенил-2-(3-гуанил-1-уреидоацетамидо)-ацетамидо}пенициллановой кислоты в 20 мл воды подвергают обработке 0,5 мл (3,8 ммолями) триэтиламина. Поспе перемешивав 80
Продолжение таблицы 4 ния в течение 5 мин небольшое количество нерастворимых продуктов отфильтровывают и фильтрат высушивают при температуре ниже О С, получая 2,1 г продукта (выход 93%). Аналогичным образом получают аммониевые соли и пригодные для формацевтического использования соли, полученные из органических амишзв описанного neimmfinfia Формула изобретения 1о Способ получения производных пенициллина общей формулы AI-CH-CONH. 1 Г СНз I т c-N-c-jj ; о i. или их солей, где А& фенил, 4-оксифенил, 2-ткенил или 3-тиснил; - алкнлеи, содержащий 1-4 атома углерода ияи нлкмлидеп, содержащий Г - 4 атома углерода; ti - : 1елос; число, равное 1-3; каждый из радикалов R., R , Кг., и 5 J- 2 R - водород или алкил, содержащий 1-4 атома углерода; Р и R,., (совместно) - алкилен, содержаилий 2-4 атома углерода;10 1 и (совмесгно) - алкияен. содержаший 2-4 атома углерода;. R и R,, (совместно) - алкилен, содер Ожащий 4-5 атома углерода; J отличающийся тем, что соединекие обшей формулы Ai-CH-CONH- .--у- pIHj20 NHj - W -СОаН 0 122 1(од1 ергают взаимодействию с саедииением общей формулы XI п fl ц Ц Т, P.J-C - N - С Х елI -Q l . где 1. - R имеют указанные значения, X -радикалы формулы -NH-А - СОС HCI ияи О мНАСо - П - W L где Аи к имеют указанные значения, последующим выделением целевых нродуктов известными способами.
Авторы
Даты
1976-02-25—Публикация
1973-04-19—Подача