(54) СПОСОБ ПОЛУЧЕНИЯ ДИАМИНОБЕНЗОФЕНОНОВ
I
Изобретение относится к способу получения новых, не описанных в литературе, диаминобензофенонов, которые обладают биологической активностью, хара.ктерной для 5 - (3 - диметиламинопропил) - 10,11-днгидро5Н-дибензо- Ь,/ -азепина, фенацетипа и фенобарбитала, и могут найти применение в медицине.
Известен способ получения производных бензофенона общей формулы:
BI
ГА
«
в,
RI бром, йод илн нитрогрунна;
R2 водород или галоид;
Rs низший алкилен;
низший алкил или ннзщий алкиRs лен, при взаимодействии соединения общей формулы:
где R, и R2 имеют вышеуказанные значения, с амином общей формулы:
.R.
X:-Ej
где RS, R4 и RS - Ка.к указано выше;
X - галоид, KOTOipbie обладают биологической активностью.
Предлагаемый способ получения диамикобензофенопов общей формулы:
Шз
4,,0Ил
где RI и R2 - насыщенный н.пи ненасыщенный, разветвленный или неразветвленный алкил или аралкил, насыщенный илн ненасыщенный цнклоалкил илн арнл, нли Ri i Ra вместе с атомом азота образуют замепген ое
или незамещенное гетероциклическое кольцо, икоторое может также содержать атом азота или .кислорода; Rs - водород нли анн, остаток Ci-С 8-1ка1рбонавой кислоты, заключается в том, что соединение обн1ей формулы:
КО г
RI
где RI и R2 имеют вышеуказанные значения, восстанавливают известным методом и полученное вещество выделяют или ацитируют С -Сш-карбоновой -кислотой или ее реакционноспособным .производным с носледую:цим выделением целевого продукта известным способом в свободном ВИде, в виде соли или в виде четвертичной аммониевой соли.
Восстановление обычно ведут в присутствии катализатора, например никеля Реиея, платины или палладия, в среде растворителя, такого, (как бензол, этанол, тетрагидрофуран или этилацетат. Платину и палладий применяют на подложке, которой служит активированный уголь или углекислый кальпий.
Температура 20-50° С, давление в интервале от атмосферного до 5 ат.
Для восстановления можно использовать Непосредственно водород или водород в момент выделения, а также соединения, я)вляющиеся донором водорода, например циклогексен.
Чаще всего для ацилирования используют галоидаигидрид Ci-С18-карбоновой кислоты и осуществляют его в среде инертного растворителя, такого, как ацетон или диоксан.
Ацилирование проводят предпочтительно при 20-50° С в присутствии акцептора кислоты, такого, как неорганические или третичные органические основания, исходный бензофенон, содержащий первичную и трегичную аминогруппы.
Исходные соединения можно получить из З-нитро-4-галоидбензофенона и вторичного амина общей формулы Ri-NH-R2, где Ri и R2 - как указано выще.
Для синтеза солей целевых продуктов используют соляную, бромистоводородную, серную, фосфорную, молочлую, лимонную, винную, малеиновую, фумаровую ашслоты, насыщенные или ненасыщенные короткоцепные алкилгалогениды, алкилсульфаты или бензилгалогениды.
Из солей и четвертичных солей известными способами выделяют свободные основания, которые можно неревести в другие соли или четвертичные соли.
Во всех примерах УФ-спектр снимают в этаноле.
Пример 1. З-Амино-4- (М,М-диизобутиламино) -бензофенон.
В аппарате для гидрирования приготовляют раствор 10,63 г 3-нитро-4-(Ы,М-дииз0бутиламино)-бензофенона в 106 мл этилацетата, вносят 5,3 г никеля .Ренея, гидрируют при атмосферном давлении и комнатной температуре до поглощения расчетного количества водорода (1,5 час, отфильт1ровыВают катализатор, упаривают прозрачный раствор под вакуумом досуха и получают 9,4 г делевого продукта, т. пл. 59-60° С (изопропанол).
Вычислено, %; С 77,73; Н 8,70; N 8,63. CsiHssNsO.
Найдено, %: С 77,68; Н 8,55; N 8,70.
ИК-опактр, 705, 725,795, 855, 1650, 2820, 2880, 2940, 2960, 3380, 3480.
А,д,ате, нм: 251, 315, 368.
Пример 2. 3-Амино-4-(М-этил-М-циклогаксиламино) -бензофенон.
Раствор 7,1 г 3-нитро-4-(М-этил-Ы-циклогексиламино)-бензофенона в смеси бензола и
этилацетата (1:1) гидрируют в присутствии
0,7 г палладия на активированном угле при
комнатной температуре и давлении 3 аг, до
поглопл,ения расчетного количества водорода
f, 1 час), отделяют катализатор, упаривают
фильтрат в вакууме досуха и получают 6,35 з
вещества. После перекристаллизации из изопропанола получают 5,8 г чистого вещества,
т. пл. 106,6-;107,5° С.
Вычислено, %: С 78,22; Н 8,13; N 8,69.
CsiHasNaO.
Найдено, %: С 78,31; П 8,13; N 8,62.
ИК-спектр, сж-ь 710, 730, 880, 1645, 2860. 2940, 3370, 3460. Я, „акс, нм: 224, 252, 326, 367.
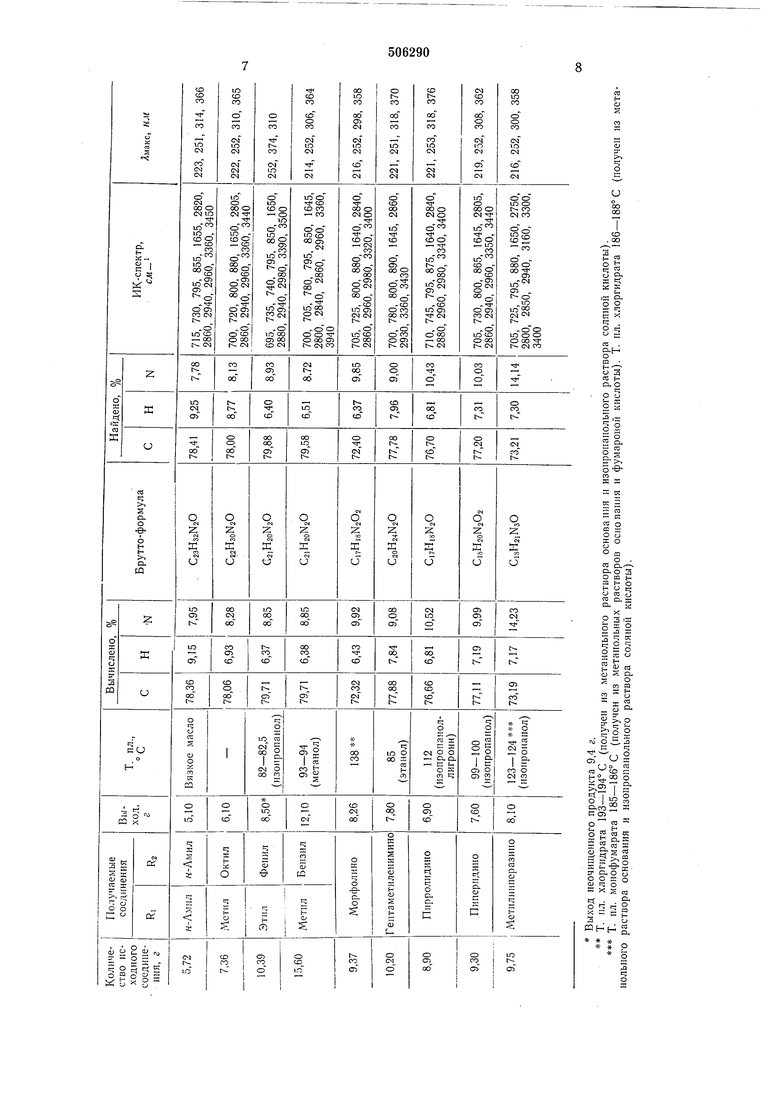
Аналогично примерам 1 и 2 из З-нитро-4N-Ri, N-R2-alMИlHo)-бeнзoфelHoнoв получают 3-а ми1НО-4 - (N - Ri, N-R2 - а.ми«о) - бензофеноны, перечисленные в таблице. П р .и м е р 3. З-А.ми.но-4-пиперидипобензофенон.
2,5 г З-нитро-4-пиперидинобензофенона в смеси 10 мл тетрагидрофурана и 2,5 мл циклогексена и 20 мг металлического палладия кипятят 16 час с обратным холодильником, отф.ильтровывают катализатор, упаривают фильтрат в вакууме досуха и после перекристаллизации из изопропапола получают 1,82 г целевого продукта, т. пл. 99-100° С. .П р и м е р 4. 3-Амино-4-1Пинеридинобензофенон.
В смесь 5,3 г железной пыли .и 25 мл ледяной уксусной кислоты при энергечном перемещивании приливают 6,5 г З-нитро-4-пицеридинобензофенона в 80 мл ледяной уксусной кислоты, выдерживают 2 час пр.и 80-90° С, охлаждают, фильтруют, упаривают фильтрат в вакууме, растворяют остаток в воде, подщелачивают, экстрагируют бензолом, .промывают экстракт водой до нейтральной реакции и сушат над безводным сульфатом магния. Затем фильтруют через колонку с силикагелем, упаривают в вакууме и получают 4,5 г твердого кристаллического продукта (см. таблишу).
Пример 5. 3-Амино-4-1пиперидинобензофенон.
К суспензии iO,.25 г активированного угля
в 10 мл этанола, приготовленной в атмосфере азота, приливают 0,5 мл 0,2 М раствора
5
хлористого пр.лладия, перемешивают 1 мин вводят 1 моль концентрирозаниой соляной кислоты, приливают 1,55 г З-ннтро-4-пипериди.иобензофенона в этаноле и при перемешивании Прикапывают 3,7 мл этанольного раствора боргидрида натрия. Через 10-15 мин отфильтровывают катализатор, приливают к фильтрату избыток водного раствора едкого натра, экстрагируют несколько раз бензолом, сушат экстракты над безводным лоташом, фильтруют и упаривают в вакууме. После перекристаллизации шолучагот 0,98 г целевого продукта, свойства которого указаны в таблице.
Пример 6. Этобромид 3-амино-4-(Ы-метилпиперазино)-бензофено.на.
Смесь 29,5 г 3-амино-4-(Ы-.метилпицеразино)-бензофенона, 300 мл ацетона и 64 г этилбромида кипятят 2 час 1при перемешивании с обратным холодильником, охлаждают, оставляют до утра, фильтруют, промывают кристаллы ацетоном и сушат. Выход 33 г, т. пл. 226-227° С.
(Пример 7. 3-(3,4,5-Триметоксибензоиламино) -4-морфолинобензофенон.
iB раствор 28 г З-амино-4-морфолинобензофенона в 560 мл ацетона вносят 17 г твердого бикарбоната натрия, при интенсивном церемешиеании приливают 25,4 г 3,4,5-триметокСкбензоилхлорида в 260 мл ацетона, .наблюдая повышение температуры на 6-10° С. Перемешивают 0,5 час при комнатной тем;пературе, -выливают в ледяную воду, отфильтровывают осадок, промывают его водой и сушат. После перекристаллизации из смеси ацетон-эфир получают 37,5 г вещества, т. пл. 171-172° С.
6
(Вычислено, %: С 68,06; Н 5,92; N 5,88.
С27Н28Н2Об.
Найдено, %: С 68,11; Н 6,10; N 5,92
ИК-спектр, сл4-: 705, 720, 800, 850, 1135, 1540, 1650, 1670, 3330.
Яиакс , им: 223, 264, 284.
(Пример 8. Хлоргидрат З-пропиониламино-4-морфолинобензофенона.
Раствор 28 г З-амино-4-морфолинобензофенона в 560 мл ацетона смешивают при комнатной телчпературе с раствором 10,2 г пропиопилхлорида в 50 мл ацетона, перемешивают 0,5 час при комнатной температуре, отделяют кристаллы, промывают их эфиром, сушат и получают 34 г целевого веш,ества, т. пл. 152-153 0.
При обработке хлоргидрата едким натром выделяют свободное основание.
Вычислено, %: С 70,98; Н 6,55; N 8,28.
C2oH2aN203.
Найдено, %: С 80,01; Н 6,66; N 8,19.
ИК-спектр, сж-1 : 705, 800, 8809, 1530. 1660, 1690, 3350.
Я-макс, им: 220, 254, 324.
Пример 9. З-Пальмитоиламино-4-морфолинобензофенон. Как в примере 8, из 2,8 г З-амино-4-морфолинобензофенона и 3,02 г хлорангидрида пальмитиновой кислоты получают целевой продукт, т. пл. 70,5-71,5° С.
Вычислено, %: С 76,11; Н 9;29; N 5,38.
СззН48К20з.
Найдено, %: С 76,18; Н 9,31; N 5,42. ИК-спектр, сл4- : 710, 730, 800, 830, 1550, 1650, 1700, 2850, 2930, 3380. А-макс, нм: 256, 324.
3«
§ё
5 л
S i
«
s ex 2 g 5 X
° ч
gШ
5303 fcx о
2i
о 3
3 5-Г§i is.
3 s ,
овco
s s
Ee
«о
Йa:
оо
Xо a
ои
«а
&gg S§
.a
p,V
X
ill
i о i °gs
H S «
U S Cb
S о
m га
CO
s Ш
i l,§
fy о л
o -J 3
S
ai7i
COT о
о S
я Й o. я a g,« ж g
Ic-eg,
s&gi
- 5 g
X ra « йgg5§
3
ШНН
ra Формула изобретения 1. Способ получения диаминобензофенонов общей формулы ь-лО- ЧЗ где RI и Rs-насыщенный или ненасыщенный, разветвленный или неразветвленный алкил или аралкил, насыщенный или ненасыщенный циклоалкил или арил, или Ri и Rg вместе с атомом азота образуют замещенное или незамещенное гетероциклическое кольцо, которое может также содержать атом азота или кислорода; RS - водород или ацильный остаток Ci- С18-кар-боновой кислоты, или их солей, отличающийся тем, что соединение общей формулы ,-О где RI и Rz имеют вышеуказанные значения, восстанавливают известным методом и полученное вещество выделяют или ацилируют С -Ci8-Kap6oHOBoft кислотой или ее реакционноспособным нроизводным с носледующим выделением целевого продукта известным способом в свободном виде или в виде соли, или в виде четвертичной аммониевой соли. 2.Способ ло п. 1, отличающийся тем, что восстановлеЕие ведут водородом в присутствии катализатора, например никеля Ренея, платины или .палладия. 3.Способ по пл. 1 и 2, отличающийся тем, что восстановление проводят в среде растворителя, такого, как бензол, этанол, тетрагидрофура-н или этилацетат. 4.Способ по п. 1, отличающийся тем, что для ацилирования используют галоидангидрид Ci-С18-карбоновой кислоты и осуществляют его в гарисутствии инертного растворителя такого, как ацетон или диоксан.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных индолилуксусной кислоты или их солей | 1971 |
|
SU503517A3 |
| Способ получения производных триптамина или их солей | 1973 |
|
SU523637A3 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИМКАРБАМАТОВ | 1970 |
|
SU280353A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 6-ОКСИПИРИДОНА-2 | 1973 |
|
SU378007A1 |
| Способ получения трициклических соединений | 1973 |
|
SU490287A3 |
| Способ получения гетероциклических соединений или их солей | 1976 |
|
SU613721A3 |
| Способ получения производных пропанаминов или их фармацевтически приемлемых солей с галоидводородными кислотами | 1989 |
|
SU1777598A3 |
| Способ получения аминофенилэтаноламинов или их солей | 1974 |
|
SU518122A3 |
| Способ получения производных норборнана | 1973 |
|
SU497764A3 |
| СПОСОБ ПОЛУЧЕНИЯ НОВЫХ АНАЛОГОВ ПРОСТАГЛАНДИНА F|3 | 1972 |
|
SU349164A1 |


Авторы
Даты
1976-03-05—Публикация
1974-07-25—Подача