.: 1 , - :
Изобретение относится к способу получения новых производных морфолина обшей углы
М-СНд О
N t
RI - водород или арилоксикарбо-
где
|нил, содержащий но более 11 атомов углерода; й - водород или алкил с 1-6 атомами углерода:
4 (одинаковые или различные) - водород, атом галогена, алкил или алкилтиррадикал с 1-6 атомами углерода, ;галоидалкил с 1-3 атомами углерода, ал:коксигруппа с 1-10 атомами углерода, ал.1кенилоксигруппа с числом атомов углерода 1не более 6, ароил, содержащий не более 11 Цтомов углерода, арил или арилоксигрукпа
|с числом атомов углерода не более 1О, ; или их фармацевтически приемлемых солей, обладающих биологической активностью.
. .
При применении известных в органической химии реакций, например алкилирорания аминов, к производным мо{:)фол1ша получают новые соединения, которые обладают ценными свойствами и могут найти применение в медицине в качестве фармацевтических препаратов.
Сущность предложенного способа полу- чения новых производных морфолина обшей фррмулы 1 заключается в том, что соединение общей формулы
Кз
20
()
25
3
.ия, его соль подвергают взаимодействию с. соедшюнием общей форкжулы
,
о
Slf
w
Rj - и имеют указанные значения а - атом галогена, например атом хлора или брома, или алкан- или аренсульфонилоксигруппа, например метансульфовилокси-или толуол- к -сул ьфонилоксигруппа.
Целевой продукт выделяют в виде основания или соли, Б виде рацемата или ( И )или ( S )-изоляера,
В соответствии с описываемым способом можно использовать сояи соединения формулы 2, получаемой взаимодействием
указанного соединения с сильным основанием, например щелочным металлом или
его амидом или гидридом, например гид ридом натрия Реакцию предпочтительно осуществлять в ра бавителе или растворителе, например диметилформамаде, :димё- тилсульфоксиде, диоксане или диметэксиатане, при этом реакция может протекать при повышенных температурах (до 150°С)
Особенно пригодным значением Kj является водород или феноксикарбонилгруппа, а для Яд,- ОДОРЗД метил, этил, 1 пропил или изопропил.
Особенно подходящими значениями Uj , S являются атом водорода, хлора или фтора либо метил, этил, И -пройил, и5опропил, трифторм ил, метилтио-, метокси-, ЭТОКСИ-, Н -пропокси-, изопроПОКСИ-, Н,-бутоксн-, втор,-; бутокси-, Н яентилокси-1 н-гексил-окси-, Н -октилокоя-, аллилокси-, фенокси-, фенилтиоради1 алы, бензоли, фениа. Предпочтительная пруппа соединений формулы 1 включает
PI. R
и,те -из них, у которых
& вадчрод.
Особенно предпочтительными соединениями формулы 1 являются те из них, у которых 1,8, - водород, а Uj - этокси-или феноксигруппа.
Подходящей сетью производного м6 олина-аддукта с кислотой согласно данному йзобрете У ию является, например, хлоргидрат, бромгидрат, фосфат или сульфат, или цитрат, ацетат, оксалат, етансульфонат, толуол- и -сульфонат, татрат, малеат, глюконат или резинат.
Производное мффолина лмеет асимметрический атом углерода, отмеченный цифрой 2 в формуле 1. Такое соединение можно выделять в виде рацемата или двух (оптически активных изомеров.
4
Для .получешш ( и )-или ( S)-изомера соединение формулы 1 может разделяться обычными методами, например дробной кристаллизацией смеси диастереоизомерйой соли - аддукта с кислотой с оптически активной кислотой. При осуществлении указанного процесса можно использовать оптически активное промежуточное соединение формулы 3, которое подвергается
расщеплению обычными методами.
Исходный продукт формулы 3, в которой Й2 - алкил с 1-6 атомами углерода, можно получить, например, взаимодействием аллилглицидилового эфира с алкиламином с последующим ацилированием продукта хлорацетилхлоридом и замыканием в кольцо. В результате получают аллилокси.метил-4-алкш1Морфолйн-5-он. Этот лактам восстанавливают с помошью л1-Я1 Щ , ал-/
лил отщепляется, а получаемый спирт реагирует с хлористым толуол-К,-сулЬфонилом. Пример. Раствор 4,8 г 2-этоксианилина и 10 г 4- Н -пропил-2-толуолfl -сульфонилоксиметилморфолина в 5О мл
ксилолр нагревают с обратным холодильни ;Ком в атмосфере азота в течение 60 час. Смолистое твердое вещество отделяют от растворителя, который перегоняют при пониженном давлении. Остающуюся клейкую
твердую массу промывают серным эфиром, получая желтое твердое вещество. Послед нее кристаллизуют из метанола /серного эфира. Получают толуол- сульфонат 2-(2этокс1ианилин)-метил-4-пропилморфолина с
т.пл. 169-1720С.
4-. Н -пропил-2-толуол- Н -сульфонилоксиметилморфолин, используемый в качестве исходного продукта, готовят следующим образом.
94,7 г аллилглицидилового эфира добавляют при помещивании к раствору 98 г (137 мл) -И -пропиламина в 200 мл этанола. Смесь нагревают с обратным холодильником в течение 18 час, а затем отгоняют растворитель и избыток и -пропила-; мина. Остаточный маслянистый продукт перегоняют, причем выделяется фракция с т. кип. 79-85°С 1 мм рт.ст. - 1-аллилокси3- Н -пропиламин-2-пропанол.
Раствор 95,2 г 1-аллилокси-З- .Н -про;пиламин-2-пропанола в смеси 275 мл беэ водного хлористого метилена и 8О мЛ три- этиламина охлаждают при -5-0°С и по .каплям в течение 2 час добавляют раствор 42 мл хлористого хлорацетила в 60 мл хлористого метилена при помещивании. Смесь нагревают до окружающей температуры { 18-2ОС) и перемешивают при этой температуре в течение 18 час. Раствор
промывают с помошью 2 М соляной кисло5
ты (2 X 100 мл), а затем водой ( 100мл и сушат над сульфатом магния. При уда леиии растворителя при пониженном давлении получают N -Ч З-аллилокси-2-оксипропил)- N - Н -пропил- ОС-хлорацетамид
(119,7 г) в виде маслянистого вещества, используемого без дополнительной очистки ; Раствор 119,7 г N -(З-аллилокси-2оксипропил)- N - Н -пропил- Л -хлор цетамида в метаноле добавляют к раствору метилата натрия, полученного растворением 13 г натрия в 900 мл метанола. Смесь перемешивают и нагревают с обрат;ным холодильником В течение 18 час, а затем растворитель отгоняют. Добавляют 400 мл воды и полученную смесь экстрагируют этилацетатом (1 х 400 мл; ;2 X 200 мл). Объединенные экстракты промывают водой, сушат над Wg S 64 , фильтруют, а фильтрат упаривают. Остаточное масло перегоняют, выделяя при этом фрак:цию с т.кип. 123-125°С/О,7 мм рт.ст. j Получают 2-аллилоксиметил-4- и -пропилморфолин-5-он (65,2 г).
I Раствор 65 г 2аллилоксиметил-4- Н |пропилморфолин-5-она в 100 мл безводного серного эфира медленно добавляют :при перемешивании к суспензии 17,5 г |литийалюминийгидрида в 70О мл безводного серного эфира. Скорость добавления быть такова, чтобы реакционная смесь умеренно вГипела с обратным холодильником. После завершения добавления реакционную смесь перемешивают при окружающей температуре ( 18-2О°С) в течение 18 час, а затем очень осторожно (по каплям) добавляют 9О мл воды для разложения комплекса и избытка литийалюминийгидрида. Эфирный раствор фильтруют и твердый остаток промывают серным эфиром. Ф1 льтрат и эфир после промывки объе;диняют, высушивают над сульфатом натрия фильтруют и из них удаляют серный эфир. : При этом получают 2-аллнлоксиметил-4Н -пропилморфолин в виде масла с т.кип.
80-90°С/1 мм рт.ст., образующий кислый оксалат с т.пл. 125-127°С.
59,7 г 2-аллилоксиметил-4-Н-пропилморфолина нагревают с обратным холодильником в 24О мл 2О%-ной согяной кислоты в течение 18 час. Раствор охлаждают, разбавляют льдом иводоР. превращают в основание с помощью едкого натра и экстрагируют серным эфиром (3 X 200 мл) Эфирный раствор высушивают над Hg 50 ;фильтруют, а затем эфир выпаривают, получая регенерированный исходный продукт. Водный слой концентрируют до небольшого обч-ема. Осажденную соль отфильтровывают и промывают серлым эфиром. Фнльт 6
грат экстрагируют верным эфиром (ЗхЮО мл1 и объед1шенные экстракты и эфир после промывок сушат над Ng 30, фильтруют, а затем эфир испаряют. Получают 2-оксиметил-4-Н -пропилморфолин ( 16,6г) в виде вязкого масла, который после кристаллизации из смеси метанол/эфир -образует кислый оксалат с т.пл. 1331350С.
16,2 г 2-оксиметил-4-Н-пропилмор(фолшА растворяют в 50 мл сухого пиридина и при помешивании по каплям добавляют раствор 21,4 г хлористого толуол Н-сульфонила в 50 мл сухого пиридина. Смесь перемешивают при в течение 3 час. Пиридин удаляют при понижен JHOM давлении, к остатку добаляют 100 мл воды, а продукт экстрагируют простым 1эфиром (3 X 15О мл). Эфирный раствор лромывают водой, сушат над Mg SO , фильтруют, серный эфир выпаривают. В результате получают 30,6 г 4- Н -пропил:2- олуол- Н -сульфонилоксиметилморфолирма в виде масла, которое дает хлоргидрат JC т.пл 172-173°С после перекристалли|зации из метанола/эфира. : Пример 2. Раствор 1,5 г 2-толу|ол- и -сульфонилоксиметилморфолина (полученного обычным способом из его уксусЬо-кислой соли) в 12 мл диметилсульфоксида добавляют к раствору натриевой соли о фенетиднне, полученного из раствора 1 г
о -фенетидина в диметилсульфоксиде при добавлении гидрида натрия (0,3 г, 60%-ная дисперсия) в гтмосфере азота и при помешивании в течение 1 часа. Смесь нагревают при в атмосфере азотгГ в течение 48 час, затем охлаждают, разб :.вляют водой и экстрагируют серным эфкром (3 X 1ОО мл). Эфирный экстракт промывают водой (2 X 5О мл), сушат и эфир выпаривают, получают маслянистое вещест;ВО, которое растворяют в 2 мл метанола, ;вводят в колонку с силикатом магния и рлюируют метанолом. Элюат собирают и метанол выпаривают. Полученный остаток растворяют в серном эфире. Затем осторож|но добавляют эфирный раствор хлористого водорода и получают монохлоргидрат, при перекристаллизации из смеси этанол/эфир получают хлоргидрат 2-( 2-этоксианил1ш)|метилморфолина с т.пл. 179-182°С. i Ацетат 2-толуол-rt-сульфонилоксиме- |тилморфолина, используемый в качестве «сходного продукта, готовят следующим образом.
Раствор 18,75 г 4-бензил-2-толуол-н -сульфонилоксиметилморфолина в 50 мл ледяной уксусной кислоты встряхивают в атмосфере водорода с катализатором ( naii-
л-|днй н,1 угле, О,.П т ..-..ный) до юч пар, пока йе прекрП1Т1л«тг:я лГ5сорбция ппдородл (около 1,1 л). Ката лил vri)p отфипьтрорывают и фильтрчг yiiapHFsaKrr при пониженном давлении, получают бесцветный аирогг, который при добаштеАии отанола отворждается. Кристаллизацией из этанола сюлучают
йиетдт .-толуг)Л-- И,-.ули1иннло1 1 щ .-тяи.мо|)фоли{(а ; т,ш(. . ,
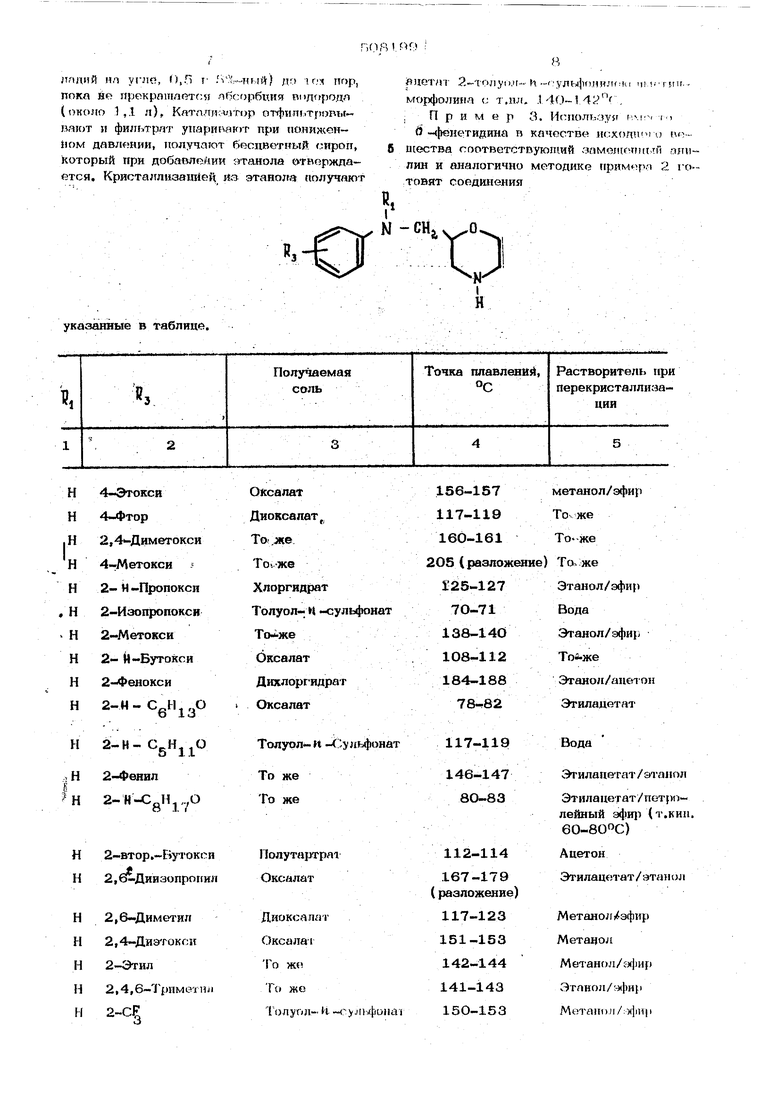
. Пример 3. Ип1юльзу$т RMIV |.,
И |юнетидина в качестве n ::xomii о .., 6 utecTBa соответстйующий зпмолюгпп.ти анилин и аналогично методике примере 2 готовят соединения
N 0
. . ; 11-
держащий не более 11 атомов углерода, арил пли арилоксигруппа, содержащая не более 1О атомов углерода, или их солей,
от л и ч а ю щ и и с я тем, что соединение обшей формулы И
-ft я t -
где KI , Hj, к JI Hj. имеют указанное значение,
ичи его соль подверГают эаик1Одействию с соединением формулы Щ
SO Si 99
12
О
чиХ
,
где B имеет указанное значение, а Zr «. атом галогена, например атом хлора или Чброма, или алкан-или аренйульфонилоксигруппа, натфимер метансупьфонип .окси-или Толуол- и. -сульфонилоксигрупгю, в виде рацемата или С R )-илй ( S )-изомера, с последующим выделением целевого продукта в виде основания или соли, в виде рацемата или ( )-или ( S 1-изоме,ра...,; :: :v V , ..
2. Способ по п. 1, отличающий с я тем, что процесс ведут в ереде разбавителя или растворителя.




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных морфолина | 1974 |
|
SU521844A3 |
| Способ получения производных морфолина | 1973 |
|
SU537627A3 |
| Способ получения производных морфолина | 1971 |
|
SU472506A3 |
| Способ получения производных морфолина | 1973 |
|
SU503521A3 |
| Способ получения производныхморфолина | 1974 |
|
SU509231A3 |
| Способ получения производных морфолина | 1974 |
|
SU508201A3 |
| Способ получения производных 1фенокси-3-амино-пропан-2-ола или их солей | 1974 |
|
SU549078A3 |
| Способ получения 9-(3-амино-1-пропенил) -9,10-дигидро-9,10-этаноантраценов | 1972 |
|
SU472498A3 |
| Способ получения этерифицированных оксибензодигетероциклов или их солей, или рацематов или оптически активных антиподов | 1977 |
|
SU648092A3 |
| Способ получения производных 2-окси-3-аминопропана или их -окисей или солей | 1974 |
|
SU659089A3 |


Авторы
Даты
1976-03-25—Публикация
1974-12-18—Подача