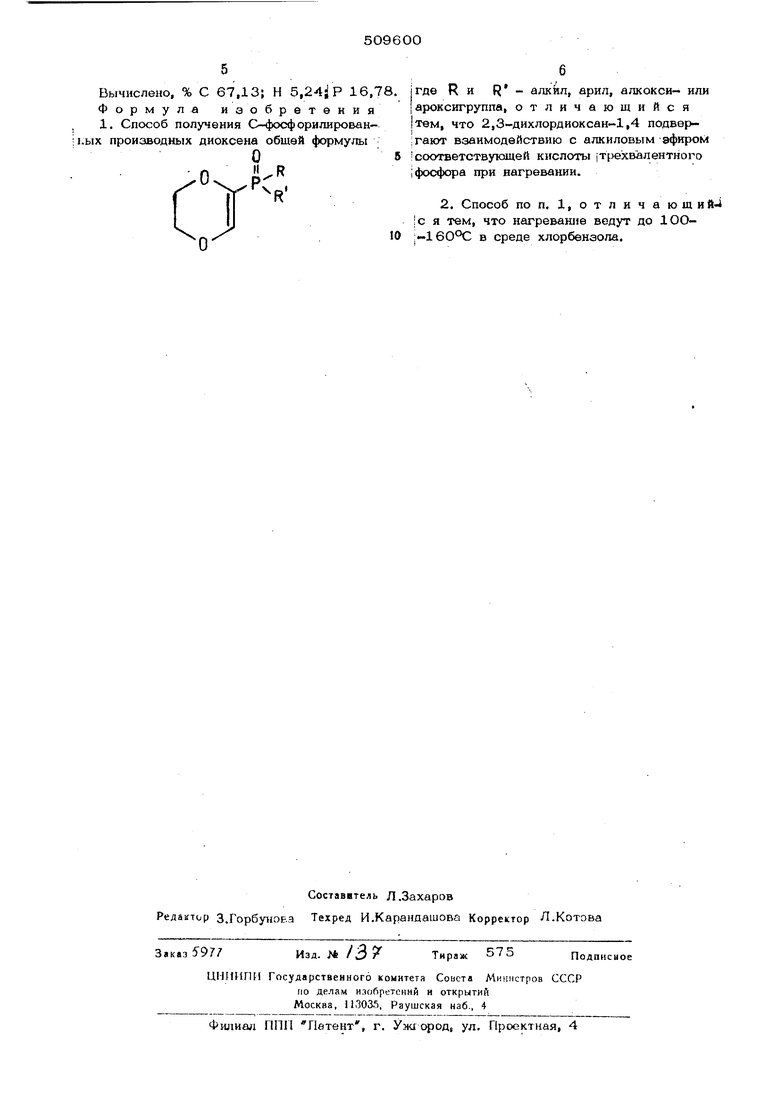
(54) СПОСОБ ПОЛУЧЕНИЯ С ФОСФОРИЛИРСЖАННЫХ ПРОИЗВОДНЫХ . Реакционную смесь выдерживают при температуре смеси 142-145°С, при этом выделяется хлористый эткл После отгонк растворителя в пояучают 5,2 г (3858%) диетилового эфира 2 -парадиоксени фосфокоБой киспотыг т. кип, 120«121-С/ оо-lOO /0,О8 мм рт. от,; а l StSS-- Й . , J) .-4 1,2О82. Найдено, %-. С 43,86 43,24; Н 6,79, 6,725 Р 13,61; 13,88. Вычислено, %: С 43,28, Н 6,89;, Р 13,85. П р и м е р 2. Дибутиловый эфир Iраднохсенипфосфоновой кислоты, В токе углекислоты смешивают 15,9 г ( MOJtt) трибутилфосфита и 12jO г (0,07 моль) 2,3-дихпордиоксайа.1,4. Ре™ ахцконкую смесь нагревают 4,5 час при 145.-14-8 С. Перего5жой получают 4-55 г (25,7%) дибутилоЕОГО эфира 2-парадиоксенилфосфокозой кисдоты, i% кип. 135-137 С /0,2 мм рт. ст., П, 1,4625;; d и4 1Д066. Найдено, %: С 51.96, 51,80 Н 8,32j 8,40; Р 1О,94;. ИДО., S, Вычислено, %: С Н 8„27; Р 11.15. П р и м е р 3, Этиловьгй уфф этил-2,.парапко1:се1шлфосфиновой , кислоты, Смесь 2О,О г (О.ДЗ моль) дкатиловог зфира этилфосфонистой кислоты 25,0 г (0,16 мояь) 2,3-дихлордиок..-1,4 и 20 мл хлорбйнзола кипятят час в токе угпекислоты при 146--149 Со fleperoj-iKOH получают 8,8 г (32Д%) этилового эфира 9П-;л-2--ларадкоксенилфосфиксвой кислоты, т. кип, 124«.125°С/0,07 мм рт, ст., п 2О „ ..„„ j2lO П 1,47685 , Найдено, %: С 46,76;-. 46.70; Н 7,44 7,38; Р 14,76| 15ДО. CgH, Вычислено,-. %: С 46,,60; Н 7,28: Р 15,00. Пример 4. Этиловый эфир п-хлорф , нил-2-парадиоксенилфосфиновой кислоты. В токе углекислоты смешивают 15,7 г (од моль) 2,3 дихлордиоксана 1,4, 20,0 г диэтилового эфира п-хлорфенилфос фонистой кислоты (оде моль) и 25 мл хлорбензола. Реакционную смесь нагревают ДО час при 152.Д54°С, Перегонкой получ ют 7./8 г (31.,6%) этилового эфира п-хлор ф-он;.л-2-Г1а-:)адьоксе11илфосфиново11 кислоты, . кип. 170-172°С/1 1О мм рт. ст., 1,5430; 1,2791. Найдено. %: С 52,60; 52,62; Н 5,7О; 5,61; Р 11,05; 1О,94. - 12«15 зРВычислено, %: С 52,65;:, Н 5,49; Р 10,76. П р и м е р 5. Окись диэтил-2-парад иоксенилфосфина, 8,0 г 10,О6 моль) этилового эфира иэтилфосфинистой кислоты, 10,о г (0,64 моль) 2,3-дихлордиоксана-1,4 и 20 мл хлорбензола смешивают в токе углекислоты в течение 12 час при 115-120°С. Пос ле О1ТОНКИ в вакууме растворителя и непрореагировавших ис.:-дных схэединений остаток перегоняют -в вакууме -и получают 2,2 г (20%) окиси дкэтип-2-парадиоксенилфосфина, т, кип. 114-11б С/10 5 мм рт. ст., 1.444. гг|° 1,4798; Найдено, %: С 5О,38; 50,45; Н 7,78; 7,84; Р 16,23; 16,30. S 15SP Вычислено} %: С 5О,52; Н 7,89; Р 16,32. П р и ; в р 6. Этиловый . эфир фенокси2-парадиоксеиилфосфоновой кислоты. 11,5 г (0,53 моль) диэтилфенилфосфи- те ЮрО г (0,064 моль) 2,3-дихлордиокса на-1;4 i-i 25 мл хлог.)бонзола перемешивают в токе углекислоты в течение 8 час при 144 г.;. После отгонки растворителя и непрореагировавших исходных соединений, и перекристаллизации остатка иэ этанола получают 4,0 г (28эО%) пелевого продукта, т/кип.. 69-70°С. Найдено, %: С 53,30; 53,15; Н 5,60; 5,56: Р 11,60. Вычислено, %; С 55,33; Н 5,56; Р 11,47, П р и ы е р 7. Окись дифенил-2-парадиоксенилфосфина. В токе углекислоты при 142-145 С в « течение 8 час перемешивают 20,0 г {О,087. моль) ртилового эфира дифенилфосфинистой кислоты, 15,0 г (0,095 моль) 2,3-дихлордиоксана-1,4 и 35 мл хлорбензола. После отгонки растворителя и перекристаллизации нз этанола выделяют 4,8 г (2О,5%) окиси дифенил-2-парадиоксенилфосфина. Найдено,%: с 66,9О; 07,02; Н 5,18; 5,15; Р 16,08; 16,32.. ibb 56 Вычислено, % С 67,13; Н 5,24|| Р 16,78.|где R и R - алкил, арил, алкокси- или Формула иаобретения|ароксигруппа, отличающийся 1. Способ получения С-фосфорилирован-|твм, что 2,3-дихлордиоксан-1,4 подверix производных диоксена обшей формулы;гают взаимодействию с алкиловым эфиром О5i соответствующе и кислоты (Трехвалентного ;фосфора при нагревании. 2. Способ по п. 1, отличаюший-i с я тем, что нагревание ведут до 1ОО10 : 160°С в среде хлорбензола.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ а.гДИЗАМЕЩЕННЫХ а-КАРБЭТОКСИ-б-ОКСИ-у- | 1972 |
|
SU332083A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКЙЛОВЫХ ЭФИРОВ 3-АЛКИЛ-2,3,4,5-ДИЭПОКСИ-6-ХЛОРГЕКСАНОВЫХ КИСЛОТ | 1972 |
|
SU340660A1 |
| Способ получения 2,6-диэтинилпиперазинов | 1973 |
|
SU492518A1 |
| СПОСОБ ПОЛУЧЕНИЯ КРЕМНИЙСОДЕРЖАЩИХ ОКСИМЕТИЛФОСФИНАТОВ | 1966 |
|
SU183207A1 |
| Способ получения основных простых эфиров енолов или их солей | 1977 |
|
SU639444A3 |
| Способ получения алкиловых эфиров арилалкилфосфинистых кислот | 1974 |
|
SU496283A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ А'-' -БУТЕНОЛИДОВ | 1970 |
|
SU282312A1 |
| Способ получения дихлор-или дибромангидридов фосфоновых кислот | 1974 |
|
SU487083A1 |
| Способ получения 4-(4-бифенилил)бутанолов | 1972 |
|
SU444358A1 |
| Аллиловые эфиры замещенной -оксиакриловой кислоты для получения химически стойких, малохрупких, прозрачных высокомолекулярных соединений | 1975 |
|
SU570596A1 |


Авторы
Даты
1976-04-05—Публикация
1974-06-18—Подача