MaKCHNiyMa пси .юиюния в оодасгях 268 275 им и 33U-347 им. В ИМР-споктрах сигналы метиленовых групп остатка алкамо- вой кислоты сдвинуты в слабые поля, что ггодтво)жлает в;п1янио па них акцеглюр- ных rpyiuinpODOK: карОоксильпой и 4-карбок- сихинолииовой. Аналогичное влияние последней группировки испытывает -метильпая группа индольного ядра (в случае N -ме тилинлолов), Ч1Х) доказывает введение хинолинового остатК в положение 3 индольного ядра. Потенциометрическое титрование полученных кислот обнаруживает две различные по киспотности карбоксильные группы (,5-5,8 и 7,9-8,2).
Пример 1. 2(.ormn-3}-4 -карбоксихилолинил-3 J -уксусная кислота. Смесь 0,54 г (0,ОО25 моль) 3-(индолил-3 )пропионовой кислоты и 0,37 г (О,О025 моль) изатина в 15 мл 33%-ного водного раствора едкого натра кипятят 50 час, затем охлаждают, разбавляют водо и фильтруют. Фильтрат подкисляют 25%-ной уксусной кислотой. Выпавший через несколь ко часов желтый осадок отфильтровьшаюгт, промывают спиртом и кристаллизуют из большого объема спирта. Получают 2-(индолил-3 )-4-карбоксихинолинил-3 уксусную кислоту. Выход 0,49 г (57% от теории), т.пл. 286-287°С (из этанола). УФ-спектр (в 1О ь-номМс|ОН ): А нм ( ) 271 (4,21), 340 (3,86). ПМР-спектр в СЬрООН,§м.д.: 4,ЗО (CHj); дублет 7,78 (2-Н-индола); дублет 9,9О ( WH индола); мультиплет 7,40 (про тоны бензольного кольца индола); мультиплет 8,10 (хинолиновые протоны). I. (здес и далее в системе: изопропиловый спирт-ам миак-вода, 8:1:1, силуфол) О,32. ,5 ,1. Найдено, %: С 68,9; Н 4,0. ЧоНцМг,0. Вычислено, %: С 69,4; Н 4,0. Пример 2. 2-(2-Метилиндолил-3 -4-карбоксихинолинил-З уксусная кислота. По примеру 1 из 0,58 г (0,0025 моль 3- 2-метилиндолил-3J пропионовой кислоты и О,37 г (О,ОО25 моль) изатина получают 2-(2-метилиндолилгЗ)-4-карбоксихинолинил-З уксусную кислоту. Выход 0,48 г (53% от теории), т.пл. 321-322 С (разл. из этанола).
УФ-спектр (в 1О%-номМаОН)Л,д. нм
(об-): 275 (4,10), 331 (3,62).
ПМР-спектр с , S м.д.; синглет .2,56 (), синглет 10,43 (N Н), синглет 4,33 (CHj), мультиплет 7,13 (протоны бензольного кольца индола), мультиплет 8,10
1хи1юли1ювыс протошл). pKfjj 5,5; рКц.ВД; 1 f 0,36.
Найдено, %: С 69,6; И 4,7.
CsiHibWaOt.
Вычислено, %: С 70,0; Н 4,4.
Пример 3. 2-(1-Метилиндолил-3 )-4-карбоксихинолинил-3 | уксусная кислота.
По примеру 1 из 0,58 г (0,О025 моль) 3-{1-метилиндолил-3)-пропионовой кислоты и 0,37 г {О,О025 моль) и пат и на получают 2-(1-метилиндолил-3 )-4-карбоксихиполини7(-З уксусную кислоту. Выход 0,495 г {55% от теории), т.пл. 283-284 С (разл., из этанола).
УФ-спектр (в 10%-номМаОН )
макс.
Ig
(-CqP): 268 (4,33), 347 (4,О8).
ffрия), т.пл. С (из этанола).
УФ-спектр (в 1О%-номМаОН) Лнм
S5
макс
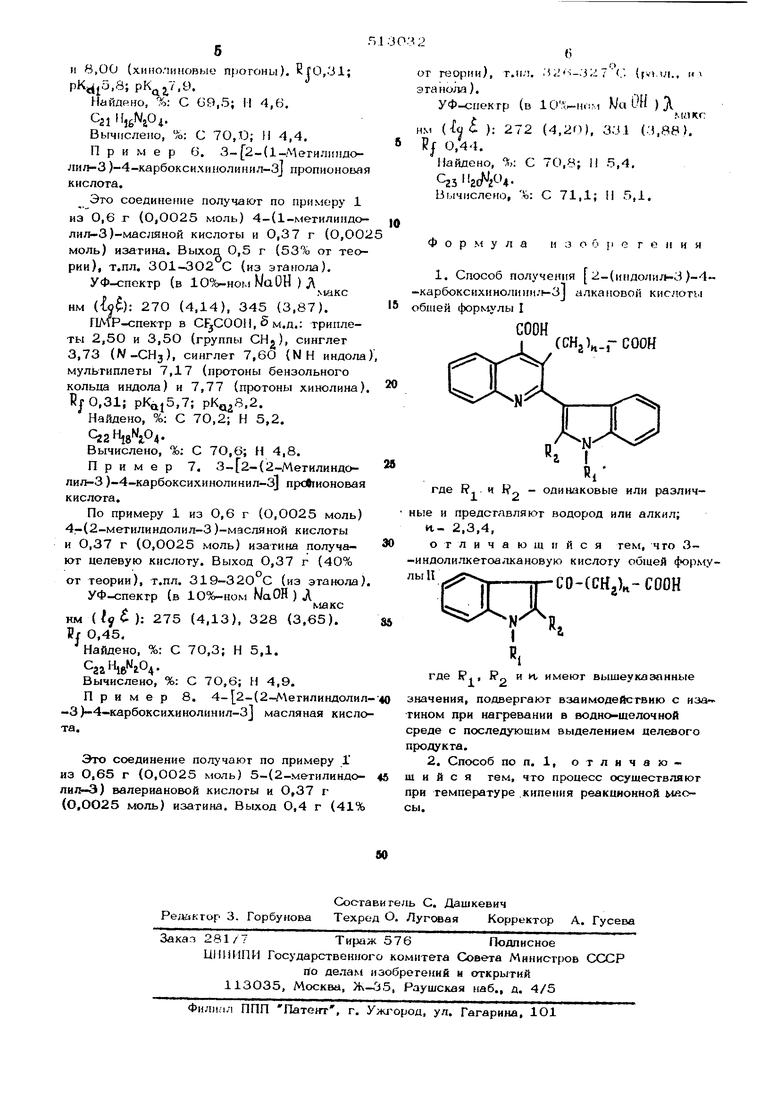
): 271 (4,29), 335 (3,86). ПМР-спектр Е CFjCOOH, 5 М.Д.: триплеты 2,53 я 3,53 (группы СН), дублеты 7,83 (2-Н-индола) и 9,83 (NH), мультиплеты 7,33 (протоны бензольного кольца индола) ММР-спектр в CPjCOOH, & М.Д.: синглет 3,85 (N-CHj), синглет 4,33 (СН), синглет 7,77 (2-И-индола), мультиплет 7,37 (протоны бензольного кольца индола), мультиплет 8,10 ( хинолина). Rf 0,36; рКд15,4; рКд2.7,94. Найдено, %: С 69,7; Н 4,6. ,. Вычислено, %: С 7О,О; Н 4,4. Пример 4. 2-(1,2-Диметилиндолил-3 )-4-карбоксихинолинил-3j уксусная кислота. Это соединение получают по примеру 1 из 0,59 г (0,О025 моль) 3-(1,2-диметилиндолил-3) пропионовой кислоты и 0,37 г (0,0025 моль) изатина. Выход 0,5 г (53% от теории), т.пл. 289-29О -С (из этанола). УФ-спектр (в 10%-номМаОН) Лнм (ij): 279 (4,16), 340 (3,72). ПМР-спектр в CFjCOOH, 5м.д.: синглет 3,67 (W-CHj), синглет 2,35 (2-СНз), синглет 4,23 (СН), мультиплет 7,13 (протоны бензольного кольца индола), мультиплет 8,1О (протоны хинолина). Иг О,37; pKQi5,6; pKjja8,2. Найдено, %: С 7О,2; Н 4,9. CsaHieNjO. Вычислено, %: С 70,6; Н 4,8. Пример 5. (Индолил-3)-4-карбоксихинолинил-З пропионовая кислота. По примеру 1 из 0,58 г (О,О025 моль) 4-(индолил-3)-масляной кислоты и 0,37 г (0,О025 моль) изатина получают (индолил-3 )-4-карбоксихинолинил-3 пропионовую кислоту. Выход 0,4 г (45% от теои в,ОО (хинолиновые прогоны). В|0,.31; .S; ,9. Найдено, %: С 69,5; I 4,6. Са Я,ЛО Вычислено, %: С 70,0; II 4,4. Пример 6, (1-Мегил1пшолил-3)-4-карбоксих 1нолинил-3| пропнонова кислога. Это соединение получают по примеру 1 из 0,6 г (О,0025 моль) 4-(1-мегилипдо лил-3)-мас;шной кислоты и 0,37 г (0,О0 моль) изатина. Выход 0,5 г (53% от тео рии), т.пл. 301-ЗО2 С (из этанола). УФ-спектр (в 10%-ном WaOH ) Л макс нм (io): 270 (4,14), 345 (3,87). Г1Л Р-спектр в С1 С0011,2м.д.: триплеты 2,5О и 3,50 (группы СН), синглег 3,73 (W-СНз), синглет 7,60 (N Н индола мультиплеты 7,17 (протоны бензольного кольца индола) и 7,77 (протоны хинолина ВгО,31; pKaj5,7; .2. Найдено, %: С 70,2; Н 5,2. . Вычислено, %; С 7О,6; Н 4,8. Пример 7. (2-Мет и ли идолил-3 )-4-карбоксихинолинил-3 прсЛтионова кислога. По примеру 1 из 0,6 г (0,0025 моль 4-(2-метил индол и л-3 )-масляной кислоты и 0,37 г (О,ОО25 моль) изатина получают целевую кислоту. Выход 0,37 г (40% от теории), т.пл. 319-320 С (из этанола УФ-спектр (в 1О%-ном WaOH ) Л макс нм (): 275 (4,13), 328 (3,65). Ь 0,45. Найдено, %: С 70,3; Н 5,1. Вычислено, %: С 70,6; Н 4,9. Пример 8. (2-А етилиндоли -3)-4-карбоксихинолинил-З масляная кисл та. Это соединение получают по примеру 1 из О,65 г (О,ОО25 моль) 5-(2-метилиндо лил-Э) валериановой кислоты и 0,37 г (О,ОО25 моль) изатина. Выход О,4 г (41 Т геории), т.пл. ..327 ;. (rv,ui., н танола).. УФ-спектр (в 10:;; -F г..1 К/а UH ) Д м;.. м ( ): 272 (4,20), 331 (3,88). Pj- 0,44. Найдено, %: С 70,8; И 5,4, (. BI ЧиcлeF{o, %: С 71,1; 11 5,1. Формула и ;з о О fi G г е Н к я 1. Способ получения 2-(индоли н-3 )-4карбоксихиноли)П1;(-3 алкановой кислоты бшей формулы I (CHj).,-СООН где R. и „ - одинаковые или различе и представляют водород или алкил; Н- 2,3,4, отличающийся тем, что 3ндолилкетоалкановую кислоту общей форму1Г 5-..-СО-(СНг)к- соон где Р , и и, имеют вышеуказанные ачения, подвергают взаимодействию с иза ном при нагревании в воднс шелочной еде с последующим выделением целевого одукта. 2. Способ по п. 1, отличаюийся тем, что процесс осуществляют и температуре кипения реакционной Мйо.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения амидов 1,2,3,4,6,7,12,12 @ -октагидроиндоло(2,3- @ )-хинолизин-1-ил-алканкарбоновых кислот или их физиологически совместимых солей присоединения кислот | 1985 |
|
SU1470193A3 |
| СПОСОБ ПОЛУЧЕНИЯ 3-АЛКИЛИРОВАННОГО ИНДОЛА И (2-НИТРОФЕНИЛ)-АЦЕТАЛЬДЕГИД | 1991 |
|
RU2054417C1 |
| Способ получения хлорацетамидометилиндолов | 1978 |
|
SU697507A1 |
| Способ получения производных индола | 1983 |
|
SU1081162A1 |
| Способ получения 2-ацилиндол-3карбоновых кислот | 1977 |
|
SU696016A1 |
| Галоидпроизводные триптицендиола-2,5 в качестве мономеров для получения поликонденсационных полимеров | 1983 |
|
SU1180367A1 |
| Способ получения алкиларилзамещенных 1,2,4-триазолов | 1984 |
|
SU1237663A1 |
| Спиропираны 2-оксаинданового ряда, проявляющие фотохромные свойства, и способ их получения | 1974 |
|
SU518491A1 |
| Способ получения замещенных 1,3,4,9-тетрагидропирано [3,4- @ ]индол-1-уксусных кислот или их фармацевтически приемлемых солей | 1987 |
|
SU1531856A3 |
| Способ получения производных бензиламина или их солей | 1973 |
|
SU571188A3 |


Авторы
Даты
1976-05-05—Публикация
1974-12-19—Подача