(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,4-БЕНЗОЛДИСУЛЬФАМИДА
на, при 20-ШО°С с последующим вьщелешем целевого продукта как такового шш переводом его
в оксисоеш1нение извесшьтш приемами.
Реакцию проводят в присутств1ш избытка исход«01О или эквивалентного количества третичного амина для удаления хлористого водорода, образующегося в процессе реакции- Реакцию проводят в течение 1-24 час при 20°С или при повышенной температуре 30-100°С в течение 1-8 час. Продукт можяо выделять простым добавлением реакционной смеси к нормальному раствору соляной кислоты, фильтрованием, промьшанием и перекристаллизацией из подходящего растворителя.
В качестве солей полученных соединений используют соли с фармацевтически приемлемым катионом, которыми являются катионы щелочных металлов, предпочтительно натрия и калия. Эти соли легко получают известны.ми способами. Например, соеданение формулы I растворяют в водном или спиртовом растворе гидроокиси щелочного металла, например гидроокиси калия или натрия, и полученный раствор концентрируют простыми способами.
Описанные соединения можно вводить в больной организм пероральным или парентеральным нутем. Значительный эффект в отношении увеличения кровопотока в €.зсуды мозга у кощек, собак и обезьян породы бабуинов достигается при дозировке 2,5- 25 мг/кг внутривенно или 10-50мг/кг нерорально в течение трех раз в день, причем действие этих соединений является кумулятивным. Хотя точная доза для лечения людей определяется врачом, в общем дозировка для внутривенпого введения составляет 0,5-100 мг/кг, а для перорального введения - 2-200 мг/кг, причем введение каждой дозы проводят 4 раза в день.
Соединения можно вводить в организм в чистом виде, но в общем их вводят в смеси с фармацевтически приемлемым носителем, выбираемым в зависимости от путей введеш я и обычной практикой, принятой в фармацевтике.
П р и м е р 1. 1 - Хлор - 4 - (4 - метоксипиперидиносульфонил) - бензолсульфамид.
Триэтила1.1ин (4,2 мл) и 4 - метоксипиперидин (3,15 г) добавляют к раствору 3 - хлор - 4 сульфамоилбензолсульфохлорида (8,7 г) в ацетоне (100 мл). Смесь перемешивают при комнатной тем-. пературе в течение } часа, а затем выливают в 50 мл 1 н. раствора соляной кислоты. Полученный продукт удаляют фильтрованием, промьшают водой и перекристаллизовываютиз изопропанола. Получают целевой продукт (8,4 г) с т.пл. 165 167°С.
Найдено, С 39,16; Н4,93; N7,53.
С) jHivCINjOsS.
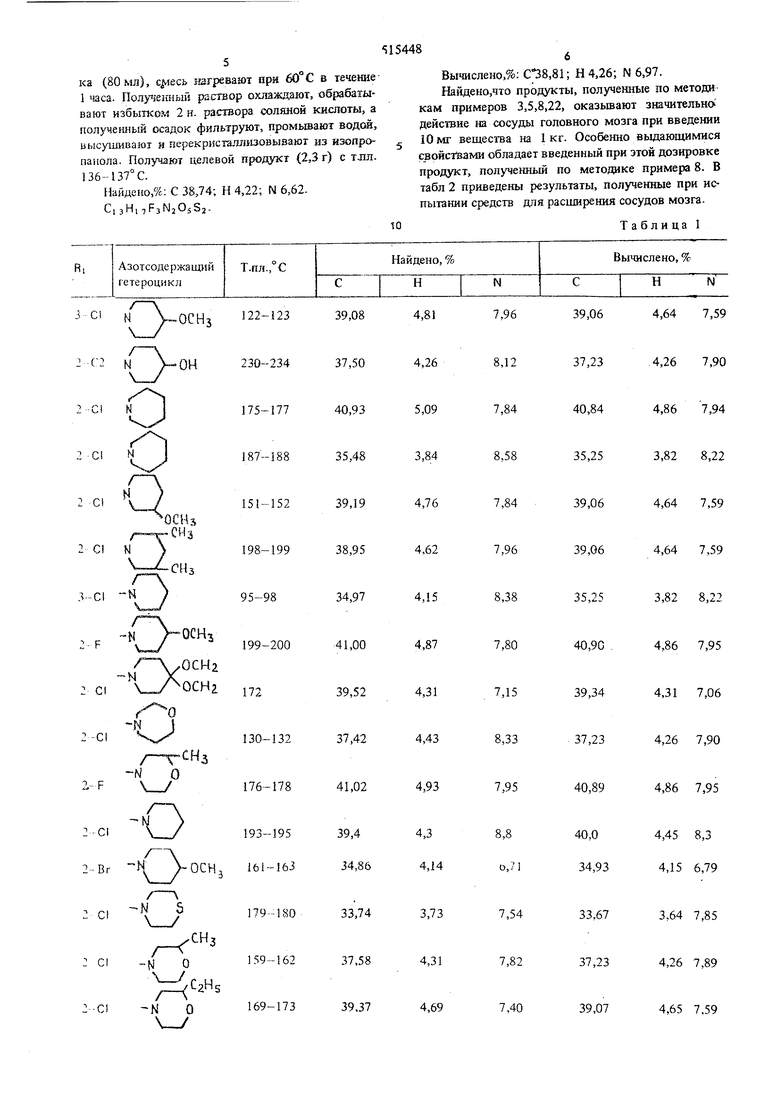
ВычисленоД: С 39,06; Н 5,64; М 7,59П р и м е р ы 2 22. Получают соединевчя, приведенные в табл.Ь по методике, описанной в примере I, с применением в качестве исходных соединений подходящего циклического амина и замещенного 4 - сульфамоилбензолсульфохлорида.
Соединения таб.гшцы имеют формулу
BGj- N
гетероцикл
П р и м е р 23. 2 - Х.пор - 4 - (4 оксопиперидиносульфон:«л) - бе 13олсульфа№1д.
Раствор продукта, полученного по методике, описанной в примере II (1,2 г) в 30 % но .м водном растворе ддметилформамида (50 мл) и концентрировашюй соляной кислоте (1,5мл) перемешивают при кипячении с обратным холодил ;инком в течение 1 часа. Смесь упаривают до небольшего объема, ползченный осадок отфильтровывают н получают целевой продукт (500мг) с т.пл. 195-196°С.
№йдено,%: С 37,33; И 3,82; N 7,96.
CiiHisCiNjOsSj.
Вытаслено,%: С 37,50; И 3,69; М 7,62. Пример 24. 3 - Трифторметил - 4 - (4 метоксипиперида1нсульфонил) - бе золсульфаг/и д.
А. Триэтиламин (1,0 г) и 4 - метоксипнперидан
(1,15 г) добавляют к раствору 4 - иитро - 2 трифторметилбензолсульфохлорида (2,89 г) в дихлорметане (40 мл)- Смесь перемешивают при 25С в течение 2 час, а затем аиривают досуха под
вакуумом. Остаточное масло растирают с водным изопропаноло-м (1:1), и получегшое твердое вещество перекристаллизовывают из изопронанолаПолучают 1 - (4 - метоксипи 1еридиносульфон ил) 4 - 1штро - 3 - трифторметилбензол с т.
пл. 141-143С.
Б. Продукт, полученный но методике А (13,5 г), растворяют в метаноле (200 мл) и гидрируют под давлением (3,5 кг/см) и при температуре 50° С в присутствии 5 % палладированного угля
(1,0 г). Получают 4 - (4 - метоксипмперидиносульфонил) - 3 - трифторметилатшлин (8,9 г) с
т.пл. 145-157° С (после перекристаллизации из изопропанола).
В. Раствор хлорида диазо шя из продукта, приготовленного по методике Б, получают добавлением раствора ттатрита натрия (1,73 г) е во.де (15 Nra) к 8,4 г, приготовленному по методике Б, в концешрированной. соляной
кислоте (60 мл), добавляют при 25°С к суспензии дипедрата хлорной меди (2,2 г) в уксзсной кислоте (80мл), предварительно насыщенной двуокисью серы. Смесь перемешивают в тече1ше часа, а получегшый осадок отфильтровьшают, промьшают
водой, высупшвают и перекристашгазоььтают из смеси ацетона с гексаком. Получают 4 - (4 метоксш1шеридиносульфо1-шл) - 3 - трифторметилбензолсульфохлорид (5 г) с т.пл. 117-1)9° С.
Г. Продукт (4,5 г), полученньгй по методике В,
добавляют к кощентрированному раствору аммиака (80мл), тг вгчот прн 60°С в течеш1е1 часа. Г1олу 5енньш раствор охлаждают, обрабатывают избьшсом 2 н. раствора соляной кислоты, а получеш1ый осадок фильтруют, промывают водой, высуишваю н нерекристаллюовывают из изопропаиола. Получают целевой продукт (2,3 г) с тлл. 1 36--137° С.
ИайдеиоД: С 38,74; Н 4,22; N 6,62.
CiaHnFjN OsSzВычислено,: Ct38,81; Н 4,26; N 6,97.
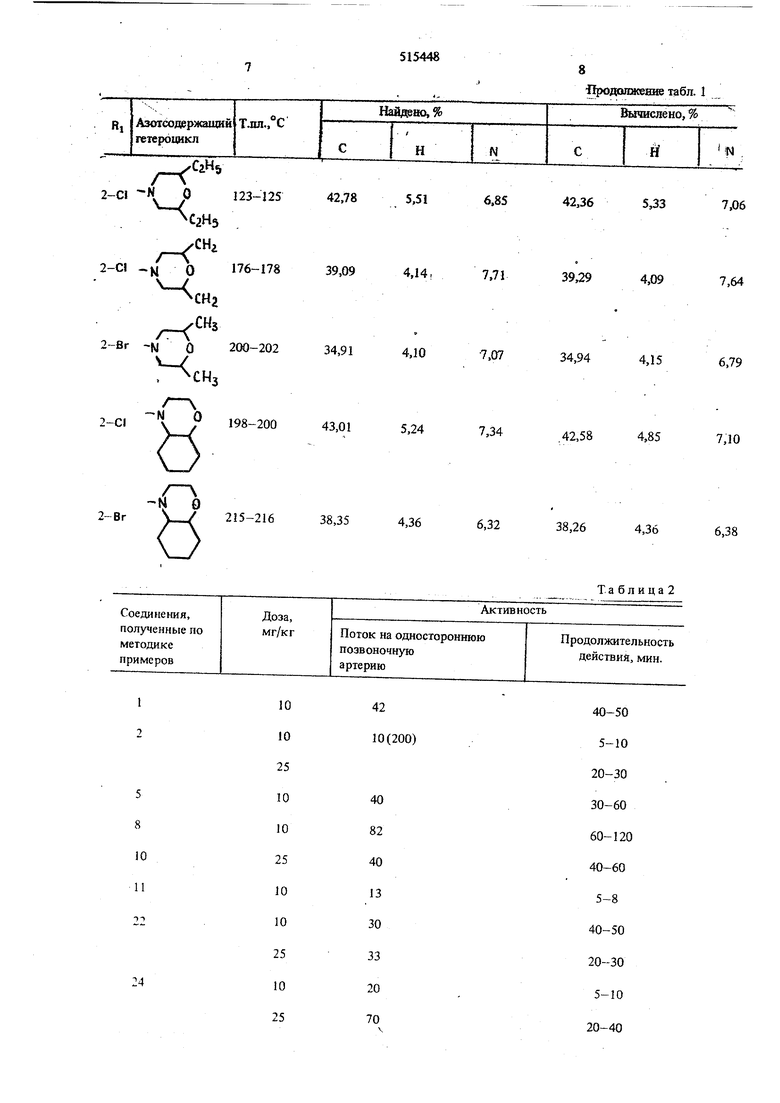
Найдено,что продукты, полученные по метода кам примеров 3,5,8,22, оказьшают значительно действие на сосуды головного мозга при введении 10мг вещества на 1кг. Особенно выдающимися cBoftctBaMH обладает введенный при этой дозировке продукт, полученный по методике примера 8. В табл 2 приведены результаты, полученные при испытании средств для расширения сосудов мозга.
Таблица 1
Продолжешю табл. 1


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения анилинового производного или его фармацевтически приемлемой соли | 1982 |
|
SU1316560A3 |
| Способ получения производных пиридазина | 1982 |
|
SU1356960A3 |
| Способ получения производных 4-амино-2-пиперидинхиназолина или их солей | 1980 |
|
SU953982A3 |
| Способ получения производных алкилендиамина,их смесей,рацематов или солей | 1982 |
|
SU1246890A3 |
| Способ получения циклоалифатических кетоаминов или их солей | 1980 |
|
SU984404A3 |
| Способ получения простых пиридин-2-эфиров или пиридин-2-тиоэфиров, или их кислотно-аддитивных солей, или пиридин-N-оксидов (его варианты) | 1984 |
|
SU1417796A3 |
| Способ получения производных флавана или их солей | 1979 |
|
SU1072805A3 |
| Способ получения гетероциклозамещенных толунитрилов или их фармацевтических приемлемых солей | 1987 |
|
SU1470184A3 |
| Способ получения производных 2-окси-3-аминопропана или их -окисей или солей | 1974 |
|
SU659089A3 |
| Способ получения производных пиридо (3,2- )пиримидина | 1973 |
|
SU515450A3 |

2-Вг м О200-202
34,91
сн. 2-CI 1 9 198-20043,015,24 5 ... -14 О 215-21638,35
34,94
4,15
6,79
Таблица2 7,34 .42,584,85 Формула изобретения Способ полуадния производных 1,4 - бензалда сульфамида общей формулы I /(CHiU. SO,NXi H N-OjS Н2)„ RI - фтор, хлор, бром или трифторметил; Х- метиленовьш радикал, кислород, сера или| о простая связь группами (CHj) и СН2)п; У-0-2; m - 2-3; п - 2-3; Rj - гидроксил, низшая алкокси - или 15 низшая алкилендаоксигрутша, если X - метиловый радикал ияи- простая связь, причем атом кислорода в радикале Rj отделен от атома азота гетероциклического кольца даумя или более атомал-ш углерода, или Rj обозначает низшую алкильную или низшую алкиленоную группу, если X - кислород или сера. 20 отличающийся тем, что 4- сульфамоил бензоЛсульфохлорид формулы П/1 HiN- где RI имеет указанное значение, подвергают взаимодействию с циклическим амином формулы Ш где Rj, m , n, у имеют указанные значения, в среде органического растворителя, например ацетона, при 20-100° С с последующим выделением елевого продукта кактакового или переводом его в оксисоединение известными приемами.
Авторы
Даты
1976-05-25—Публикация
1973-08-29—Подача