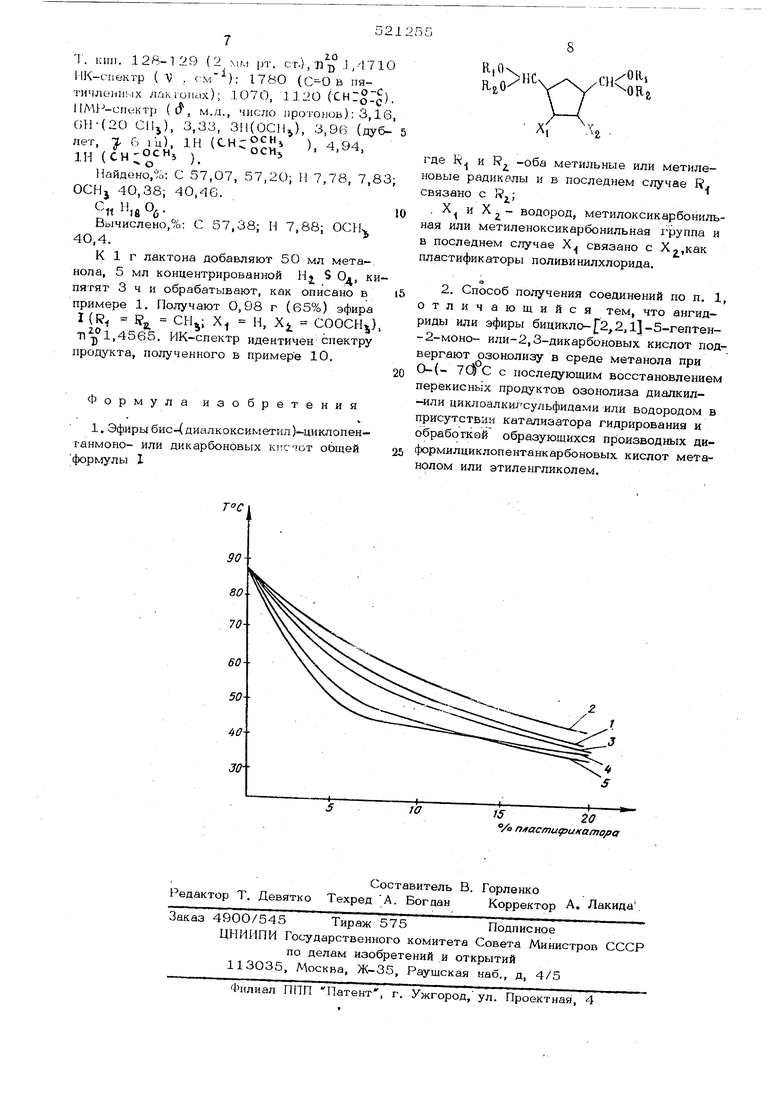
суг весового содерполивинилхлоридажания пластификатора. Кривые даны для следующих вешеств: 1 - диметиловый эфир 1,3-циклопентандикарбоювой кислоты; - тетраметиловый эфир 1,2,3,4-цикпопентантетракарбоновой кислоты; 3- диметиловый эфир 3,4-бис-{диметоксиметил) -1,2-циклопентандикарбоновой кислоты; 4- 9,10-бис-(1,3-диокса-2-циклопентил)-3,6-диоксабицикло- б,3,03-ундекан-2,7-Дион; 5- метиловый эфир 2,4-бис-(диметоксиметил)-циклопентанкарбоновой кислоты. Пластификатор вводят по методу Воскресенского при механическом перемешивании ПОЛНЕЙнилхлорида с соответствующим количеством пластификатора (5,10 и 2О% от веса полимера). Смесь выдерживают в течение 1 ч при 10О С до полного поглощения пластификатора. Прессованием под давлением 30 кг/см и обжигом при 90 С в течение 20- мин изготавливают таблетки размером 6x1,5 мм.. Термомеханические испытания проводят на динамометрических весах В. А. Каргина при нагрузках Ю кг/мм , времени действия 1,5 ч и скорости нагрева 90 С Б час. Результаты термомеханических испыта ний показывают, что предложенные соединения превосходят по своим пласти4шцирую щим свойствам известные пластификаторы: Заявленные соединения получают озонол зом ангидридов или эфиров бицйкло- 2,2, ij -5 гептен-2-моно-или 2,3-дикарбоновых кислот, в метаноле при О-{-)7О С с после дующим восстановлением перекисных проду тов озонолиза диалкил- или циклоалкилсуль фидами или водородом в присутствии катализатора гидрирования и этерификацией образующихся производных диформилциклопен танкарбоновых кислот метанолом или этиленгликолем. Целевые; продукты выделяют известными приемами, например перегонко Выход составляет 75-85%. Пример. I Диметиловый эфир 3,4 -бис- {диметоксиметил) -1,2-циклопентандикарбоновой кислоты. В четырехгорлую колбу, снабженную ме шалкой, обратным холодильником с отводом термометром и трубкой для ввода газа, за ружают 4,1 г (0,025 г.моль) ангидрида эндо, цис-бнцикло- 2,2,1 -гепт-5-ен-2,3-дикарбоновой кислоты (а) и 16О мл метанола. При (-)7О С через раствор пропус кают озон-кислородную смесь (5,5 вес.%: озона) со скоростью 25 л/ч до появления голубой окраски раствора. Реакционную см одувают аргоном, добавляют 2,6 мл диетилсульфида, перемешивают 1 ч и оставяют на 12-15 ч при комнатной темперауре. Затем добавляют 16 ivoi концентрироанной Hj, S 0 и кипятят 3 ч, после охаждения добавляют 5О мл эфира, промыват водой (2 раза по 50 мл), 5%-ным водым раствором соды (2 раза по 50 мл), одные растворы экстрагируют эфиром (3 аза по 40 мл). Объединенный эфирный аствор промывают 5О мл воды и сушат над/ ульфатом магния. Эфир отгоняют, получат 6,35 г (76%) эфира 1 (R., -Xj,COOCHj), т. кип. 143-143,5°С 2,5 мм DT. ст.). -Лмм рт. ст.), л 1,4590, ИК-спектр : 1745 () 12О5 С - О СН), дублет 1070, 1135 ( .С ). ПМР-спектр- ( , м. д. числопротонов) : 3,2, 12Н (-ОСНд), 3,5 6Н (), 4,05 (дублет, Q Гц), 2Н , -ru OfiС ь Найдено,%: С 54,14, 54,23; Н 7,69, 7,51. Sf z6°eВычислено,%: С 53,88; Н 7,84. Пример 2. 8,2г ангидрида (а) озонируют, как описано в примере 1, в 32 О мл метанола. После отдувки аргоном добавляют 5,2 мл диметилсульфида и оставляют на Ю-12 ч при комнатной температуре. Метанол отгоняют под вакуумом, остаток разбавляют водой и отфильтровывают 5,8 г (48%) син-3,5-бис-(метоксиметил)-1,1 :,2,1 -циклопентандикарболактона, т. пл. 178,5-179,5 С (из спирта). ИК-спектр ( V , см) : 178О (СО в 5-членном лактоне). ПМР-спектр ( , , м. д. число протонов) : 3,48, 3,42 и 3,35, 6Н (-OCHj), 5,2-5,О5 2Н (-CHlSu ) . Найдено,%: С 54,23; 54,8; Н 5,95, 5,69. с«н,о. ; Вычислено,%: С 54,54; Н 5,83. К 5 г дилактона добавляют 50 мл метанола, содержащего 16,5% хлористого водорода, и кипятят 3 ч. Далее обрабатывают, как описано в примере 1. Выход эфира 1 (); (.:OOCHj) 6,05 г (87%), ИК- и ПМР-спектры идентичны спектрам продукта, полученного в примере 1 Пример 3, 4,1 г ангидрида (а) озонируют в 16О мл метанола, как описано в примере 1. Реакционную смесь продувают аргоном, добавляют 0,2 г катализатора палладия на Ва$0д и гидрируют при комнатной температуре и нормальном давлении до отрицательной реакции на перекись (проба с йодистым калием), катализатор отфильтровывают, добавляют 16 мл концентрированиой if, 5 0 и обрабатывают, как указано в примере 1. Выхоц эфира 1 (К , СООСН5) 6,75 (82%). Пример 4. 8,2 г ангидрида (а) :озонируют в 320 мл метанола, как огисано в примере 1. Избыточный озон отдувают аргоном, добавляют 16,8 мл смеси цик ; лоапкилсульфидов с т. кип. 190-23О С, ; вы деле иных из нефти. Обрабатывают, как описано в примере 3, отфильтровывают 6,5 г (54%) дилактона, т. пл. 178-179°С Полученный дилактрн растворяют в 50 мл метанола, содержащего 16,5% хлористого водорода, кипятят 3 ч. Далее обрабатывают, как описано в примере 1. Получают 8,1 г (90%) эфира I (.F.CH,: Х , Xj COOCHj). Пример 5. 4,1 г. ангидрида экао, цис-бицикло- . 2. ij -гепт-5-ен- 2,3-дикарбоновой кислоты озонируют в 16О мл мета нола и далее обрабатывают, как описано в примере 1. Получают 6,5 г (78i%) эфира I (,CHj; X:| Xj COOCHj), т. кип, 142,5-144°С (2,5 мм рт.;ст.),459 ИК- и ПМР-спектры идентичны спектрам продукта, полученного в примере 1. Пример Q. 2г эфира эндо, цис-бицикло- 2.2.1J-гепт-5-ен-2,3-дикарбоновой кислоты (б) озонируют в 50 мл метанЬла, как описано в примере 1. Вносят 0,2 rPd/BaSO H гидрируют, как описано в примере 3. Добавляют 5 гил концентрированной HI $ Од и далее офабатывают, как описано в примере 1. Выход эфира I (К R. MDHj; Х Х COOCHj) 2,62 г (82%). Пример 7. Зг |эфира (б) озониру ют в 5О мл метанола, как описано в примере 1. Добавляют 1,5 мл диметилсульфи,да и обрабатывают как в примере 1, полу3,6 г (74%) эфира 1 (R Rj, X,j COOCHj). П р И м е р 8. 3 г Монометилового эфира эндо, цис-бицикло-{ 2.2.13-гепт-5-ен-2,3-дикарбоновой кислоты озонируют |в 1ОО мл метанола, как описано в примере il. Добавляют 1,6 мл диметилсульфида и обрабатывают как в примере 1, получая 13,5 г (67%) эфира I (R R. :Х Х2 СООСН5). Пример 9. 9, lO-биc-(l,3-диoкca-2-циклoпeнтил)-3, 6-диоксабицикло- 6-3-0 -ундекан-2,7-дион. 3 г диметилового эфира эндо, цис-бицикло- Е2.2. i -гепт-5-ен-2,3-дикарбоновой кислоты озонируют в 50 мл метанола, как описано в примере 1. Приливают 1,5 мл диметилсульфида, перемешивают 1ч и оставляют на 10-15 ч при комнатной температуре. Затем метанол отго няют, добавляют 25 мл бензола, 1,14 г : этиленгликоля, 0,26 г п-толуолсульфокис:лоты и кипятят С насадкой Дина-Старка до прекращения выделения воды. Реакцион|ную смесь после охлаждения промывают |5%-ным водным раствором соды, затем водой до нейтральной реакции, сушатМо$ОдИ |упаривают. Выход соединения 1 ( 9 -O-CH -CHj-Q-9-5 2,5 г (54%), т. кип. 170°С1(2,5 мм рт.ст.;.; j ,п« ; 1,4837. ИК-спектр Г , см); ;1740 (), широкая полоса с расщеплением при 1180, 1210 и 1280 {С-О-СН), дублет 104О, 11ОО (сн::; ПМР-спектр («J-, м. д., число Н): 3,47 (триплет, 1 Гц), 8Н (2О-СН СНи-0), 3,72 (триплет, /- 3,5 Гц), 4Н (9 О-СН -СН -О-С-), 4,70 (дублет, ), 2Н (2СН1 Найдено,%: С 54,59; 54,80; Н 6,30, 6,16, .,QOg. Вычислено,%: С 54,87; Н 6,14. Пример 10. Метиловый эфир 2,4-бис- (д иметоксиметил) -цик лопентанк ар брно(вой кислоты. 3 г эндо-бицикло- 2.2. ij-гепт-5-ен-2-карбоновой кислоты озонируют в 5О мл метанола, как указано в примере 1, приливают 2,4 мл диметилсульфида, размеишвают 1 ч и оставляют на 1О-15 ч при комнатной температуре, добавляют 5 мл концертрированной Hj S Од и кипятят 3 ч. Выделяют проаукт, как указано в примере 1. Получают 4 г (7О%) эфира (1 А CHj; Хд Xi COOCHs), т. кип. (4 мм рт. ст), я iJ 1,4568. ИК-спектр (V , см): 174О (СО,СН,) 1180, 120О, 127О .(д-О-СН.), дублет 1070, 1135 (CHCoIc). о ПМР-спектр ( о , м. д., число протонов): 3,19, 12Н (4 ОСИ,); 3,54, ЗН (); 14,03 (дублет, 5гц), 2Н (2CHrgli ) Найдено,%: С 57,10, 56,85; Н 8,47, 8,35. СпН|40бВычислено,%: С 56,50; Н 8,75. П р ер 11. 3 г эндо-бицикло- 2. 2Л -5-гептан-2-карбоновойкислохы озон руютв 5О МП метанола, как описано в примере ij добавляют 2,4 мл диматилсульфида, размешивают 1 ч И: оставляют на 10-15. ч при комнатной температуре. Затем реакционную смесь разбавляют водой (4О мл), экстрагируют эфиром 3 раза по 20 мл), эфирный pacTBOp промывают водой (3 раза по ЗО мл), сушат над .gSO., эфир отгоняют, остаток на носят на окись алюминия в колонке и / элюируют эфиром. После упаривания получа- г (63%) 2-мeтoкcимeтил-4-(димe- ют 2,5 тoкcимeтил}-l, 1 -циклопентанкарболактона.


| название | год | авторы | номер документа |
|---|---|---|---|
| Диалкиловые эфиры 3-окса-2,4диалкокси-6,7-бицикло-/3.2.1/-октан-дикарбоновых кислот как пластификаторы поливинихлорида и способ их получения | 1974 |
|
SU521254A1 |
| Способ получения производных циклопентановой кислоты | 1973 |
|
SU682124A3 |
| Способ получения бициклических простагландинов или их солей | 1977 |
|
SU978725A3 |
| Способ получения производных простановой кислоты | 1973 |
|
SU648088A3 |
| Способ получения 1-формил-2-ацил3-оксициклопентанов | 1976 |
|
SU639854A1 |
| Способ получения производных бициклических карбоновых кислот или их аддативных солей с кислотами | 1973 |
|
SU583749A3 |
| Способ получения эндо=цис=бицикло [3.3.0=ОКТЕН=6=ОЛА=2 С ИСПОЛЬЗОВАНИЕМ ЩЕЛОЧНОГО ГИДРОЛИЗА | 1979 |
|
SU780428A1 |
| Способ получения 6-диметоксиметил-3-оксо-2-оксабицикло-(3,3,0)-окт-7-ена | 1980 |
|
SU967052A1 |
| Макроциклические гексаперекиси в качестве инициаторов радикальной полимеризации и структурирования полимерных систем и способ их получения | 1976 |
|
SU586169A1 |
| Окси- -карбметокси- -алканолиды в качестве пластификаторов поливинилхлорида и способ их получения | 1975 |
|
SU550388A1 |



Авторы
Даты
1976-07-15—Публикация
1974-08-27—Подача