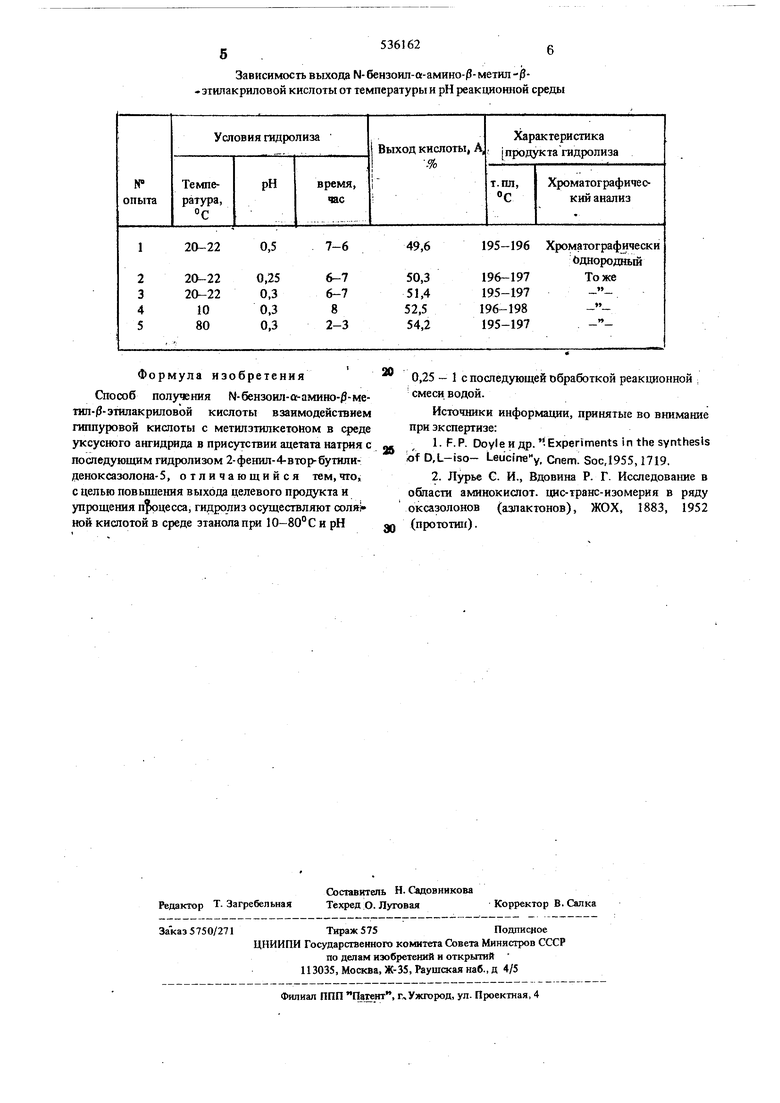
обработки,что значительно упрощает процесс получения Й-бензоил-а-амимо-/ -мётил-0-этйд рило вой кислоты. Возможность применения этанола вместо метанола улучшает условия проведения прюцесса. Способ заключается в следующем: при взаимодействии гиппуровой кислоты с метилэтилкетоном в среде Уксусного ангидрида в присутствии ацетата натрия после упаривания реакционной массы и обработки водой получают технический 2-фенил-4-втор-бутилиденрксазолон-5 (красное масло). Оксазолон Б растворяют в этиловом спирте, опиртовый раствор подкисляют концентрированной соляной кислотой до -сильнокислой реакции и выдерживают при lO-SOC 5-8 ч. По окончании гидролиза раствор частично упаривают в вакууме при 20- 30 мм рт.ст., в упаренную шссу доливают воду д|1Я растворения neopraHHiecKHX примесей и выделения кислоты А. Пример 1. Загружают 54 г (0,3 моля) гиппуровой кислоты, 1300мл метилэтилкетона, 24 г (0,29 моля) ацетата натрия и при перемепшвании в течение ЗОмин добавляют 76 мл (0,75 моля) уксусного ашидрида. Реакдаонную смесь кипятят при нагревании в течение 6 ч. По охлаждении реакционную смесь отфильтровывают и упаривают. Остаток выпивают в 1 л воды и выдерживают при 15-20°С в течение 6 ч. Затем красное масло отделяют на делительной воронке и растворяют в 300 мл этилового спирта. Спиртовьш раствор, подкисляют 40мл концентрированной соляной кислоты. После стояния в течение 5 ч. при 2Q-22C гидролизную смесь упаривают до 1/2 первоначального объема, добавляют 300 мл дистиллированной-воды и отфильтровьшают 34 г N-бензоил -о -амино-/3-метил-/3-этилакриловой кислоты. Кислоту А промьшают водно-спиртовым раствором. Выход 48,6%, считая на гиппуровую кислоту; т.пл.196- 99С. Найдено,%: С 65,29; И 6,55; N 5,58. CijH.sOjN Вьпшслено,%:С66,92; Н6,49; N6,12. Пример 2. Загружают 54 г (0,3 моля) гиппуровой кислоты, 1300 мл метилэтилкетона, 24 г (0,29 моля) ацетата натр«я и. при перемешивании в течение 30 мин добавляют 76 мл (0,75 моля) yKcycHOjo ангидрида. Реакционную смесь кипятят при нагревании в течение 6 ч. По охлаждении реакциоЩ1ую смесь отфилыровьгеают и упаривают. Остаток выливают в 1 л воды и выдерживают при 15-20°С в течение 6ч. Затем красное масло .отделяют на делительной ворюнке и растворяют в 250мл этилового спирта. Спиртовьш раствор подкисляют 55 мл концентрированной соляной кислоты. После стояния в течение 8 ч при 20-22° С гидролизнзто смесь упаривают до половины первоначального объема, добавляют 400 мл дистиллированной воды и отфильтровывают 35,2 г кислоты А. Кислоту А промывают водно-спиртовым раствором. Выход 50,3%, считая на гипцуровую кислоту. Пример 3. Загружают 27 г (0,15 моля) ги4пуровой кислоты, 650 мл метилэтилкетона, 12 г (0,145 моля) ацетата натрия и при перемешивании в тече1ше 30 мин добавляют 38 мл (О, 38 моля) уксусАого ангидрида. Реакционную смесь кипятят при нагревании в течение 7 ч. По охлаждении реакционную смесь отфильтровьюают и упаривают, упаренный остаток растворяют в 250 мл этилового спирта. Спиртовой раствор фильтруют и фильтрат подкис гяют 25 мл концентрированной соляной кислоты до рН 0,3. : После стояния в течение 6ч при 20-22° С к гидролизной смеси добавляют 1 л дистиллированной воды. Отфильтровьшают 18,12 г N-бензоил-а-амино-Д-метил-/3-этилакриловой кислоты. Выход 51,4% в расчете на гаяпуровую кислоту; Т.ПЛ. 195-197°С. Найдено, %: С 65,53; Н6,46; N6,19 CijHisOjN Вычислено,%: С66,92; Н6,49; N6,12 Хроматографшкски однородный. Пример 4. Технический 2-фенил- 4-втор- бутилиденоксаэолон- 5, полученный аналогично примеру 3, растворяют в 250-300мл этилового спирта, спиртовый раствор фильтруют, фильтрат доводят до заданной температуры, добавляют 20-25 мл концентрированной соляной кислоты (рН 0,2-0,5) и выдерживают гидролизуемую смесь при этой температуре. Кристагты М-бензош1Ч1 -амино-13-метил-| -этилакриловой кислоты отфипьтровьюают. Результаты приведены в таблице.
Формула изобретения
Способ получения N-бензоил-а-амино- -метип- Этилакриловой кислоты взаимодействием гиппуровой кислоты с метнлзтилкетоиом в среде Зтссусного ангидрида в присутствии ацетата натрия с последующим гидролнетм 2-фенил-4-втор-бутилиденоксазолона-5, отличающийся тем,что, с целью повьпиення выхода целевого продукта и упрощения п цесса, гидролиз осуществляют соля ной кислотой в среде зтанолапри 10-80° С и рН
0,25 - 1 с последующей обработкой реакционной ; смеси водой.
Источники информации, принятые во внимание при экспертизе:
1.F.P. Doyle и др. .Experiments in the synthesis of D,L-iso- LeucineY Cnem Soc,1955,1719.
2.Лурье G. И., Вдовина P. Г. Исследова ше в области аминокислот, цис-транс-изомерия в ряду оксазолонов (азлактонов), ЖОХ, 1883, 1952 (прототш).

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения метилового эфира -бензоил- -амино- -метилэтилакриловой кислоты | 1975 |
|
SU529154A1 |
| Способ получения -изолейцина | 1976 |
|
SU573478A1 |
| Способ получения д -изолейцина | 1975 |
|
SU592817A1 |
| Способ получения -пролина | 1975 |
|
SU525673A1 |
| Способ получения производных индолизина или их солей | 1977 |
|
SU674674A3 |
| Способ получения замещенных оксикротоновых кислот | 1970 |
|
SU474134A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 1,2-ДНГИДРО-1,2,4- | 1968 |
|
SU231412A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ 3-ОКСИБЕНЗХИНУКЛИДИНА | 1969 |
|
SU242172A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,5-ДИАРИЛОКСАЗОЛОВ | 1992 |
|
RU2057127C1 |
| Способ получения производных аминопропанола или их солей, рацематов или оптически-активных антиподов | 1975 |
|
SU586835A3 |


Авторы
Даты
1976-11-25—Публикация
1975-04-28—Подача