Под соединениялш общей формулы 1 подразуме ваются также стереоизомеры и оптически активные соединения и их смеси, в особенности рацемат.
Преддочитаемые , заместители, представленные выражением те)- это остатки пиррола, пиразола, имидазопа, фурана, тиофена, тиазола, пиридина, пиридазииа, пиримидина и пиразина.
Если заместители Rj и Нз вместе с атомом азота, с которым они связаны, и в соответствуюшрм случае с дополнительным гетероатомом кислорода или серы образуют насыщенный 5- или 6-членный гетероцикл, то это, в частности, остатки пирролидина, пиперидина, морфолина и тиоморфолина.
Пригодными для образования солей с соединениями общей формулы 1 ярляются неорганические и органические кислоты. Подходящими кислотами являются, например, хлористоводородная, бромистоводородная, фосфорная, серная, щавелевая, молочная, винная, уксусная, салицильная, бензойная, лимонная, адишшовая или нафталин- 1,5- дисульфокислота.
Для получения соединений формулы I 1-фенокси-3- амино-пропан-2-ол общей формулы И
о-ш -сн-йНз- н он
где А имеет указанные значения, подвергают взаимодействию с соедине шем общей формулы III
У-Х где X имеет указанное значение;
У означает галоген, например, хлор или брс л, и если X означает
С- CH-d--(Het)
Если X означает
-с сн-со-ше
то ускоряют реакцию путем добавки кислоты, предпочтительно хлористоводородной кислоты. Примерами других подходящих кислот являются карбоновые кислоты, например муравьиная, уксусная, пропионовая, масляная, сульфокислоты, например бензойная сульфокислота, р-толуолсульфокислота, минеральные кислоты, например серная и фосфорная. Если применяют соединение общей формулы 111, 5де У ОН, то каталитические количества 1йислоты, например уксусной или муравьиной достаточны для ускорения реакции. Если применяют соединения общей формулы III, где У ONa, или ОК, то прибавляют примерно 1 моль кислоты. Вместо добавки кислоты можно
применять 1 моль кислоты. Вместо добавки кислоты можно применять для ускорения реакции и соединение общей формулы II в виде его соли, например в виде гидрогалогенангидрида. Если применяют соединение общей формулы 111, где У означает атом галогена, то можцо применять это соединение общей формулы III и в виде гидрогалогенангидрида. По предлагаемому способу можно получать кислотно-аддитивные соли соединений 1 .или при добавке связующих кислоты средств.
например поташа или соды свободные амины.
Требуемые исходные соединения общей формулы III представляют собой в зависимости от значения X или производные пропен- (2) -она-1 общей формулы IV или пропанола- (1) общей
формулы
Т-С Сй С-Щ€1)
К,
то у означает такЖе и -ОН,ОК или ONa. Взаимодействие осуществляется обычно в подходящем растворителе или диспергаторе, в котором растворяют или взвешивают вещества, участвующие в реакщ{и. Такие растворители или диспергаторы представляют собой, например, ароматич еские углеводороды, например бензол, толуол, ксилол, кетоны, например ацетон, метилэтилкетон, галогенированные углеводороды, например хлороформ, четыреххлористьшуглерод, хлорбензол, хлористые метилен, простые эфиры, например тетрагидрофуран и диоксан, сульфоксиды, например диметилсульфоксид, третичные амиды кислоты, например диметилформамид и N-метил-пирролидон. В качестве растворителей применяют, в частности, полярные растворители, например спирты. Подходящими спиртами являются, например, метанол, этанол, изопропанол, трет-бутанол и т. д. Решсция осуществляется при температуре от 20° С до температуры дефлегмации применяемого растворителя .или диспергатора. Во многих спучаях реакция происходит joKe при нормальной температуре,--,
Hai-CH-CH2--CH ra.€t) -Ri он
где У имеет указанные значения;
Hal означает галоген, в частности хлор или бром.
Кислотно-аддитивнью соли соединений общей формулы 1 можно получать известным способом из компонентов. В общем применение разбавителя является преимущественным, нр51чем получают при избытке кислоты в общем ди-солн соединений формулы. Моно-кислотно-аддитивные соли получают или путем определенной добавки только 1 моля кислоты или путем частичного гидролиза да-кислотно-аддитивных солей.
Пример. 5,1г1- (р-метоксибутокси-феноксй) -З-аминопропан-2-ола формулы
«Hse-«3H,)4-0
О -PHf CH-CHj-Nfl, ОН растворяют в 50 мл этшюла, затем добавляют 3,3 i никогиноилацетона формулы f do-CH -co-CHj Ц и после добавления 1 капли муравьюгой кислоты раствор пагревают 3 часа до температуры дефлегмации. Раствор концентрируют в вакууме. Остается твердый остаток, которьш одаш раз перекристаллизовывают из толуола. Таким образом получают 1- (2-никотиноил-1-метилвиниламино) -3- (р-метоксибутокси-фенокси) пропан-2-ол формулы (CH,U-0-о-снг-сн-сн7- ин; сн-соонсн. СТ. ПЛ. 108°С. Выход продукта 78% от теоретического. Требуемый никовшоилацетон можно получать или из этилового эфира никотиновой кислоты и безводного ацетона в присутствии эгилата натрия или из ацетилпиридина по следующему способу. 22,4 г трет-бутилата калия взвешивают в 150мл безводного бензола, затем по каплям при перемешивании и температуре 10° С медленно Добавляют смесь, полученную из 18,3 г этилацетата и 24,2 г 3-ацетилпиридина, после чего смесь выдерживают в течение суток при комнатной температуре. После этого отсасывают, дважды промьшают свободным от воды бензолом, затем дважды безводным этанолом и дважды простым диэтиловым эфиром. В результате получают калиевую соль никотиноилацетона с выходом 77% от теоретического. Из соли калия можно получать с помощью кислого гидролиза практически количественно свободный никотипоиладетон. Требуемый 1- (р-метоксибутокси-фенокси)-З-аминопропан-2-ол можно получать следующим образом. Из простого монобензилового эфира гидрохинона и (4-бром-бутил)- метилового эфира получают нагреванием с ацетоном в присутствю избьтгка поташа 4- (4-метоксибутокси) -фенилбензилов ый эфир Ш50-( ст. пл. 60-6 г с. Гидрированием в метанольном растворе (никель Ренея, 50 ати HI , 50°) получают 4(4-метоксибутокси) -фенол СНзО(СН2) в виде масла с т. кип. 138-143 / 0,1 торр. Этот фенол можно подвергать взаимодействию с эпихлоргидрином. Получе1шый 4- (4-метоксибутокси) -фенилглицидиловый эфир
,бс
CHjO-lCHs).
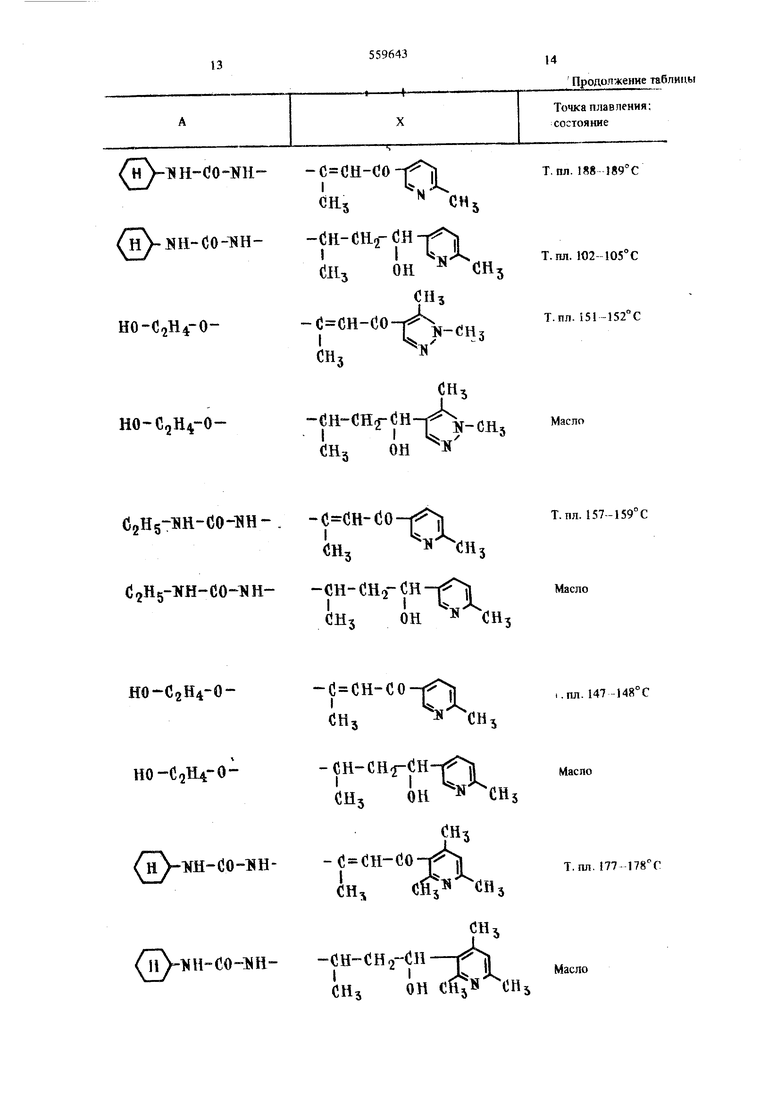
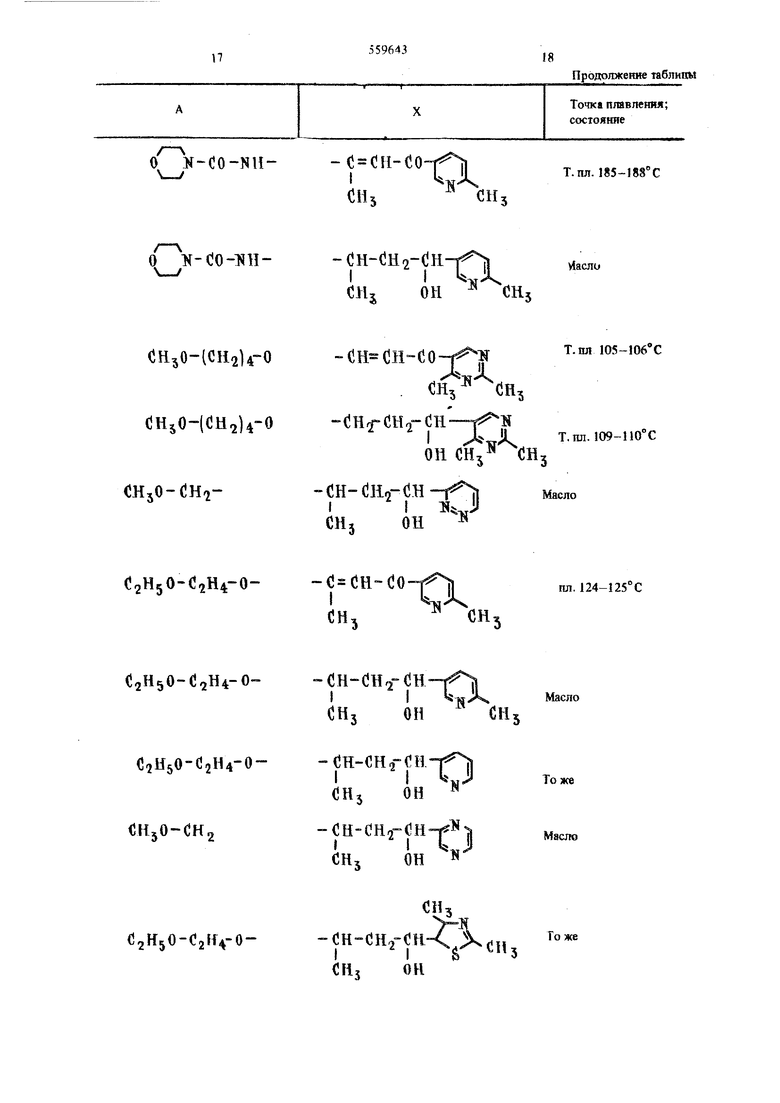
ИС ОИз . непосредственно перемешивают 20 час при комнатной температуре с избыточным насыщенным водно-спиртовым аммиач1сым раствором. Реакщюнную смесь вьтаривают при по1шжешюм давлении и остаток перегоняют в вакууме. Таким образом получают 1- 4- (4-метоксибутокси) -фенокси -З-аминопропан-2-ол -O-CHj-CH-CH -HH, eHsO-i iH,j)4-oQHс выходом 57%; т. кип. 207-219°/0,1 торр, т. пп. 84-88°. После перекристаллизации из толуола или переосаждения из разбавленной соляной кислоты т. пл. 92-93°. При применении простого /3-бромэтилэтилового эфира вместо (4-6poM6yTiui)- метилового эфира получают одиншсовым образом простой 4- (2-этокси) -фешшбензиловый эфир fl HjOс т. пл. 35-37° и из последнего соответственно указажюму способу следующем соединения: 4- (2-этоксиэтокси) -фенол (J2 U-04 у-ОН в виде масла; (2-этокспэтсжси) -фенилтлицидипростой 4ловьш эфир gHgO-i sUoOHj O-CH -CH-CH в В1ще 1шзкош1авкого твердого вещества с т. кип. 135-143°/0,1 торра; 1 - 4 - (2 - этокси - этокси) - фенокси - 3 - амино nponaH - 2 - ол HsOrC lU-O- O-dHfCH-CHf- H, ст. пл. 84-86° с. Последний дает после конденсации с никотиноилацетоном 1- (2-никотиноил-1- метклвишшамино) -3- . (р-этоксиэтоксифенокси) -пропан-2-ол i с т. пл. 88-89° С. О р п м е р 2. Соешше1ше формулы Н ВН-СО-ВН -о-сн -сн-.сн.-ин, I он астворяют в 50 мл безводного толуола, добавляя ,7 г безводного поташа. К этой смеси при охлажении и переме1Ш1ванин медленно прибавляют месь из 4,4 г 2-никотнноил-1- метйлвинилхлоридидрохлорида )Пз1 (получен нз натриевой соли никотиноилацетона, с переводом его сначала газообразным НС1 в пщ)охлорид свободного никотиноилацетона и затем тионилхлоридом в гидрохл6рид-(3-никотиноил-а-метилвинилхлорида) в 50 мл безводного толуола, после чего дополнительно перемешивают в течение 36 час при комнаткой температуре. Затем отсасывают, остаток растворяют в воде, чарбонатом натрия доводят до шелочного состояния и раствор трижды экстрагируют хлороформом. Хлороформные экстракты вместе с первоначальным толуольным фильтратом концентрируют в вакууме приблизительно при 14-20 торр. В результате повторной перекристаллизации из водного этанола получают 1- (2-НИКОТИПОИЛ-1- мегилвиниламино)-3- (р-циклогексилуреидофенокси) пропан-2-ол формулы к)-нн- do-«и- 3 f t с т. пл. 168° С и выходом 81% от теоретического. П р и м е р 3. 6,1 г 1- (р-циклогексилуреидо-фенокси) -3- аминопропан-2-ола формулы -O-CHfCH-CHj-lRH, -ии-со-ннрастворяют в 50 мл безводного тол)ола и добавляют 5,7 г безводного поташа. К этой смеси при юремецшвашш и охлаждении медленно прибав ляют смесь, полученную из 4,4 г гидрохлорида 1(-пиридил) -3- хлорбутан-1-ола формулы (Си, он (получен восстановлением из описанного в примере 2 гидрохлорида 2-никотиноил-1- метклвинилхлорида) в 50 мл безводного толуола, с последуюпщм нагреванием смеси в течение 18 час при перемешивании, охлаждают, отсасывают, остаток растворяют в воде и раствор доводят 2 и. соляной кислотой до рН 1. Затем кислый раствор трижды промьшают уксусным эфиром, нейтрализуют до рН 5, трижды промывают уксусным эфиром, с помоа ю содового раствора раствор доводят до щелочного значения рН9 и трижды экстрагируют хлороформом. Соединенные хлороформные экстракты высушивают и концентрируют в вакууме. Таким образом получают 1- (р-циклогексил-уреидофенокси) -3- (1-окси-1-пиридил) -3-(бутил-З-амино) -пропан-2-ол в виде бесцветного масла формулы (и)-:йн.-со-«н-0-CHf CK-CH -TiH-CH-CH CHВыход продукта 63% от теоретического. П р и м е р 4. 2,6 г пвдрохлорида 1-амино-3-(р-этокснметилен-фенркси) - .пропан - 2 - ола фор мулы -O-CHj-CK-CHf-«и, НС1 ;7Нг«- 5Н7 взвешивают в 40 мл этанола, затем добавляют 1,8 г 1 атриевой соли теноил (2)-винилового спирта формулы СН(ЗН-ОЖа и смесь перемешивают в течение суток при комнатной температуре. Затем отсасывают, остаток промьтают спиртом. Фильтрат вместе с промывочным стшртом концентрируют в вакууме. Остается масло, которое после длительного вьщержнвания получает твердое состояние и подвергается перекристаллизации из разбавленного спирта. Получают I- {тепоил (2)-виниламино -3- (р-этоксиметилен- фенокси) -пропан-2-ол формулы jHsO-CHj-Q-О-(Нг-сн- ;н2-яй- :н-сн-со-О Л 5УI 1 с т. пл. 103° с. Выч..слено,%: С 63,1; Н 6,4; N 3,9. CislbjNOAS Найдено,%: С 62,9; Н 6,5; N3,9 Выход продукта 91 % от теоретического. Требуемую натриевую соль теоиил (2)-вшшлового спирта можно получить ел. ук)Щим образом. 32 г 2-ацегилтиофена и 18 г зтилового эфира муравьиной кислоты добавляют при перемеишванйи по каплям в течение 20 шн и температуре 10-15°Сквзвеси 1,3г метилата в 100 мл абсолютного простого зфира. Затем смесь выдерживают 29 час при комнатной температуре. Отсасывают, остаток промывают небольшим количеством абсолютного спирта и затем простым эфиром. Получают натриевую соль тейоил (2)-винилового спирта с выходом 95%. П р и м е р 5. 2,5 г гидрохлорида 1- (р-метоксиметилен-фенокси) -3- амино-пропан-2-ола фор мулы ,1НзО-СН2- 0- 5112- н- Н,-1ГН,-НС1 ОН звешивают в 40 мл этанола, затем прибавляют 1,6 г натриевой соли фуроил (2)-винилового спирта ормулы /Л-СО--(}Н-СН-0 а 0 смесь перемешивают в течение суток при коматной температуре. После этого смесь перерабатывают аналогично примеру 4. В результате получают 1- фуронл (2)-вюшламино -3- (р-метоксимет лен-фенокси) фопая-2-ол формулы «B.O-CHJ-rV« - lB,-Cn-CH,-NH-CH«CH-Co-O Р1 УIо с t. Ш1. 108 С. Выход продукта 73% от теоретического. Требуемую в качестве исходного продукта натриевую соль фуроил (2)-вшшловог6 шнрта получают из 2-ацетилфурана, этилового эфира муравьиной кислоты и метвлата яатрвя анялогячво йолЯения натриевой сехпи теноял (2) -винилового спирта, описанному в примере 4. f iiT«tr n/4T /ArV4 /«ГГигъЧ 41 rru/XktnXJ &JXr tk rtt Vt AAffVl A П р и м е р 6. Соответственяо примерам Ь5 получают соедииения общей 1фсфмупы 1,пр«ведеяные в таблице.







| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 1-фенокси-3-аминопропан-2-ола или их солей | 1974 |
|
SU598557A3 |
| Способ получения производных 1фенокси-3-амино-пропан-2-ола или их солей | 1974 |
|
SU549078A3 |
| Способ получения производных 1-фенокси3-аминопропан 2-ола | 1973 |
|
SU493958A3 |
| Способ получения производных 1-фенокси-3-аминопропан-2-ола | 1973 |
|
SU489309A3 |
| Способ получения производных 1-фенокси-3-аминопропан2-ола или их солей | 1973 |
|
SU563120A3 |
| Способ получения производных 1-фенокси -3-аминопропан-2-ола | 1972 |
|
SU457211A3 |
| Способ получения производных 1-фенокси3-аминопропан-2-ола | 1972 |
|
SU487484A3 |
| Способ получения производных урейдофеноксиалканоламина | 1971 |
|
SU496268A1 |
| Способ получения 1-фенокси-3-аминопропан-2-ола или их солей | 1974 |
|
SU580830A3 |
| Способ получения производных 1-фенокси-3-аминопропан-2-ола | 1972 |
|
SU481150A3 |

С,Е5-1Н еО- Н- -С-Щ-СО-C-Cll2-CB.-f
Н
-CKf-CH,
(
1 1
т. Ш1,50° с (разшмйяше)
сн.
Oil
Масло
он
Тоже
он т. ал. 143С
А
CHjO-tdH lrotiHj dii.«
НзО(Н2)гО -Ш-Шу-СН
€% Oil CHf т
/HVlH dO-3fH С. :z/IL i
(
ц, ш cnJ с
и СИ-соCgH-sO-CH Uii-dHf С2Н50-СН2-Продолжение таблицы
Точка плавления;
X состояние
J.m.79-Bl°C
Масло
Т. ПЛ. 179-180° С
прело; соль с 0,5 моля (-J.)винной кислоты; т. пл. 113-118° (разложеьша)
.пл. 133 134°С 11Масло Нч
i :CiiCgHg-NE-CO-MliГ, пл. 155-157° С
C HSO-CH С Hg-NH-OO- й- -СПЬСН -СЯ -T
Масло II Л СН N ios-io6°c Масло; соль с 0,5 моля .-i Ho Cll-Г .I ИIf ) винной кислоты; М Ниг, пл. 69-70° (гигроско аV/ II ч
НО С2Н4-0--С СН-СОСНч СН
-CH-CHr lH-fi
ОШз он
-((H-CO-rJ
oo-sHСН,
liVXH-CO-lUHСИ-СНо-СН
СИз он CRjS CHj
Продолжение таблицы
,.пл. 147-148°С
Масло
ъ
Т.пл. 177-1784
Масло
I eiig-t H-ciif iH-iio-flii --с ciTj-cii-cii -Nfi-co-sih -ai-dii -CH SH -CO-liliNH2 dO-NlI
CHjO-CH CHjO-CH
n-CAligO-CH --С ен-СО
n-d4H90-«rif,2Ё-(},П7 Ш1-СО- 11i - с 5117-iiii-ЙО-iJ II- продолжение г,1Гип1Им
I очка . сосгоямие «Из OK -C dH-6o I
(n-| IS
Macno I ,
OH CHj
СэШ-СО-Г HТ.ПЛ.118
.
ъ
-d-CHn-Cli
Масло
I I
dlig oil
H:
Oil
Масло
I
Ijll
CH. OH CH Olij 63 г ii-sCС И 5 Clu« H. Т.ПЛ. 192 -C Cli-CO-f T,nn, 165 . Gil, C-Hj CHj cii - сH r с H --t
О ir-CO-NUо -со-1«н-Он-(ЗН2-Он-т (CH2)4-0 dHsO-tCH lrOCH-diin-C.H-t
CiH-i«I J
СИ он
3
C CH-CO
02H50-C2H4-0-I
СНч
CH-on-2- 2H t
I twX
СНзOH
С2И50-С2Н4-0 - CH-CHrf и 1
riunu Д
CH, OH
СИ-СН2-СН-|
CHjO-CHg CHj OH «
(3H-CH2-C l- 4
02114-0Clij
Продолжение таблипм
Точка плавпсния; состояние
( Cri-CO-f
tЦ
Т.пл. 185-188°С
CHsСИ;
асли
I I
CHj он CHj
Масло
XX
пл. 124-125°C
сн
3
Масло
S
CH.
Тоже
Масло
Cib
Тоже
I OH (Н,гбН2 н--т dH-CH-CO-f WТ.ш, . . СН,(5И, I .Т.пл. 109-1Ю-С он CHj- OHj fnldaHyO-CHa H -
Формула изобретения
Способ аолучения производньк 1-фенокси-З-{ив1нопроп8Н-2-ола общей формулы I
О- (Hf (JH-OHfl tt-X ОН
rfleXN - |j /Het)
I II -
Bl о
Продолжение таблицы
Rj И Вз - водурод, алкил, алкенил, циклоалкил или вместе с атомом азота, с которым они связаны, и при необходимости с допо.гшительным гетероатомом кислорода или серы насыщенный 5или 6-членньш моноциклический цикл, причем алкилостатки содержат 1-4 атома углерода, алкоксиостатки - 1-4 атома углерода, алкенилостатки-3 или 4 атома углерода и циклоалкилостатки - 5-7 атомов углерода,
или их солей с кислотами, отличающий тем, что соедине1ше общей формулы II
2 -CH CJH2-T fH2 I Ч-.. ал. 72-74°С
ШШ,
(H€i
1 I В| он
А - СНз - алкокси, -О - алкоксиалкил, -О - оксиалкил,
- Н-СО-Ж(
R.
Д1 - водород или метил;
Йеу- связанный через атом углерода ароматическдашш кьазиароматический 5- или 6-членный моноциклический цикл с 1 или 2 гетероатомами, причем один из гетероатомов представляет собой атом кислорода, азота или серы, и имеющийся в соответствующем случае второй гетероатом представляет собой атом азо±а, который может еще бьпъ замещен одной или несколькими метильными группами;
Oli
грё А имеет указанные значения подвергают взаимодействию с соеданением общей формулы 111
У-Х
где X имеет одно из указанных значешй;
У - галоген, и если X означает
ТО у может означать также -ОН, -ОК и ONa,
в инертном органическом растворителе или разбавителе при температуре от 20° С до темнературы дефлегмации применяемого растворителя или разбавителя с последующим вьщелением целевого продукта в свободном ввде или в виде соли.
Источники информации, пртятые во внимание
при экспертизе .
М.,Мир, 19о6г,стр. 244.

Авторы
Даты
1977-05-25—Публикация
1974-12-19—Подача