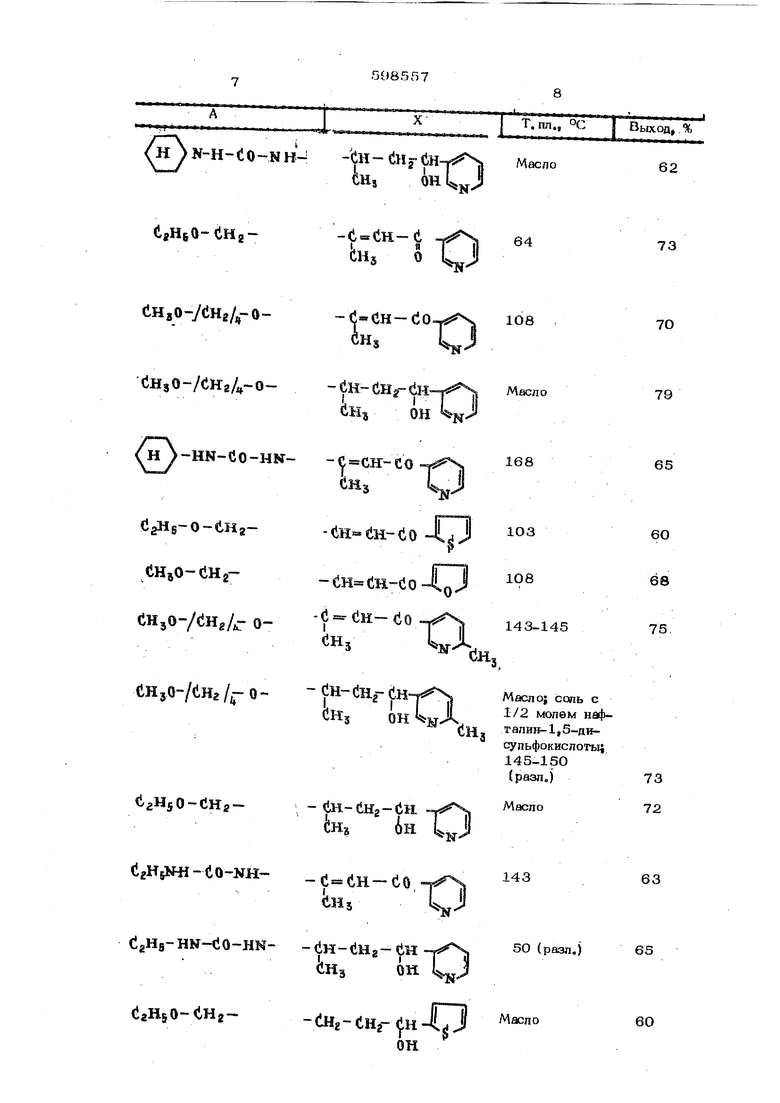
Изобретение касается способа получе шя новых производных 1-фенокси-З-аминопропан-2-ола, обладаюших ценными фармакопошческйми свойствами, Способ основан на известной редакции нук пеофипьного раскрытия оксиранов аминами (чпк реакции нукпеофипьного замещения атома галоида в гапоидгиюринах амнгнами) ,i, что позводяет поЛучить соединения, которые обладают лучшими свойствами, чем известные ранее структурные аналоги 2. Описывается способ получения соединений ri6iaeft Лормулы О-СНг- бН (JHj-NH-X (и ОН где X - rpynti «1 СН-С-(Нв1)«л (iH-dHa-dH-i II III BIон RI О А означает алкокси, О- алкокси- алкил, -О- оксиалкил или группу. -HN -СО-КРгРэ. PI - атом водорода или метил, Het представляет собой связанный через атом углерода ароматический или квазиароматический пяти- или шестичленный цикл с 1 или 2 roTepoaTOMaNOi, причем один из гетероатомов представляет собой атом кислорода, азота или серы, а второй гетероатом атом азота, причем этот цикл может быть замещен одной ипи несколькими метильными группами; Р и PJ-водород,алкил,алкенил,циклоалкип ипи вместе с атомом азота, с которым они связаны, а также с дополнительным гетероагомом кислорода или серы образуют пасыисэнный пяти- или шестичленный цикл, причем указанные алкилос татки содержат 1-4 атома углерода, алкоксиостатки - 1-4 атома углерода, алкенилостатки 3 или 4 атома угперода и циклоалкилостатки 5-7 атомов углерода, а также солей соединений формулы I с органическими или неорганическими кислотами. Согласно изобретению способ получения сстедтюний формулы Т или их со;юй заклю чается в том, что соединения формулы (11) где А имеет указанные значе1 йя, а 2 озна чает группу . (JH-(iHg- Hal ООН где Hat - атом галогена, подвергают взаимодействию с соедишнием общей КН.-Х Где X - имеет указанные значения Взаимодействие о уществпяют в среде органического растворичепя при температур от 2О С до темперазуры книения; используемого растворителя. Строение полученных соедивеннй подтверждено данными физико-химического (, ЯМР-спектры) и эпекаентного анализбаПример 1, К раствору 3 г l-{ft -пиридип)-3-аминобутш -1-ола в 50 мл без водного толуола прибавп5нот при перемешива НИИ при комнатной температуре 5,4 г 1-(п-метоксибутоксиф8нокси)2,3 эпоксипропана Смесь перемешивают в течение 36 ч при комнатной температуре, экстрагируют трижды разбавленной соляной кислотой, водные кислые экстракты доводят до щелочной реак ции бикарбонатом натрия и экстрагируют трижды толуолом. Толуопьные экстрасты сушат и концентрируют в вакууме.. Получайт в результате 4,4 г {58% от теории) l-(tt-мe окси токсифенокси)-3-(1-окси-1-пиридил- тил 3-амино)пропан-2-ол в виде бесцветного масла. Исходный 1-( -пиридил)-3-аминобутан-1-ол получают спедукэшим образом, а) 2 г калиевой соли никотиноилацетона суспендируют в 5О мл этанола, прибавляют 1,6 г бензиламингидрохлорида и смесь перемешивают в течение 24 ч при комнатной TeMnepaiyjie. Реакционную смесь фильтруют, остаток промывают этанолом, а фильтрат вместе с иромывным спиртом концентрируют в вакууме. Получают в остатке масло, которое затвер девает. Затвердевшее масло вместе с оставшимся при промывке спиртом обрабатывают водой и перекристаллизовывают из этанола. Получают К-(2-никотинош1-1 МетилвннилЙМ11 но) бензил амин с 88%-яым выходом. ., пп. 1О2-1О4 С. Последующим восстановлением с помощью натрийборгидрида получают с 62%-ным выходом 1-( -пиридил)-3-бензиламино-бутан -1-ол (масло), который подвергают гидрогенолизу в автоклаве, В результате образу- ется 1-( ft -пиридил)-З-аминобутан-1-ол (вязкое масло), б) 5 г 2-никотиноил-1-метилвиниламина растворяют в 5О мл этанола и при 7О С и перемешивании прибавляют по порциям 6 г натрийборгидрида, Вьщерживают смесь в течение Ю ч при 70 С, концентрируют, остаток растворяют в хлороформе (воде))органическую фазу отделяют, сушат и концёнтриууют в вакууме. Образующееся в остатке масло перегоняют в вакууме, Собираот фракцию 125-150 С/0,3 мм рт, ст., которую растворяют в диоксане, К полученному раствбру прибавляют раствор винной кислоты в диоксане. Вьтавшии тартрат отфильтровывают.перекрис- таллизовывают из смеси, диметилформамидсложный уксусный эфир и переводят в свободное основание. Получают с 73%-ным выходом 1-( -пиридил)-3-аминобута11-1-ол, 2-Никотиноил-1-метилвиниламин получают .следующим образом, 7,5 г никотиноилацетона растворяют в 45 мп безводного этанола, прибавляют 20 мл аммиака и перемешивают в автоклаве в течение 3 сут при 50°С, Прозрачный раствор после концентрирования :дает масло, которое затвердевает. После перекристаллизации из толуола получают с 91%ным вьрсодом 2-никотиноил-1-метилвиниламин (т. пп,82°С). Пример 2, К раствору 3,24 г 1- (6-мвтилпирид ил- 3) - 3-аминобу тан-1 -ол а в 5О мл безводного бензола прибавляют при перемешивании при комнатной температуре раствор 5,4 г 1-(1г-н-пропокс«этоксифенокси)-2,3-эпоксипропана. Смесь перемешивают 6ч при 45-50С и кипятят в течение 1 ч. Затем реакционную смесБ экстрагируют три раза разбавленной соляной кислотой, водные кислые экстракты подщелачивают бикарбонатом натрия и экстрагируют три раза бензолом. Бензольные экстракты высушивают и концентрируют в вакууме. Получают 4,7 г (59% от теории) (()-пропоксиэтоксифенокси)-3-(1-окси-1-)-6 метил-пиридил- 3 -бутил-3-амино)пропан-2-опа в виде бесцветных кристаллов, т,пл. 72-74°С, При использовании в качестве растворителя хлороформа получают целевой продукт с выходом 52% от теории, а при использовании йетролейного эфира выход целевого продукта составляет 38%. Пример 3, К раствору 3,45 г 1-{2,4| аиметилпиримидип-5)-3 аминобутан-1-опав 5О МП сухого тетрагидрофурана прибавляют при перемешивании при комнагной ч-емпературе 4,4 г 1-(г1-эгоксиметипфенокси)-2,3-эпоксипропана, Смесь перемешивают 6 ч при комнатной температуре, затем еще 10 ч при 50-55°С и 4 ч при 65°С, Реакционный раствор выпивают в 500 МП 8%-ного раствора NdHCO и экстрагируют :три раза 50 мл хлористого метипена. Органическую фазу экстрагируют три раза разбавленной соляной кислотой, водные кислые экстракты подщелачиваютбикарбонатом натрия и экстрагируют три раза бен зопом. Бензольные экстракты высушивают И; концентрируют в вакууме. Получают 4,3 г {59% от теории) 1-(а-этоксиметипфенок ;и)-3- 1-окси-1-( 2,4-димeтилпиpимидип-5)-бyтил-3-aмш o пропан-2-опа в виде бесцвет ного масла, из которого С-1/2 мопя L )-винной кислоты получают гигроскопическую соль с т. пп. 69-7О С, Пример 4. К раствору 2,9 г 2-никотиноил-1-метипвиниламина в 5О мл без водного ацетона приб авляют при перемешивании при. комнатной температуре раствор 5,4 г 1-( п-метоксибу токсифенокси)-2,3-эпоксипропана. Смесь перемешивают 6 ч при комнатной температуре, 10 ч при 40-45°С, а затем 4 ч кипятят при перемешивании с обратным холо ципьником. Полученную смесь выливают в раствор 4О г бикарбоната натрия в 500 мл воды и экстрагируют три раза 5О мл хлороформа Экстракт встряхивают три разас разбапленной соЛяной кислотой, водные кислые вытялски подщелачиваот бикарбонатом натрия и экстра гируют три раза бензолом. Бензольные экстракты высушивают и концентрируют в вакууме. Получают 4,6 г (62% от теории) 1- Тп-ме токе ибу токе ифе нокс и (- 3-) - 2-т-ник отиноил-1-метилвиниламино пропан-2-опа, т. пл, 108°С (из бензола). Пример 5. К раствору 3 г l-(ji -пиридил)-3-аминобутан-1-опа в 50 мп 6с;оводного диметипформамида прибавляют при гюремешивании при комнатной reMneparyf:ie раствор 5,1 г 1-(гьэтилам11нокарбонияамин1 фенокси)-2,3-эпоксипропана. Смесь перемешивают в-течение 24 ч при комнатной температуре, затем выливают в |500 МП 8%-ного водного раствора бикарбоната натрия. Полученный раствор экстрагирует 3 раза 50 мл хлороформа. Хлороформную фазу промывают 3 раза 250 мп водного 8%-ного раствора бикарбоната натрия и один раз 150.МП воды, а затем 3 раза экстрагируют разбавпе1шой соляной кислотой} водные экстракты подщелачивают бикарбонатом натрия и экстрагируют три раза бензолом. Бензольные экстракты высушивают и концентрируют в вакууме. Получают 4,6 г (63% от теории), 1-(а-этиламинокарбошшаминофенокси)-3-(1-окси-1-пиридип- з -бутип-3-амино)пропан-2-ола, т. пл. 5О С(раз(Ложение). Если вместо диметипформамида в качестве растворителя применяют диметипсульфоксид, то получают целевой продукт с выходом 53% от Teopira. Пример 6.К раствору 3,3 г 1-(2,4-диметилпиримидил)(-3-амино)пропан-1-ола в 50 мл безводного этанола прибавляют при перемешивании и комнатной температуре раствор 5,4 г 1-(п-метоксибу токсифенокси)-2,3-эпоксипропана. Смесь перемешивают 24 ч при комнатной температуре и 4 ч при 50-60°С, выливают , в 500 мл водного раствора бикарбоната натрия и водный щепочной раствор экстрагируют три раза толуолом. Толуольные экстракты высушиваот и коше1гтрируют в вакууме. Получают 5,3 г (68% от теории) 1-( ПгмеТоксибу токсифенокси)-3- 1-ОКСИ-1-(2,4-диметилпиримидил-5)-пропил-3-амиHOJ пропан-2-опа, т. лл. 109-11О С. Аналогично получают соединения формулы I , приведенные в табшще.
(1гН|ЬШ-СО КН
(
Сн
CgHa-HM-tO-HN- н-енг-ен Y
СНз он
-(Ufg-CHa- H-ITj °
143
63
so (разл.)
65
60 ОН
Продолжение таблицы







| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 1-фенокси-3-аминопропан2-ола или их солей | 1973 |
|
SU563120A3 |
| Способ получения производных 1фенокси-3-амино-пропан-2-ола или их солей | 1974 |
|
SU549078A3 |
| Способ получения производных 1-фенокси3-аминопропан 2-ола | 1973 |
|
SU493958A3 |
| Способ получения производных 1-фенокси-3-аминопропан-2-ола или их солей | 1974 |
|
SU559643A3 |
| Способ получения производных 1-фенокси-3-аминопропан-2-ола | 1973 |
|
SU489309A3 |
| Способ получения производных 1-фенокси3-аминопропан-2-ола | 1972 |
|
SU487484A3 |
| Способ получения йодалкенильных соединений | 1974 |
|
SU589905A3 |
| Способ получения производных 1-фенокси -3-аминопропан-2-ола | 1972 |
|
SU457211A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ АЛКАНОЛАМИНА | 1973 |
|
SU400079A1 |
| Способ получения производных простановой кислоты | 1973 |
|
SU648088A3 |

-й-«сн-со
iH,o-/dH«/i oбНз
ЙН- еНг- CH-fi маспо
енз (
-е,(1Н-еО-пг 179-180
. Н /-HW-dO-HK- H-CHj-6K-| V HSOl A, tigHgo-engЙНз
fH енг - iH
C2HeO-dH2 teaAH
t s «iH- Co -f ti155-157
енз JS,A
-ЙН-СНг-еН-,масло
tiHjОНЛ„
ЙгНаО-бНг , ен-енгйн-, UgHgO-CHgенз омиЦгЛ
82
79-81
80
йНз СИз
68
з сн. СН, dHg .wr .
Q
78
Масло
CHj
67
(iHj енз
65
wHj
81
105-106 щ Масло, соль с 63 1/2мшвм-Ь )-ВНННОЙ {ч- -винной КИСЛОГОЙГТ. ПП. 113-118° (раэп.) т. roi. 133-134° 77 Масло, соль с 1/2 молем -(+)вшшой кислоты: т. пл. 69-70°, rffrpocKonH4Ha
Продояжеиие таблицы
- Н- г-СНу НМаспо
йНзOH jJ
СНз iH3 (iH-dO-Y 192-193
ЩУ
-си-енй-йн
NH ftO-KHсн, он
с«,о-е„.-| ;«- -Qt
-U«ftH-(iO-T,118-119
- Сн-(
4нз ЬО «-°
ензО- 6Н2-CeCH-to-f
Х
1Нг
.СН-еНа-еН-,Маспо
gO-ftHatn онЦг,
-( -Со -f 165-167
СзНт И-СО-НКiiHsА Л.
СНз СНз сн- СНг- tin -f
eJHr NH-tO NH-снз 1)нЛ«-Л
-tef- -а
/ .
О N-CO-NH.Сн- сн,- dH
( л
ч
tH,ОН / Масло
K-CO-NHПродолжение табтшы
61
75
СНз
о
76
Маспо
ЙН,
71
4нз
70
енд
82
1О7-108
83
Нз
72
70
йНз: ciHj
68
185-188
йн.
65
СН:
15598557IQ
IXТ. пп., ОС I Выход, % йНзО-/№4-0- ен,о-/(1н,/,-о СНзО-еНгt,H,0-e,H.O-«гНвО-€гН.-0бгИэО-С«Н| --0---ен-(1Нг-СН- 1н, он
(1н,о-ен,--CH-CH -eH N-j
Ьнз он WN.
tieHH-O- .(,
L
СНгОН ,..,н,о-«н,«..«- -| .н-| 0 -Си - Шг - tiH-« я.«,н,о-ен,(Нг-в- 1, U1Д
Продолжение таблицы
Маспо
CHj
Маспо iH-CH-COji 105-10681 1н О ° -СН-СНг-СН Y Сн,он f-(JH-CO ,124-125 СН-СН2- Н-7 ч 1нзОН/ СНз Сн енз снз Маспо61 СНз 106-10787 72-7489 Формула зобрегени Способ получения производных 1-фенокси -З-аминопропан-2-опа общей формулы I 0- JH«-eH- iH|-NH X Vон где X c«eH-t-(Hrti I ула - (iH-tiHj- lH(Het и. 8 HiОН где А - СН2 - апкокси; -О - алкоксиапкил -О-оксиалкил или группу -ЫН-СО-ЫК Я Е - атом водорода или метал. Het представляет собой связанный атом углерода ароматический или к в ази ароматический пяти- или шестичпенный моноцикп с 1 или 2 гетероатомами, в котором один из гeтepoaтo oв представляет собой атом кислорода, азота или серы| а второй гетероатом - атом азота, причем моиоцикп может быть еще замещен одной или несколькими метильными группами. Bi и Pj - атом водорода, алкил, алкенил, цикпоалкил или вместе с атомом азота, с которым они связаньь .а также с дополнитель ным гетероатомом кислорода или серы образуют насыщенный пяти- или.шестичленный мо ноцикл, в которых алкилостатки содержат 1- 4 атома углерода, алкоксиостаткн - 1-4 ато ма углерода,алкенилостатки - 3 или 4 атома углерода и циклоапкилостаткн - 5-7 атомов ушерода, или нос солей, отличающийс я тем, что соединение общей формулы II 2 me А - указанные значения, 2 - л наяает грутшу dH-CHa- - ;н СНг-На1 V ООН где Hat - атом Галогена, подвергоот взаимодействию с соединением общей формулы Ш ННй-Х где X имеет указанные значения, в инертном органическом растворителе при температурах от 20 С до температуры кишния применяемого растворителя с последующим вьщелением целевого продукта в свободном виде или в виде соли. Источники информации, принятые во внимание при экспертизе: 1, Пакетт Л. Основы современной химии гетероциклических соединений. Москва, Мир, 1971, стр. 32. 2 Патент Великобритании № 118.5046, л. С2С.
Авторы
Даты
1978-03-15—Публикация
1974-12-19—Подача