(54) СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛКЕТОНОВЫХ ПРОИЗВОДНЫХ
ИЛИ ИХ СОЛЕЙ -wQ JIf Иб 7 где )i/ - два атома водорода или ат кислорода; R- - атом водорода или низшая алкильная группа; R/ и R (каждый) - атом вод рода, атом галоида или низшая алкильна группа, а пунктирная линия - произвольн связь между атомами углерода, в третье и четвертом положениях пиперидинового кольца где NW два атома водорода или ато кислорода; Я - атом водорода или низшая а кильиая группа; R(- атом водорода, галоида, низ шая алкильная или низшая алкоксилышя группа (CH2) где -.атом водорода, галоида, ни шая алкильная, низшая алкоксильная или трифторметильная группа; И - целое число 0-2 или где - атом водорода, галоида, гид роксильная, низшая алкильная, низшая алкоксильная или нитрогруппа; или их солей, заключающийся в том, что соединение общей формулы где R, , R, ук подвергают взаимодействию с соединелием обшей формулы H,N-X-H,, где R, и X - аналогичны указанным, в среде и} ертного растворителя с после- дуюшям выделением целевого продукта в виде основания или переведением его в соль известными приемами. Предпочтительно проводить процесс в присутствии кислого катализатора. Реакцию обычно ведут в таком инертном растворителе, как ароматические углеводороды (например бензол, толуол, ксилол), органические кислоты (например диметил- сульфоксид), спирты (например метанол, этанол, пропанол, бутанол), эфиры (например диоксан, тетрапщрофуран, диэтиловый эфир) и т. п. В качестве кислого катализатора исиол зуют, например, минеральную кислоту (например соляную, серную, фос(}юрную), О()ганическую кислоту (например уксусную), кислоту Льюиса (нанримор хлористый цинк, хлорное олово). Можно использовать основные катализаторы, например ка()бонаты щелочного металла (ка1збонат )1атрия, карбонат калия), бикарбонат щелочного MOTajuia (например бикарбонат натрия, бикарбонат калия), гидроокись щелоч)1ого металла (например гидроокись натрия, гидроокись калия) или органический амин (например пиридин, тркэтиламин). Даже не применяя такие катализаторы, реакцию можно вести при комнатной температуре или при нагревании. i3 качестве заместителей в фенилкетоновых произвелных общей формулы I понимают под низшим алкилом такие алкилы С.,. как метил, этил, н-пропил, изопронил, н-бутил, втор.бутил и трет.бутил, под низшим алкоксилом - такие алкоксилы С „ как метокси, этокси, н-пропокси, изопропокси, }i-бутокси, втор.бутокси, трет.бутокаи, под галоидом - фтор, хлор, бром и иод, под ацилом - такие алканоилы С , как ацетил, пропионил, бутирил и валерил и бензоилы, произвольно замещенные одним или двумя заместителями из ряда водорода, галоида, гидроксила, низшего алкила, низшего алкок- сила, нитро- или трифторметила; к произвольно замешенным фенилам относятся фе1ШЛ, галоидфенил, толил и мотоксифошл; к низшим алкиленам относятся метилен, этилен, триметилен, пропилен, тетраметилен, м.етилтриметилен и бутилен. Примерами фенилкетоновых производных обшей формулы I могут служить гидразон, метилгидразон, -диметилгидразон, фонилгидразон, галоидфенилгидразон, алкилфонилгидразон, алкоксифенилгидразон, нитрофенилгидразон, трифторметилфенилгидразон, Ц К -дифенилгидразон, оксим, О-метилок- сим или семикарбазон следующих кетонов: )р-( 4-фторбензоил1 прошшЗ -4-(4-хлорфешш)-4-.оксипиперидин; 1- (2,4-дифтopбeнзoил)-пpOIШлJ -4-{4-хлорфеиил)-.4-.оксишшеридда; (2-диметиламино.4--фгорбензоил)-пропш1 J -4- (4-зслорфенил )-4-оксш1Иперидин; 1- (2-эгш1амино-4;-фторбензоил)-пропил -4-( 4-хлорфенил)-4-окси1Шперидин; 1- f-(2-aминo-4-фтo{ бeнзoшl)-пpoшtл -4-(4-хлорфенил)-4-оксипиперидии; 1- (2-aцeтaминo-4-фтopбeнзoил)-пpoпил -4-(4-хлорфенил)-4-оксипиперидин; 1- у-(2-нитро-4-фтор5ензоил)--пропилД -4-окси--4-{ 3-трифторметилфеш1л) -пиперидин; 1 )р-{4 фторбензоил)-.пропил -4-окси-4--{3-трифгоомегилфенил)-пиперидин; l-df -(2-хпор-4-фторбензоп)-пропил -4;-окси-4-(3-трифторметипфенил)-пиперидин; 1- (2,4-дифторбензоил)-пропил -4-окси-4-(3-трифторметилфенил)-пиперидии; 1- Т -(2-диметиламино-4-фгсрбензокл)-пропил3 -4-ОКСИ-4- (3-трнфтормегилфенил)-шперидЕн; (2-этиламино 4-фторбензoил)пpoпил 3-4-окси-4-{3-трифтормегилфенил)-пиперидин; (2-амино-4-фторбензоил)-пропилЗ-4-окси-4-(3-трифторметилфенил)-пиперидин; 1- (2-амино-4-фторбензоия)-пропил -4-окси- (3-трифторметилфенил)-пиперидин; 1- (2-ацегамино-4-фторбензоил)-пропил -4-окси-4-(3-трифторметилфенил)-пиперидин; (4-фгорбензоил)-пропил -1-феннл-З ,3,8-трназоспиро 4,5 j декан-4-он; 8- /у- (2,4-ди фторбензоил)-npomraj -1-фенил-i ,3,8-1-риазоспиро 4,5 декан--4-он; (2 димеги амино-4-фторбензонл)-пропил -1 фенил 1, ,3,8-триазоспиро 4,5 декан-4- он; (2-эгиламинс.4-фторбензоил)-пропил -1-фенил-1,3,8-триазоспиро 1:4,5 декан-4-он (2-аминс 4-фгорбешоил)-пропил -1 -фенил-1,3,8-триазоспнро14,5 J докан-4-он; (р-(2-ацетамино-4-фторбензоил)-пропил -1-фенил-1,3,8-триазоспиро L4,5Jдeкaн-4 -он; 1- Jp- (4-фторб ензонл )-прошш - 4- (2-кето-1-бензимидазолинил)-пиперидин; 1-1Т-(2,4-дифгорбензоил)-пропил} -4-(2-ке то-1-бензимидазолинил)-пиперидин; 1- LX -(2-амино-4-фторбензонл)-пропилj -4- (2-кего-1-бензимидазолинил)-пиперидин; -(2-ацетамино-4-фторбензоил)-пропи71 -4 - (2 -кето - 1 - бензимидазолинил) - пиперидин; .(2,4-дифтopбeнзoшr)-пpoпилJ 4-(2-кето 1-6 ензимидазолинил)-1,2,3, Ь-гетрагидропиридин; 1-f у--(4-фторбензоил -пропипГ-4- (2-кето-1 бензимидазопинип)-1 ,2,3,6-гетрагидропиридин; (4-фтopбeнзoил)-пpoг ич -4- 2-метокси(Ьенил)-пип р разин; 1- (2-амино 4-фторбензоил)-про пилJ-4-(2-мeтoкcифeIЧIл)-пиaepaзин; 1- Т -(2,4-дифгорбензоил)-прош{л J-4- (2-м&токсифеншО-пиперазин; 1- у-(4-фгорбензоил)-пропил -4-фенилпиперазин; (4- -фгорбензоил)-пропил j-4-бензил-4-оксипи- перидия; 1-1 ((4-фторбензоил)-Еропил -4- -окси-4-(4-толил)-пиперидин; 2- ( 2-аьдано-4-фторбензоил)-пропил J -1,2,3,4-гетра- гидроизо хинолин; 2- - (2,4-дифторбензоил)-пpoш лJ-l,2,3,4-гeгpaгидpoизoxииoлин; (4-фторбензоип) -пропип - 1, 2, 3, 4-тетрагидрохинопин; 1 -fv - (4 - диметип амино- 2 -фторбензоип ) -пропип - 4-оКси-4- ( 3- трифторметилфенип ) - пиперидин; 1 - f -- ( 4 - эткпам11но - 2 Лторбенэоип ) Пропил 4-окси-4-(3-трифгорметилфенил)- -пиперидин, 1- т.- (4-бeнзlшal шнo-2-фтopбeнзoил)-пpoшiл 2 -4-ОКСИ-4-(3 трнфгорме- гилфеш л)-пиперидин; 1- У-( 4-амино-2-фторбешоил)-пропил -4-окси-4--(3-грифгорметилфеш л)-пиперцдин; (4-фгорбензоил)прошшЗ -4-(4-хлор-3-трифторметилфеШ1л)-4-оксишшер1од1Н-, 1- Jf-(2,4-дифтор-. бeнзoил)-пpoл iлJ -4- (4-хлор-З-трнфторметипфенип)-4-оксипиперидкн; (2-aминo-4-фторбензоил)-пропип1-4-(4-хлор-3-трифторметнлфенил)-4-оксйпиперид ш; 1- Y-(2,4-днфгорбензоил)-пронип -4-бензил-4--оксипнперидин; 4-фгорбензоил )-пропил -4-(4--хлорбензнл)-4-окс1шиперидин; 1- Г7Г(2 ,4-дифгорбензоил)--прогшлД -4-(4- -хлор5ензил)-4-окскпнпернди11; 8- J-(2-дкметиламино--4-фгорбе;13оил)-пропил -1-феиил-Х.ЗЗ-триазоспиро декан--4-оь:; 1- У(2-димог лам но-4-фторбензоил)-пропил -4--(2-метоксифен1ш)пиперазин 1- 7Г-{2,4-дифторбензоил)-пропил 4-фе- нилпиперазин; 1- (4-фторбензоил)-пропил -4-бензилшшеразин; 1- f-(4-фторбе зоил)-пропил -.4-..окси-4-.(4-метоксифенил).„иперидин; 1-(Т--бензоияпропил)-4-окси-4-(3-трифтормет1шфенил)-пииеоидин; 8( .оилпропкл)1-(Ьешш-1,3,8-триазоспнро 4,5 декан. f- J Ei к дчесгве соединений общей формулы Н N - Х- Т, можно применять гидразин, нилгидразин, замещенный фенилгидразин, 1,1-дифенилгидразин, алкилгкдразиН;, диалкилгидразнн, гндроксиламин, семикарбазид и т.п. Эти соединения можно применять в. виде свободного ос1ювания, пщрата или соли. Фенилкегоновые производные общей формулы 1 можно про вращать в соли обработ кой минеральныки кислотами (например соляной, бромистоводородной, серно, азотной) органическими кислотами (например уксуоиой. лимонной, щавелевой; молочной, корич-
ной, винной, янтарной, аскорбиновой), галоидалкклами (например мегилхлоридом, этилхлоридом, метилбромидом, метилиодидом), , алкилтозилитами (например мегилтоаилагом, этилтчэзилатом), алкилсульфагами (например мегилсульфатом, этилсульфагом, диметил- сульфатом).
Пример 1. К смеси 1,6 г хлоргидрата 1- Jf - (2 s4-дифторбензоил)-пропил -4-(4-хлорфенил)-4-оксипиперидина и
120 мл этанола по кашшм добавляют раствор 1,2 г гидразингидрата в 30 мл этанола при комнатной температуре. Смесь нагоевают с обратным холодильником 1 ч ЗО мин при перемешивании и выпивают в ледяную воду. Выпавшие кристаллы отфильтровывают и перекристаллизовывают из водного этанола.
Получают гидразон 1-f 1(2,4-.цифторбензоил)-пропил -4-(4-хлорфенил). сипиперидина с т. пл, 172,5-174, (выход 80,5%).
Пример 2. К суспензии 4 г 1 ЕУ-{4-фторбензоил)-пропил -4-(4-хлорфенил)-4-оксипиперидина в 50 мл этанола добавляют по каплям раствор 4 г гидразингидрата в 1О мл этанола при перемешивании. Смесь нагревают с обратным холодильником 5 ч, охлаждают до KOMJiaTHOE темпе- |ратуры и выливают в ледяную воду. Осадок отфильтровывают и перекристаллизовывают из этанола.
Получают гидразон (4-(1)торбелзоил)-пропилД-4-(4-хлорфенил)-4-оксипиперидта с т, пл. 155-158°С (выход 85%).
Пример 3. К перемешиваемой смеси 3 г (4-фторбензоил)-пропил (4-хлорфенил)-4-оксипиперидина, 2,1 г хлоргидрата гидроксиламина, 15 мл воды и 45 мл этанола доба,вляют 5 г карбоната натрия. Эту смесь нагревают с обратным холодильником в течение 5 ч. После охлаждения реакционную смесь выливают медленно в лед5шую воду. Выпавшие кристаллы отфильтровывают и перекристаллизовывают из водного этанола.
Получают оксим (4-фторбензоил)-прошшJ -4-(4-хлорфенил)- 4-оксипиперидина с т.пл. 135-137°С (выход-75%).
Пример 4. Смесь 4 г (4-фторбензоил)-пропил -4-окси-4-(3-трифторметилфенил)-пиперидина, 4 г гидразингидрата и 60 мл этанола нагревают 12 ч с обратным холодильником. После охлаждеНИН реакционную смесь выливают в воду. Выпавшие кристаллы отфильтровывают и перекристаллизовываюг из этанола. I Получают гидразон 1-{ J-(4-фгopбeнзoил)-пpoпилJ -4-окси-4-(3-трифторметилфеншО-пиоеридина с т. пл. 128-131°С (вььход 83%).
Пример 5. Смесь 3,6 г I-ГT-(4-4l pбeнзoшI)пpoпилJ -4-(4-хлорфенил ) 4-оксипиперидина, 1,7 г 3-фторфенилгидразина и 6О мл уксусной кислоты перемешивают при комнатной температуре в течение 2 ч 30 мин. Полученную смесь Б,ЪЬ ливают в воду, подщелачивают и экстрагируют этилацетатом. Экстракт промывают насыщенным водным растворюм хлористого натрия, сушаг над сульфатом натрия и выпаривают при пониженном давлении. Оста&шееся твердое вещество перекристаллизовывают из этанола.
Получают З-фторфенилгидразон-1-L У-(4-фтopбeнзoил)-пpoпилJ -4-(4-хлорфенил)-4-оксипиперидина с т. пл. 174,5-175, (выход 88%).
Пример 6. Смесь ЗД г l-fjГ-(4-фторбензоил)-пронил )-4-(4-хлорфенил)-4-оксипиперидина, 1,9 г 4-хлорфенилгщьразина и 40 мл уксусной кислоты переменшивают при комнатной температуре в течение 7 ч 30 мин. Полученную смесь выливают в ледя1{ую воду и подщелачивают при перемешивании. Осадок отфильтровывают и пе- рекристаллизовывают из этанола.
Получают 4-хлорфенилгидразон 1-CT(4-фтopбeнзoил )-пропил J -4-(4-хлорфенил )-4- -оксипиперидина с т. пл. 188-190°С (выход 86%).
Пример 7. Смесь 5,0 г (2-амино-4-фторбензоил)-пропил}-4-окси- -(3-грифторметилфенил)-пиперидина, 5,0 г гидразингидрата и 60 мл этанола нагрева. ют с обратным холодильником в течение 28 ч. Реакционную смесь выливают в холодную воду, осадок отфильтровывают, промывают водой, перекрисгаллизовываюг из этанола.
Получают гидразон (2-aминo-i-фгорбензоил)-пропил - 1-окси-4-(3-три- фторметилфенил)-пиперидина с т. пл. 141- (выход 63%).
Пример 8. Смесь 2,0 г i-lf-(4-фторбензоил)-пропилJ -4-окси-4-(3-трифторметилфенил)-пиперидина, 2,1 г хлоргидрата гидроксиламина, 5,0 г карбоната натрия, 15 мл воды и 45 мл этанола нагревают с обратным холодильником в течение 7 ч ЗО мин. Полученную смесь выливают в ледяную воду и экстрагируют этилацетатом. Экстракт промывают насыщенным водным раствором хлористого натрия, сушат над безводным сульфатом натрия и выпаривают при пониженном давлении. Оставшееся твердое вещество перекристаллизовывают из диизопропилового эфира.
Получают оксим (l-Фгopбeнзoил)-u роиш J-4-окси-4-(3-трифторме тилфенил)-пииеридиыа с т. ал. 16О-162 С (выход 90%).
Примере. Смесь 1,О г l-ff-(-1-фторбс1 зоил )-про11Ил} -4-окси-4-( 3-трифгорметш1фенил)-пиперидина, 0,2 г хлористого цинка, 1,0 г М, N -днметилгидразина и ЗО мл этанола перемешивают при 40-50с в течение 30 ч. Смесь выливают в ледяную воду, иодщелачиваюг водным раствором гидроокиси аммония и экстрагируют этилацетатом. Экстракт промывают водой, сушат над безводным сульфатом натрия и выпаривают при пониженном давлении. Оставшееся твердое вещество первкристаллизовывают из водного этанола. Получают N, N -диметилгидразон 1- Jp- (4- -фторбензоил)-прош1л -4-окси-4-( 3-трифторметилфенил)-пиперидина с т. пл. 12 7 С (выход 45%).
Примеры 10-11. Аналогично примеру 8 из 1-ЕJ-(2,4-дифторбензоил)-пропил J -4-ОКСИ-4-(З-трифторметилфенил)-пиперидина получают оксим 1-1.у-(2,4 дифторбензоил)-пропил 4-окси-4-( 3-трифторметилфенил)- пиперидина, с т. пл. 133135 0 (выход 84%).
Из (4-фторбензоил)-пропил -1-фе1Ш№-153,8--триазоспиро 4,5 декан-4-он получает его оксим с т. пл. 22О 224-С (зьзход 55%).
Пример 12. Аналогично примеру 9 из (4-фторбензоил)-пропил -4- -фенилпиперазина получают его N , N -ди метилгидразон с т. пл.. 125-132,5 С (выход 53%).
Приме-ры 13-17. Аналогично примеру 4 из 8- 5-(4-фторбензоил)-проnjuij -1-фенкл-1,3,8-триазоспиро 4,5 декан-4 она получают его гидразон с т. пл. 161-166°С (выход 84%).
Из хлоргидрата ( 4-фгорбензоил)-пропил J --4-(2-метоксифешш)-пиперазина получают его гидразон с т. пл. 85,5-90°С (выход 83%).
Из (2,4-дифторбенаоил)-пропил -1-фенил-1,3,8-триазоспкро 4,5 декан-4- -она получают его гидразон с т. пл. 156°С (выход 55%).
Из (4-4торбензоил)-пропил -4-(2-кето-1-бензимидазолиннл)-пиперазина получают его гидразон с т, пл. 175 С (выход 67%).
Из (4-фторбензоил)-пропил -1,2, 3,4-тетрагидрюхинолина получают его гидразон с т.пл. (выход 75%).
Формула изобретени
1. Способ получения фен;1Л1кего1 овых изводных общей формул1л
Rb
C-A-Z
R2 N-X-R 2
где R - атом водорюда, галоида, низшая алкильная, низшая алкоксильная, акаиюнизшая алкиламино-, ди-низшая алкиламинобензиламино- или трифторметильная, группа;
RJ - атом водорода, галоида, амиНО-, ащшамино-, низшая алкиламино-, ди- -низшая алкиламино- или нитрогруппа;
R - атом водорода, низшая алкильная, карбомоильная или произвольно зам&щенная фенильная группа;
А - низшая алкнленовая группа с 2-3 атомами углерода;
X - атом кислорода или-N-R j/ где В - атом водорода, низшая алкильная или произвольно замещенная фенильная группа;
1 - одна из групп
2
-О
-R
где R - атом водорода или гидроксильная группа;
Rjj - атом водорода, фенильная или бензильная группа, причем фенильная или бензильная группа имеют произвольно один или два заместителя из ряда галоида, ниэ шего алкила, алкокси- или трифторметила в бензольном кольце
ллг
.ч
-О-
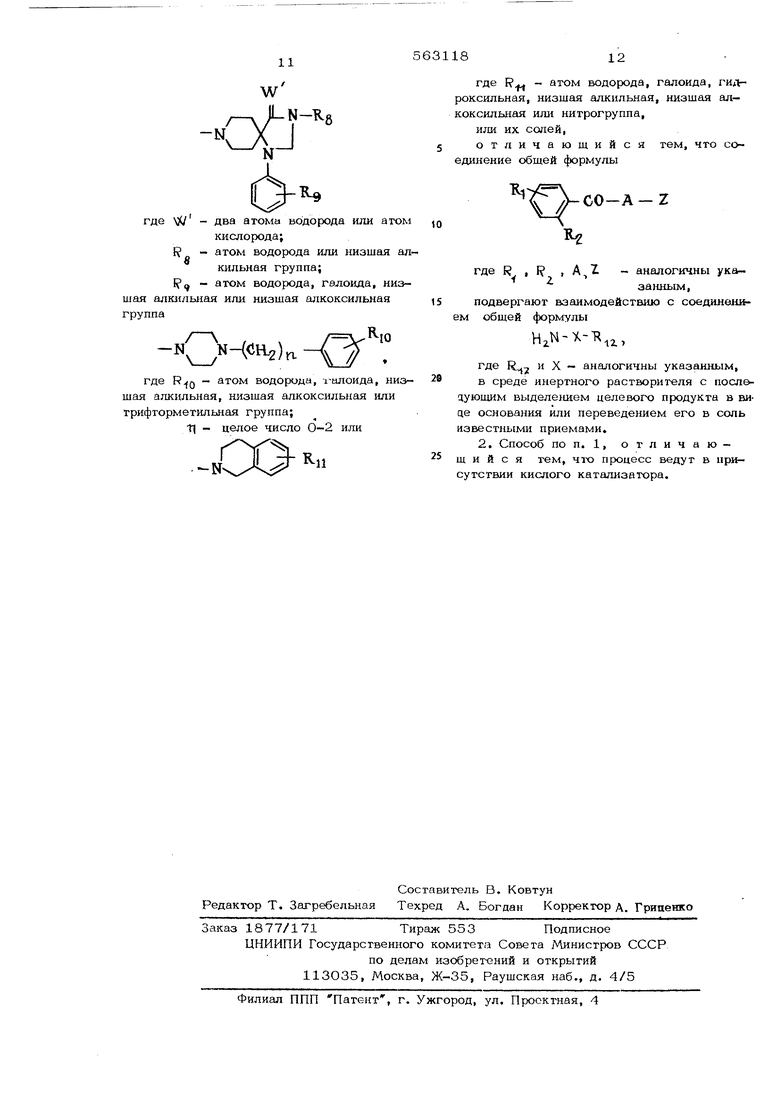
W
два атома водорода или атом
кислорода;
атом водорода или низшая ал-
клльная группа;
R, и R (каждый) - агом водорода, атом галоида или низшая алкнльиая группа, а пунктирная линия - прои.звольиая связь между атокшми углерода в трст1 ем и четвертом положениях пипери/илювого кольца
NW
- два атома водорода или агом
кислорода; R
- атом водорода или низшая алSкильная группа; I, - атом водорода, гелоида, низ1льная или низшая алкоксильная
(CR2)r.
где - агом водорода, 1-ЕШОида, низшая алкильная, низшая алкоксильная или трифторметильная группа;
tl - целое число О-2 или
.-кОО
где R - агом водорода, галоида, гидроксильная, низшая алкильная, низшая ал- коксильная или нигрогруппа,
И7Ш ИХ солей,
5огличаюшийся тем, что соединение общей формулы
СО-А
10
где R , R . А, Z - аналогичны указанным,
подвергают взаимодействию с соединением общей формулы
,
где R,2 и X - аналогичны указанным, в среде инертного растворителя с последующим выделе}шем целевого продукта в виqe основания или переведением его в соль известными приемами.
2. Способ по п. 1, отличающийся тем, что процесс ведут в присутствии кислого катализатора.




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения ацилгидразоновых соединений или их солей | 1975 |
|
SU656512A3 |
| Способ получения производных бутирофенона или их солей | 1973 |
|
SU568361A3 |
| Способ получения производных бутирофенона или их солей | 1974 |
|
SU592350A3 |
| Способ получения производных -(BTOP.АМиНО)-АМиНОбуТиРО-фЕНОНА | 1977 |
|
SU795455A3 |
| Способ получения производных арилкарбоксамидов или их солей | 1976 |
|
SU694073A3 |
| Способ получения производных 1-(бензазолилалкил)пиперидина или их солей | 1976 |
|
SU701534A3 |
| Способ получения 2,2-диарил-4-/4 -ОКСипипЕРидиНО/-буТиРАМидОВ илииХ СОлЕй | 1971 |
|
SU845776A3 |
| Способ получения производных 1-(4-арилциклогексил)пиперидина или их солей с кислотами, или их стереоизомеров | 1982 |
|
SU1099845A3 |
| Способ получения производных бутирофенона | 1970 |
|
SU459888A3 |
| СПОСОБ ПОЛУЧЕНИЯ 4-АРИЛ-1- | 1972 |
|
SU340168A1 |


Авторы
Даты
1977-06-25—Публикация
1973-06-12—Подача