(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ
БУТИРОФЕНОНА ИЛИ ИХ СОЛЕЙ
Р / VC tmcSHptooX
F , где Z- вторичная аминогруппа из числа:
jTii-т
;г-уМг (ена)п 5
где R водород или гидрокЬил; .r водород, галоид, алкил Сц,
15
,- V-H-Rj
20
водород или алкил С Cj, ;
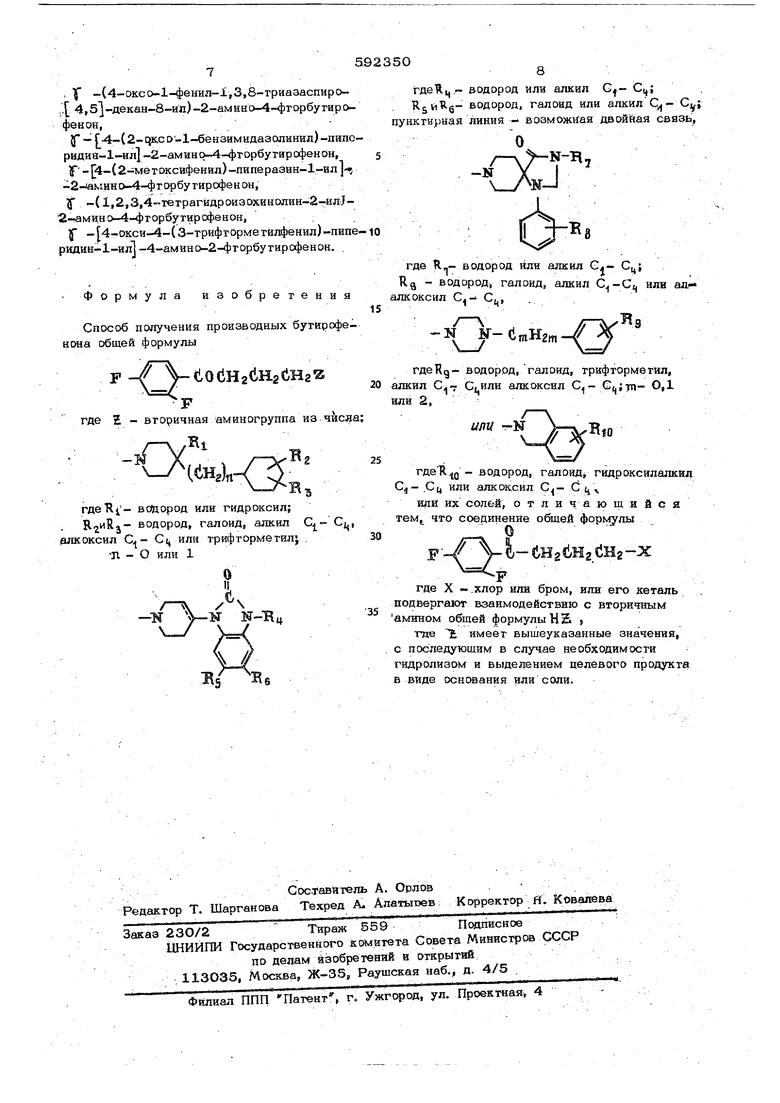
Rg- водород, гаяоид, алкил С,- С,или алкоксил Сц, rneftg-водород, талоид, грйфторметил, ялхил С - С или алкоксил С m - 0,1 или 2, где йщ- водород, галоид, гидрсжсилалкнл Сц или алкоксил С, или их солей заключается в том, что соединение обшей формулы Vb-uHg iHeeHe-: : где X - хлор или бром , или его кеталь подвергают взаимодействию с вторичным амином общей формулы Н,2, где 2. имеет ш 1шеуказанные 3 1ачений, с последующим в случае необходимости гид пизом и выделением целевого продукта в виде основания или соли, Исходные диф горбу тир офеноны можно получать взаимодействием м-дифторбензола с галоидангидридом f -галоидмасляной кислоты. Кeraли этих соединений можноjполучать, например, обработкой псхзледних этиленгликолем или этилепдитиоглкколем в присугствни катализатора дегидратации, такого, как п-гояуолсульфокислрта или концентрированная серная кислота, в среде инертного раст ворителя, например бензола, ксилола, толуо ,ла, при нагревании. Для перевода кеталя в целевые продукты проводят гидролиз в присутствии минеральной кислоты, такой, как солйная, серная ил фосфорная, или органической кислоты, такой как щавелевая, винная, при комнатной темп ратуре. Этот перевод можно осуществлять также с помощью ионообменных смол. Взаимодействие дифторбутирофенонов со вторичным амином проводят в среде инертного растворителя, например диметилформамида, бензола, толуола, ксилола, этанола, пропаЕ1Ола бутанола,ацетона, бутанона-2, 4-метилпентанона-2, в присутс;твии акцептора кислоты - неорганического или органического основания . Для ускорения реакции вводят небольшое количество катализатора, например йодистого калня. Полученное производное дифторбутирофен на можно легко превращать в аддитивные соли с органическими или неорганическими кислотами известными способами. ГIpимepa lн производных пифто1)бутирг1фвнотш являются у(4-фенигтиперипи ь.1-«л.-2,4 Д1фто бутирофенон, .(4-окси-.4 феншшштериди1ь-1-ил)-2,4 -днфтopбyтиp(Jфeнoн, (4-хло11фенил -4- oкcипипepидин- -l-илJ-2,4-дифторбутирофенон, 4-окси-.4-(3-тр19})торметш1фенил )- пиперидин-1-ил -2,4-днфторбутирофенон, - }4-окси-4- 4-метилфенил)-пш1ервди -1-ил -2,4-дифторбутиро4в оЧ| - 4-окси 4- (4-.метокси})енил )пш1ерядин- ,4-днфтортирофенон, (4-xлop-3-.тpифтopмeтилфeнил)-1- oкcипипepидин-l ил2-2,4-дифторбутирофенон, -( 4-бензил-4-оксипиперидин-1 ил )-2,4-дифторбутирофенон, (,4-хлорбензил -4-оксип1териаин - ,4-дифторбутирофенон, .4-12-оксо-1-.бензимидазопинил l-nmteриди№-1-илЗ,4-дифторбутирофе он, .12-oкco-l-бeнзимидaaoлинил)-1,2,3,6-тетрагидропирид ин 1-.И л1 2,4«-дн« фторбутирофенон, У-4 оксо-1-фенил-i 1,3,8 триазаспиро Sj-декан-8-ил-2 j4-дифторбутирофенон, -(4-фенилпиперазин- l-.,4-дифтор бутирофенон, - - 2-метоксифенил)-пйпepaзи№l- -илJ-2,4-дифторбутирофенон, Jf - (1,2,3,4-тетрагидроизохиноли в-1 ,4-дифторбутирофенон, 2f - ( 2-метилфенил -пшшразин -1-ш -2,4-дифторбутирофенон, 5- Е4-(4-фторфенил -пш1еразив .1 ил}-2,4-дифторбутирофенон , Получение исходных соединений. К смеси Хлористого алюминия (340-г) и сероуглерода (1л) добавляют 114 г м-дифгорбензола при охлаждении. Затем по каплям добавляют раствор хлорангидрид, у-хлормасляной кислоты (142,5 г) в сероуглероде (2ОО мл) при температуре ниже 15 С. Полученную смесь постепенно нагревают до кипячения, а затем нагревают при непрерывном кипячении с обратным холодильником в течение 2 ч. После охлаждения реакционную смесь выливают в воду (З л) и экстрагируют хлористым метиленом, Экстракт промывают последовательно водой, разбавленным водным раствором гидроокиси натрия и насыщенным водным раствором хлористого натрия, сушат над безводным ульфатом натрия и концентрируют.. Переонкой в вакууме Остатка получают if -хлор,4-дифторбутирофенона, г.кип. ;97-111°С/ 1хО-1,5 мм;п . 1,5О7. При кипячении смеси if-хлор-2,4-дифторутирофенона (1О2,3 г), этялеигликоля (58,1 г), гидрата п-толуолсуль сжислогы (3,2 г) и бензола (5ОО г) с обратным холодильником в гечейие 30 ч удаляют воду в вид(; азеотропа, охлаждают смесь, промьтвают ее водой и сушат над безводным суль})атом натрия. Бензольный слой концент рируют. Перегонкой получают 4-хлор-1-(2,4-дифторфенил)-,- этилендиоксибутан.т.кип. 109-12000/1,3-1,5 мм; п J 1,405. Пример, Смесь 1 хлор-2,4-д№ торбутирофенона (14,2 г), 4-(4-хлорфенил)-4-оксипиперидина (13,8 г), безводного карбоната калия (9,0 т), йодистого калия (0,5 г) и димети формамида (170 мл) нагревают в течение 20 ч при 9О-11О С. После охлаждения реакционную смесь разбавляют водой и экстрагируют эфиром. Эфирный экстракт промываю водой, сушат над безводным сульфатом натрия, обрабатывают хлористым водородом, а затем концентрируют. После растирания и перекристаллизации остатка из метанола получают хлоргидрат TГ4-(4-xлopфeнил)-4 юкст1иперидин-1- илЗ-2,4--дифторбутирофе нона, т.гш. 245°С (разл). П р и м е р 2. Смесь 4-хлор-1-(2,4-дифторфенил)-1,1этилендиоксибутана (5,3 г), 4-оксо-1-фенил-1,3,8-триазас11иро- 4,5|-декана (4,6 г) безводного карбоната калия (0,1 г) и диметилформамида (58 мл) нагревают при кипячении с обратным холодильником в течение 2,5 ч. После охлаждения реакционную смесь выливают в холодную воду (4ОО мл) при тщательном перемешивании, собирают осадо и промывают его водой. Получают 4-(4-оксо-1-фенил-1,3,8-триазаспиро-г ,5 -декан-8-ил)-г1-(2,4-дифторфенил)1,1-этилендиоксибутан. т. пл. 58-62°С. П р и м е р 3. 4-(4-окс -1-фенил-1,3,8-тр№азаспиро- 4,5 -декан-8-ил),(2,.ифтор фенил)-,1-этилендиоксибутана (2,0 г), метанола (29 мл), 35%-ной соляной кислоты (4,7 мл) и воды (1О мл) нагревают при кипячении с обратным холодильником в течение 30 мин. После охлаждения реакцио iiyro смесь разбавляют водой, подщелачиваю насыщенным водным раствором карбоната натрия и экстрагируют хлороформом. Экстракт промывают водой, сушат над безводны сульфатом натрия и концентрируют под вакуумом. Остаток перекристаллизовывают из этанола и получают jf-(4-оксо-1-фенил3,8-триазаспиро- {4,5 -дeкaн-8-ил)-2,4-ди фтopбyтиpoфeнoн, т. пл. 190-2О4°С. П р и м е р 4. По методике примеров 1-3 получают следующие соединения: 4- 4-окси- 4-( З-трифтормети/и епил)- пepидиlI-l-ил -l-(2,(4fнкл)-.l. L 8тилендиокси5утан, J- „Г4-окси-4-(3-тргвфторметилфенш)П1 перидин-1-ил1-2,4-дифторбутирофе1 он, т. пл. 90-93 С, хлоргидрят имеет т. пл. 235-23 8°С, 4- 4-(п-хло ч|1енил)-4-оксипиг1ериди11 -ил -1-(2,4-дн(}|гО()фенил)-1 ,-этилендисж сибутан, 4- 4-(2-оксо- -бенаимйдаэолинил)-пипвридин- -ил -1-(2,4-дифто{)фенил)-1,1-9тилендиоксибутан, 3 4-(2-оксо-1-бензимидазолинил)-пи.периднн-1-ил -2,4-дифторбутирО|} енон, хло)гидрат имеет т. пл. 6О- 65-С, 4-(4-фенилпиперазилин-1-ил)-1-(2,4дифторфенил)-1,1-этилендиоксибутан, 1 -(4-фенилпиперазин-1-ил)-2,4-дифторбутирофенон, дихлоргидрат имеет т. ,пл. 2 9-225°С (раал.). 4-( ,2,3,4-;тетрагидроизохинолин-2-ил)(2,4-дифторфенил7 -1, -этиленди оксибу тан, If -.(,2,3,4-тетрагндроизохинолик-2-ил)2,4-дифторбутирофенон, хлоргидрат имеет т. пл. 205-2О8 С, 4- 4-(4-хлор-3-тpифтopмeтилфeнил)-4oкcипипepидин- -ил -l-(2,4-дифтo|эфeнил)l| -этилeндиoкcибyтaн, f -4-(4-xлop-3-тpифтopмeтилфeнил)-4oкcипипepидин-l-ил-2,4-дифтopбyтиpoфeнoн, хлоргидрат имеет т. пл. 226 (разл). П р и м е р 5. Смесь Jf l -4-окси-4-(3-трифторметилфенил)-пиперидип- -ил -2-бензиламино-4фторбутирофенона (3,8 г), палладия на угле ( 1,0 г) и соляной кислоты (2,0 г);в этаноле (45 мл) тщательно перемешивают в среде водорода ггри 25 С до израсходования эквимолярного количества водорода. Катализатор отфильтровывают и фильтрат концентрируют в вакууме сполучениемхлоргндрата у -f4-окси-4-(3- тpифтopмeгилфeнил)-пипepиди№-l-илЗ-2-aмвh нo-.4-фтopбyтиpoфeнoнa, т, пл. 23О-235 С (разп). Хлоргидрат взбалтывают со смесью вогь.ного аммиака и эфира. Эфирный слой промывают водой, сушат над безводным сульфатом натрия и концентрируют в вакууме с получением свободного основания, которое перекристаллизовывают из водного этанола, т. пл. 105-107 °С. П р и м е р 6. По методике примера 5 получают следующие соединения: 1Г 4-(4-хлорфенил)-4-оксипиперйДин-1-ил| 2-амино-4-фторбутирофенон, т. пл. 45-147 °С, хлоргидрат имеет т. пл. разл.). , If -(4-ок;со-1-фенил-1,3,8-триаааспиро.. 4,5 -декан-8-ип) -2-амйно-4-4)горбугирофенон, |р -Г 4-(2-ЧКСО-1-бeнaимидaaoлинил)-пнпGpидив-l-ип -2-амино-4-фгорбугирофенОн,5 If (2- п 1етоксифенип)-пиперазин-1-ип - -2-в инo-4-фгopбyгиpoфeнDH, -(1,2,3,4 Теграгидроизохинолин-2-ил12-гамино-4-фгорбутирофенон, Tf - 4-окси- -(3-трифгормегил|)енил)-пипе-10 ридин-1-ил1-4-амино-2-фторбугирофенон. . Формула изобретения Способ получения производных бутирофенона общей формулы 1,0(1Н2 1Н2еНг где Е - вторичная аминогруппа из -О (tojn-/ ; водород ИЛИ: гидроксил; водород, галоид, алкил С |алкоксил С ц или трифторметил . 41 - О или 1 20 G|- гдеЯц- водород или алкил водород, галоид или алкил С - Cyj нктирная линия - возможная двоййая связь, -/-ЛМ-Т17 JfJ где R-- водород или алкил g - водород, галоид, алкил , или аякокснл Сц -N -imHgm гдеRg- водород, галоид, трифгорметил, кил Сцили алкоксил Cj i-pi- ОД или N isR jg - водород, галоид гидрокснлалкид C или алкоксил С i или их солей, отличающийся теМ( чго соединение обшей формулы Q / |( СНг-X где X .хлор или бром, или его кетаяь подвергают взаимодействию с вторичным амином обшей формулы Н S где IL имеет вышеуказанные значения, с последующим в случае необходимости гидролизом и выделением целевого продукта в виде основания или соли.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных бутирофенона или их солей | 1973 |
|
SU568361A3 |
| Способ получения производных 1,3,8-триазаспиро-/4,5/-декан4-она | 1976 |
|
SU656519A3 |
| Способ получения фенилкетоновых производных или их солей | 1973 |
|
SU563118A3 |
| Способ получения 8-бензофурилметил1,3,8-триазаспиро-/4,5/-деканов | 1972 |
|
SU442597A1 |
| Способ получения ацилгидразоновых соединений или их солей | 1975 |
|
SU656512A3 |
| Способ получения производных 1-(бензазолилалкил)пиперидина или их солей | 1976 |
|
SU701534A3 |
| Способ получения производных арилкарбоксамидов или их солей | 1976 |
|
SU694073A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БУТИРОФЕНОНА | 1973 |
|
SU404242A1 |
| Способ получения производных -(BTOP.АМиНО)-АМиНОбуТиРО-фЕНОНА | 1977 |
|
SU795455A3 |
| Способ получения производных 1-(4-арилциклогексил)пиперидина или их фармацевтически пригодных солей или их стереоизомерных форм | 1981 |
|
SU1095878A3 |


Авторы
Даты
1978-02-05—Публикация
1974-12-13—Подача