СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ХИНОЛИНА
(54) ИЛИ ИХ СОЛЕЙ


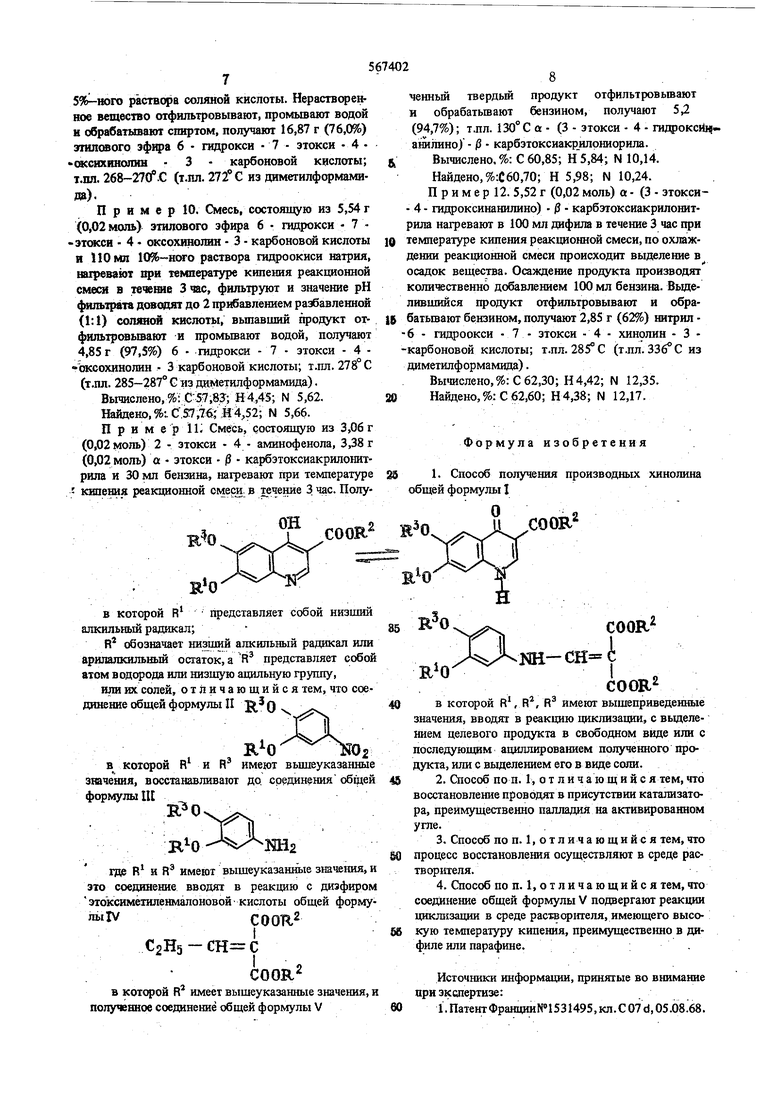

Изобретение касается способа получения новых 1ФОИЗВОДНЫХ хинолина общей формуль I, которые могут применяться в качестве промежуточных продуктов при синтезе известных фармакологически
активных соединений, а именно сложных эфиров 6,7 - диалкоксихинолин-карбоновых кислот, а также в качестве лекарственных препаратов, содержащих эти соединения. В общей формуле,
значительно ограничивает возможности осуществления перекристаллизации (1.
При осуществлении предлагаемого способа новые соединения формулы I получают в результате того, что соединения общей формулы
п
N02
в которой R и R принимают вышеуказанные для этих символов значения, подвергают восстанов жнию До соедине1 шй общей формулы
в кспарок R и R принимают вышеуказанные для зтих символов значения, полученное соедине1ше вводят в реакцию с диалкиловым зфиром зтоксиметиленмалоповой кислоты, соответствующим общей формуле
СООЯ
CsHs
IV
COOR
в которой R принимает выщеуказа1шые для этого символа значения, и полу«нные соединения общей формулы
COOR
NH-CH CV
COOR2
1 13
в которой R , R и R принимают вьпиеуказанные для этих символов значения, вводят в реакцию циклизадии.
В общей формуле I R представляет собой линейный или разветвленный алкильный радикал, содержащий в своем составе 1-4 атома углерода, преимущественно зтильный радикал.
R представляет собой линейный или разветвленный алкильный радикал, содержащий 1-4 атома углерода, преимуществешю этилыый радикал и, кроме того, арилалкильный остаток, предпочтительно бензильный;
R обозначаеТ|атом водорода или низший ацильный остаток.
Восстановле1ше соответствующих общей формуле П соединений проводят преимущественно в присутствии катализатора, главным образом в присутствии палладия на активировашюм угле при атмосферном давлешш или более высоком давлении.
При восстановлении ацильных производных реакцию проводят преимущественно в среде растворителя, в качестве которого наиболее целесообразно применять этиловый эфир уксусной кислоты.
Восстановление фенолов, соответствующих общей формуле Л (R обозначает атом водорода), наиболее благоприятно проводить в водной соляной кислоте или в смеси, состоящей из водного раствора соляной кислоты и уксусной кислоты.
Реакцию конденсации восстановленного соединения общей формулы Hi с соединением, отвечающим общей формуле IV, в том случае, когда R представляет собой ацильный остаток, преимущественным образом проводят в среде растворителя при
температуре кипения реакционной смеси, причем в качестве растворителя используют, например, зтиловый эфир уксусной кислоты.
Если соединение общей формулы 111 представляет собой гидроксильное соединение, то его вводят в реакцию конденсации с соединением общей формулы IV также в среде растворителя, причем реакцию осуществляют при нагревании. В качестве растворителя наиболее предпочтительно использовать бензин в качестве разбавителя. Реакция также
может бьггь осуществлена в расплаве без использования разбавителя.
Если реакцию соответствующего общей формуле III гидроксильного соединения с производным малоновой кислоты осуществляют в расплаве без
.использования растворителя, то нет необходимости производить выделение соединения, отвечающего общей формуле V, а реакционную смесь непосредственно вводят в реакцию циклизации, осуществляемую в дифиле при температуре 250° С.
В соответствии с другим вариантом осуществления предлагаемого способа реакцию циклизации соединений общей формулы V, в которых R представляет собой атом водорода, проводят в
среде растворителя, представляющего собой смесь серной и ангидрида уксусной кислот. В этом случае способное конденсироваться соединение растворяют в ангидриде уксусной кислоты и к приготовленному раствору прибавляют по каплям серную кислоту. В процессе прибавления по каплям серной кислоты реакционная смесь нап)евается примерно до температуры 60° С. При указанной TeNmepaType реакционную смесь перемелпшают в течение 10 мин. Непосредственно после этого реакционн ю
смесь выливают в воду, в результате чего происходит выделе1ше в осадок продукта.
Пример 1. 22,52 г (0,1 моль) 4 - ацетокси - 3- этоксинитробензола растворяют в 225 мл этилового эфира уксусной кислоты и в присутствии 5 г
палладия па активирова1шом угле производят гидpHpoBajme при давлении 5-Шатм. После поглошешя рассчита1М()Го количества водорода отделяют катализатор фильтрованием, и реакционную смесь упаривают досуха. При охлаждсмши выпавший 4 ацетокси - 3 - этоксиапилии фильтруют на нутчА фильтре, промывают холодным этиловым спиртом. Выход 86%. Вычислено, %: С 61,53; Н6,71; N7,17. Найдено, %: С 61,30; Н6,40; N6,81. П р и м е р 2. 25,4 г (0,13 моль) 4 - ацетокси 3 -этоксианилина растворяют в 250 мл этилового эфира уксусной кислоты и к приготовленному раствору прибавляют 32,4 г (0,15 моль) диэтилового эфира этоксиметиленмалоновой кислоты. Реакционную смесь нафевают при температуре кипения 3 час и упаривают досуха. По охлаждении закристаллизовавишйся продукт фильтруют на нутчфильтре, промьтают холодным спиртом, получают 91% этилового эфира 4 - ацетокси 3 - этоксианилинометиленмалоновой кислоты; т.пл. 102°С. Вычислено, %: С 59,17; Н 6,54; N 3,83. Найдено, %: С 59,3; Н 6,50; N 3,91. П р и м е р 3. 35,45 г (0,1 моль) диэфнра 4 -ацетокси - 3 - этоксиа1{илинометиленмалоновой Г кислоты в течение 60 мин нагревают при температуре кипения реакдаонной смеси в 365 мл дифила. Постепенно из раствора вьщеляется в осадок продукт. Суспензию охлаждают, разбавляют 350 мл бензина и непосредственно после этого производят фильтрование. Полученный продукт промывают на нутч-фильтре бензином. В результате с выходом 95% получают плавящнйся при температуре 300° С с разложением этиловый эфир 6 - ацетокси - 7 -этокси- 4- оксихинолин - 3-карбоновой кислоты. После перекристаллизации из диметилсульфоксида температура плавления продукта составляет 310°С. Вычислено, %:С60,18; Н 5,36; N4,38. Найдено,%: С 60,20; Н5,16; N432. П р и м е р 4. Способом, аналогич1гым описанному выше, из примененного вместо этиловогоэфира этоксиметиленмалоновой кислоты бензилового эфира этоксиметиленмалоновой кислоты получают соответствующее бен;зильное эфирное соединение. 4 - ацетокси - 3 - з oкctta ШIШll вводят в реакцию в среде этилового эфира уксусной кислоты с дибензиловым эфиром этоксиметиленмалоновой кислоты и получе1шое соединение после упаривания реакционной смеси без выделения тотчас вводят в реакцию циклизации в дифиле, получают бензиловый эфир 6 - ацетокси - 7 - этокси - 4 -оксохинолин - 3 - карбоновой кислоты; т.пл. 260 С (с разложением). После перекристаллизации из диметилсульфоксида т.пл. 265°С (с разложёнием). Вывдслено,%: С 66,14; Н 5,02; N 3,67. Найдено,%: С 65,80; Н 5,27; N3,78. П р и м е р 5. 18,31 г (0,1 моль) 2 - этокси - 4 -нитрофенола по.таергают восстановле ию в смеси, состоящей из 180 мл воды, 10 мл ко1щентрированной соляной кислоты и 50 мл уксусной кислоты, причем реакцию проводят в присутствии катализатора, представляющею оо()ой палладий на угле. После отделения посрсдство.м фильтрования катализатора значение рН реакционной смеси доводят до б посредством прибавления 10%-ного раствора углекислого натрия. Выделившееся в осадок вещество отфильтровывают, промывают водой н вепосредственно после этого обрабатывают аоетож, получают 13,6 г (89%) 2 - этокси - 4 амякофенола. Вычислено,%: С 63,73; Н 7,23; N9,14. Найдено,%: С62,22; Н7,18; N 9,08. П р и м е р 6. 1531 г (0,1 моль) 2 этсясся 4 аминофенола и 26,0 г (0,12 моль) эфира этоксиметиленовой кислоты нагревают в течение двух часов на водяной бане, к реакционной массе прибавляют 30 мл бензина и смесь нагревают при температуре кипения с обратным холодильником в течение .2 час. При охлаждении из двухфазной смеси вьшадает вещество, которое отфильтровывают и промывают бензином, получают 27,78 г (86%) зфира 4 - гидрокси - 3 - этоксианилкнометиленмалоновой кислоты; т.пл. 80° С. Вычислено, %: С 59,43; Н 6,54; N 4,33. Найдено,%: С 59,57; Н6,61; N4,30. П р и м е р 7. г (0,06 моль) этилового эфира 4 - гидрокси - 3 - этоксианилинометиленмалоновой кислоты нагревают в течение 30 мии в 190мл дифила при температуре 250° С, реакционную смесь охлаждают и полученный в результате реакции циклизации продукт переводят в осадок посредством добавления 190 мл бензина. Полученный продукт промывают на фильтре бензином, получают 14,8 г (89,3%) этилового эфира 6 - гидг рокси - 7 - этокси - 4 - оксохинолин - 3 - . карбоновой кислоты; т.пл. 266° С. После перекристаллизации из диметилформамида т.пл. 270-272 С. Вычислено,%: С 60,64; Н 5,45; N 5,05. Найдено, %: С 60,24; Н 5,55; N 5,04. П р и м е р 8.4,59 г (0,03 моля) 2 - этокси - 4 минофенола и 10,52 г (0,031 моль) дибензилового эфира этоксиметиленмалоновой кислоты нагревают в течение 4 час на водяной бане при температуре 10(f С, прибавляют 50 мл дифила и массу в течение 60 мин нагревают при температуре 250° С, по охлаждении смецшвают с 50 мл бензина, вьщелившийся в осадок продукт отфильтровывают и промьша- ; ют спиртом, получают 3,4 г (50,2%) бензилового эфира 6 - гидрокси - 7 - этокси - 4 - оксохинолин - 3- карбоновой кислоты; т.пл. 25 С. Вычислено,%:С67,25; Н 5,05; N4,13. Найдено,%: С 66,76; Н4,88; N 4,37. П р и м е р 9. Смесь, состоящую из 25,52 г (0,08 моль) этилового эфира 6 - ацетокси - 7 этокси - 4 - оксихинолин - 3 - карбоновой кислоты, 2000 мл этилового спирта, 200 мл воды и г (2,4 моль) кислого углекислого калия, нагревают при температуре кипения в течегше I час, растворитель удаляют в вакууме и полученную густую . суспензию смешивают с 2000 мл воды. Нерастворивщееся вещество отфильтровьшают и находящийся на нутч-фильтре во влажном состоянии продукт суспендируют в 200 мл воды. Значение рН приготовленгюй суспензии доводят доЗ добавлением
Авторы
Даты
1977-07-30—Публикация
1974-08-27—Подача