(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ КСАНТЕНА
i
Изобретение относится к способу получения новых соединений, которые могут найти применение в медицине.
Известны методы окисления 8 -функций до сульфоксидов.
Цель изобретения - разработка способа получения новых биологически активных соединений.
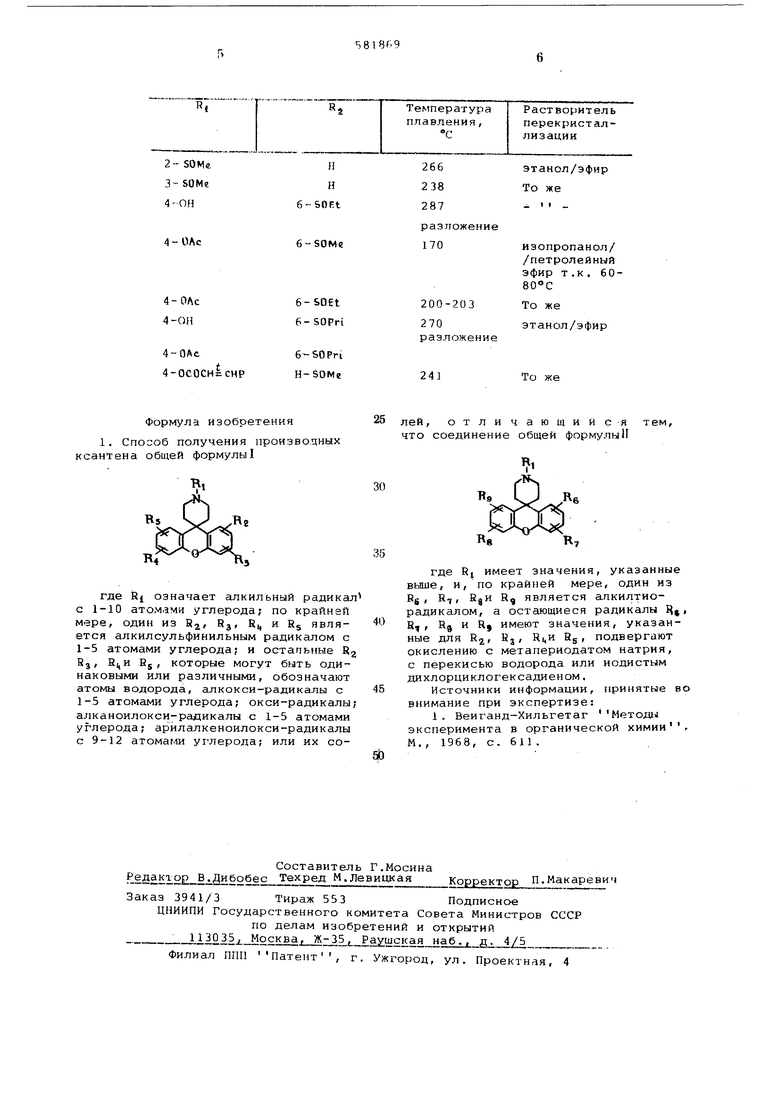
Эта цель достигается применением известного метода окисления для синтеза производных ксантена общей формулы
(1)
де R( означает алкильный радикал с 1-10 атомами углерода; по крайней меэе, один из R, Rj, йц и RS является глкилсульфинильным радикалом с 1-5 атомами углерода и остальные R, R, R и Rj , которые могут быть одинаковыми или различными, обозначают атомы водорода, алкокси-радикалы с 1-5 атомами углерода;Iокси-радикалы«
алканоилокЬи-радикалы с 1-5 атомаьш углерода; арилалкеноилокси-радикалы 9-12 атомами углерода; или их солей.
Способ получения указанных выше соединений заключается в том, что соединение общей формулы
подвергают окислению в присутствии метапериодата натрия,перекиси водорода или йодистого дихлорциклогексадиена.
Целевой продукт выделяют в свобод ном виде или в виде кислотно-аддитив ной соли.Фармацевтически приемлемой кислотно-аддитивной солью является, например, хлоргидрат бромгидрат, фогфат или сульфат или цитрат, ацетат, малеат или оксалат
Пример 1.
Смесь 0,5 г 4-метокси-1-метил-6-(метилтио)-ксантен-9-спиро-4-пиперияина и водного метапериодата натрия
(5 мл в 0,5 М растворе) перемешивают до получения раствора. Реакционную смесь добавляют к водному бикарбонату натрия и экстрагируют этилацетатом. Этилацетат выпаривают и основно органический остаток превращают в гидрохлорид, получая 4-метокси-1-метил-6-метилсульфинилксантен 9-спиро-4-пиперидингидрохлорид (Т.пл, 183-185 C) перекристаллизацией из этанол/эфира,
4-Метокси-1-метил-6- (метилтио) -ксантен-9-спиро-4-пиперидии, используемый как исходный продукт, может быть получен следующим образом.
Смесь 9,5 г 2,5-дихлорбензойной кислоты 7,4 г 2-метоксифенола и l,0ir медной бронзы добавляют к раствору метилата натрия в метаноле, полученному из 2,53 г натрия и 50 мл метанола. Избыток метанола выпаривают из 50 мл 1,2-дихлорбензена, добавляют к остатку. Смесь перемешивают и нагревают в течение 2,5 ч.
Смесь охлаждают, подкисляют 3 к. соляной кислотой, фильтруют, чтобы удалить медную бронзу и экстрагируют хлороформом. Органический слой отде-ляют и экстрагируют насыщенным раствором гидрокарбоната натрия. Экстрак гмдрокарбоната натрия подкисляют. Осадок отфильтровывают, растворяют толуоле и раствор подвергают действию угля, фильтруют и растворитель выпаривают. Остаток перекристаллизовывают из смеси толуол - петролейный эфир (т.кип. 60-80°С), получая 5-хлор-2-(2 -метоксифенокси)-бензойную кислоту, т.пл. 115-118°С.
Смесь 15 г 5-ХЛОР-2-(-2 -метоксифенокси)-бензойной кислоты и 75 г полифосфорной кислоты нагревают,на паровой бане в течение 3 ч. Смесь выливают в 10 н. раствор хлористого аммония и осадок фильтруют. Сушат и перекристаллизовывают из толуола, получая З-хлор-5-метокси-ксантон, т.пл, 201-202 С.
Спустя час реакционную смесь выливают в воду и экстрагируют эфиром, после отгонки которого получают 5-метокси-3-(метилтио)-ксантон, т.пл. 201-203°С, который перекрисгаллизовывают из метанола.
5-Метокси-3-(метилтио)- ксантон затем восстанавливают раствором борантетрагидрофуранового комплекса в тетрагидрофуране, чтобы получить ксантен, который перекриста тлизовывают из метанола, и идентифицируют инфракрасным спектром.
Этот замещенный ксантен затем подвергают реакции с N -метилди-12-хлорэтил/амином в диметилсульфохлориде в присутствии метилсульфинилметила натрия, чтобы получить 4-метокси- l-метил-б- (метилтио)-ксантен-9-спиро-4-пиперидин, выделяют в виде гидрохлорида (т.пл. 112-114°С), перекристаллизованного из этанол/эфира.
П р и м е р 2. Используя методику примера 1, берут эквивалентное количество 4-окси-l-метил-б- (метилтио) -ксантен-9-спиро-4-пиперидина, как исходное вещество, и получают таким образом 4-окси-1-метил-6-метилсульфинилксантен-9-спиро-4-пиперидин гидрохлорид полугидрат, т.пл. 282-283
Таким «е образом можно провести процесс с использованием перекиси водорода в уксусной кислоте или йодистго дихлорциклогексадиена в водном пиридине в качестве окисляющего агента
4-Окси-1-метил-б- (метиптио) -ксантен-9-спиро-4-пиперидин, как исходны продукт, может быть использован для получения диметилата 4-метокси-1-метил-6- (метилтио) -ксантён- 9-спиро-4-пиперидина с избытком трибромистого бора в метилен хлориде при минус
Продукт выделяют в виде гидрохлорида . 27б-277°С, перекристаллизовывают из этанол/эфира.
Примерз. Используя методику примера 2, берут подходящее исходное соединение и получают соединение следующей формулы;
Суспензию 5 г З-хлор-5-метокси-ксантона (5 г) в диметилформамиде добавляют к раствору избытка тиометоксида натрия в диметилформамиде, полученному ия метилмеркаптана и гидрида натрия.
RI-HCI
6-bOEt б- SOPri
6-SOPri H-SOMe
/петролейный эфир т.к. 60вО С
То же
этанол/эфир
24
То же
Формула изобретения 1, Способ получения производных ксайтена общей формулы
где К| означает алкильный радикал с 1-10 атомами углерода; по крайней мере, один из К, Нз RI, и Rj является алкилсульфинильным радикалом с 1-5 атомами углерода и остапьные Rg Bj, КцИ BS, которые могут быть одинаковыми или различными, обозначают атомы водорода, алкокси-радикалы с 1-5 атомами углерода; окси-радикалы; алканоилокси-радикалы с 1-5 атомами углерода; арилалкеноилокси-радикалы с 9-12 атомами углерода; или их со25 лей, отличающийся
тем. что соединение общей формулы
где RI имеет значения, указанные выше, и, по крайней мере, один из Kg, а,, R, является апкилтиорадикалом, а остающиеся радикалы Ч. В-, Hg и R, имеют значения, указанные для Rj, Hj, Нци Rg, подвергают окислению с метапериодатом натрия, с перекисью водорода или йодистым дихлорциклогексадиеном.
Источники информации, принятые во внимание при экспертизе:
1 . Веиганд-Хильгетаг Методы эксперимента в органической химии М. , 1968, с. 611.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 7-азабензимидазо-лОВ или иХ СОлЕй | 1978 |
|
SU795478A3 |
| Способ получения N-/4-пиперидинил/бензамидов, их фармацевтически приемлемых солей присоединения кислоты, стереоизомерных форм или N-оксидов | 1988 |
|
SU1625331A3 |
| Способ получения производных пиримидона-4 или их кислотно-аддитивных солей | 1979 |
|
SU999971A3 |
| Способ получения амидинов или их фармацевтически приемлемых солей | 1989 |
|
SU1826969A3 |
| Способ получения гетероциклических спиросоединений или их солей | 1974 |
|
SU508191A3 |
| Способ получения проивзодных бензимидазола или их солей | 1975 |
|
SU581866A3 |
| Способ получения производных аминопропанола или их солей, рацематов или оптически-активных антиподов | 1975 |
|
SU586835A3 |
| Способ получения хинолонов | 1980 |
|
SU1124886A3 |
| Способ получения производных пиперидина или их солей | 1973 |
|
SU522796A3 |
| Способ получения производных 2-аминопиримидона | 1979 |
|
SU944504A3 |


Авторы
Даты
1977-11-25—Публикация
1975-12-25—Подача