Н2$
CFjdOOH
с «Не
+
бНз
-f
IIU
6Hs
СГдСОО
(1,НзСООН
НбЮ CgHs
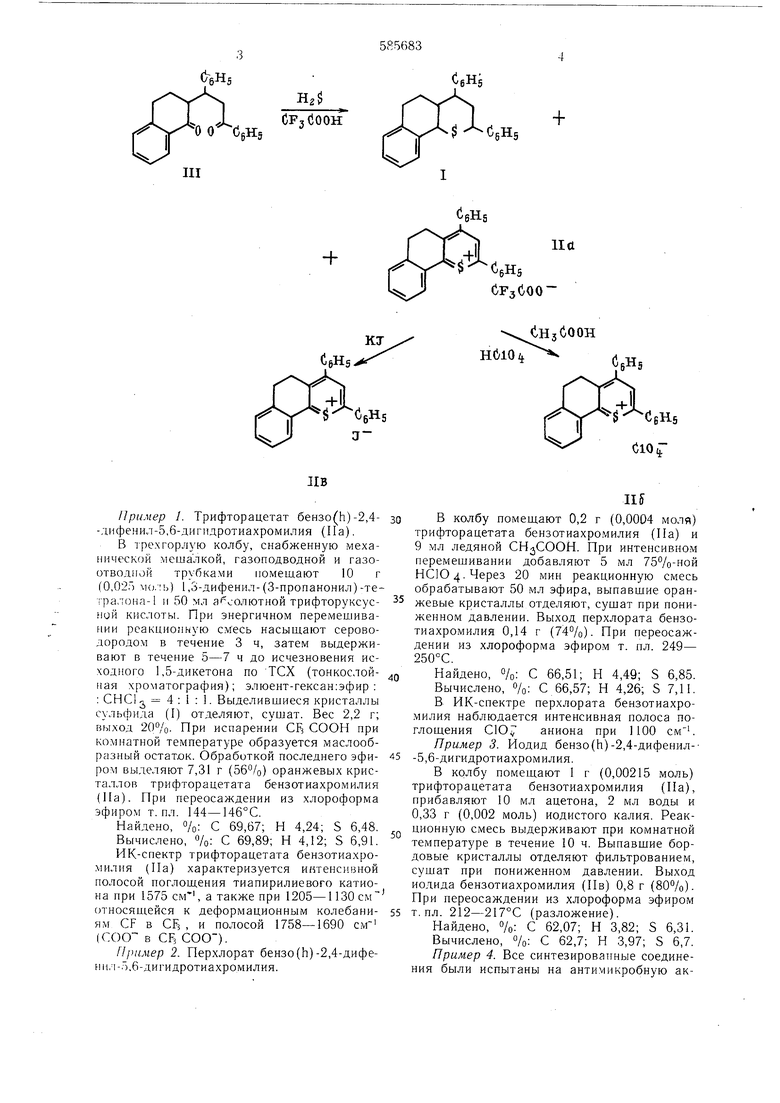


Пример 1. Трифторацетат бензо(Ь)-2,4-дифенил-5,6-диг11дротиахромилия (На). В 7ре.хгорлую колбу, снабженную механической мешалкой, газоподводной и газоотводной трубками помещают 10 г (0,02Г) vi(j.;b) 1,3-дифенил-(3-пропанонил)-тетралона-1 и 50 мл а оолютной трифторуксусной кислоты. При энергичном перемешивании реакннонную смесь насыщают сероводородом в течение 3 ч, затем выдерживают в течение 5-7 ч до исчезновения исход}1ого 1,5-дикетона по ТСХ (тонкослойная хроматография); элюент-гексан:эфир : : CHClj, 4:1:1. Выделивщиеся кристаллы сульфида (I) отделяют, сушат. Вес 2,2 г; выход 20/о- При испарении CR СООН при комнатной температуре образуется маслообразный остаток. Обработкой последнего эфиром выделяют 7,31 г (56%) оранжевых кристаллов трифторацетата бeнзoтиaxpoмИv ия (На). При переосаждении из .хлороформа эфиром т. нл. 144-146°С. Найдено, %: С 69,67; Н 4,24; S 6,48. Вычислено, %: С 69,89; Н 4, 2; S 6,91. ИК-спектр трифторацетата бензотиахромилия (Па) характеризуется интенсивной полосой поглощения тиапирилиевого катиона при 1575 см , а также при 1205-1130 см относящейся к деформационным колебаниям CF в СРз , и полосой 1758-1690 с. (СОО в CF, СОО). Пример 2. Перхлорат бензо(Ь)-2,4-дифенп,ч-5.6-дигидротиахромилия. В колбу помещают 0,2 г (0,0004 моля) трифторацетата бензотиахромилия (Па) и 9 мл ледяной . При интенсивном перемешивании добавляют 5 мл 75%-ной нею 4-Через 20 мин реакционную смесь обрабатывают 50 мл эфира, выпавщие оранжевые кристаллы отделяют, сушат при пониженном давлении. Выход перхлората бензотиахромилия 0,14 г (74%). При переосаждении из хлороформа эфиром т. пл. 249- 250°С. Найдено, %: С 66,51; Н 4,49; S 6,85. Вычислено, %: С 66,57; Н 4,26; S 7,11. В ИК-спектре перхлората бензотиахромилия наблюдается интенсивная полоса поглощения С1О аниона при 1100 см . Пример 3. Иодид бензо(Н)-2,4-дифенил--5,6-дигидротиахромилия. В колбу помещают I г (0,00215 моль) трифторацетата бензотиахромилия (Па), прибавляют 10 мл ацетона, 2 мл воды и 0,33 г (0,002 моль) йодистого калия. Реакционную смесь выдерживают при комнатной температуре в течение 10 ч. Выпавщие бордовые кристаллы отделяют фильтрованием, сущат при пониженном давлении. Выход иодида бензотиахромилия (Пв) 0,8 г (80%). При переосаждении из хлороформа эфиром т. пл. 212-217°С (разложение). Найдено, %: С 62,07; Н 3,82; S 6,31. Вычислено, %: С 62,7; Н 3,97; S 6,7. Пример 4. Все синтезированные соединения были испытаны на антимикробную активность и показали высокую активность в отношении стафилококков и грибов рода Кандида. Результаты приведены в таблице. Противостафилококковая активность подтверждена на 10 клинических штаммах, обладаюших множественной антибиотикорезистентностью (минимальные бактериостатические концентрации равны 0,78-3 мкг/мл). Соли бензо(Ь)-2,4-дифенил-5,6-дигидроти ахромилия проявляют также фагостатическое действие. Добавленные в систему фагбактерии в концентрации 300-700 мкг/мл они полностью задерживают размножение ДНК-содержащего Т-6-фага на Е. соИ В и РНК-содержащего фага f-2 на Е. соИ HfrC. Синтезированные соединения повышают чувствительность стафилококков и кишечных Анти.микробная активность солей
Минимальные бактериостатические конценграции,
Формула изобретения, Соли бензо(h) -2,4-дифенил-5,6-дигидротиахромилия обц;ей формулы
(ieHs мкг/мп
где X - CFsCOO, СЮ. или J . проявляющие активность против стафилококков и грибов рода Кандида.
Источники информации, нринятые во внимание при экспертизе:

Авторы
Даты
1978-10-15—Публикация
1976-06-01—Подача