(54) ДИПЕРХЛОРАТЫ 3,5-ДИМЕТИЛ-2,6-ДИФЕН1Ш-4- (ОКСНАЙИПАММОНИЙ) -ТИМШРтИЯ .ПРОЯВЛЯЮЩИЕ АНТИСТАФИЛОКОККОВУЮ АКТИВНОСТЬ и СПОСОБ их ПОЛУЧЕН1И жении Сд солей тиапирилия в результате реакции нуклеофильного замещения с ароматическими аминами L2 J. Однако даиньй способ отличается очень большой длительностью процесса. Реакции нуклеофильного замещения Тиапирилиевых солей с аминоспиртами в литературе не описаны и осуществлены впервые. Диперхлорат 3,5-диметил-2,6-дифенш1-4-(оксиалкиламмоний)-тиапирилия при И 2, X ) получают из перхлората 3,5-диметил-2,6-дифенилтиапирилия формулы ,НэС СНз хк НзОб § )бН5 в результате реакции нуклеофильного - замещения в незанятое положение С тиапирилиёвой соли с диметила 4иноэтанолом.-Реакция протекает в растворе абсолютного диоксана;при комнатной температуре в присутствии небольших количеств хлорной кисло,ты. Роль нуклеофила выполняет кисл род гидроксильной группы, роль основания-третичный азот. Диперхпораты 3,5-диметил-2,6-дифенил-Д-(оксиалкиламмоний)-тиапирилия указанной выше ФОРМУЛЫ пои. V 3, К-Н (15) и к / HjO Н R H3O-C H9{IB) получают аналогично ,соединению Га из перхлората 3,5-диметил-2,6-дифенилтиапириЛИЯ в результате взаимодействия с 3-(-метил-2-цирролидил }-пропанолом-1 и 3-б-метил-З-изобутил-Зпирролидил) -цропанолом-1. Пример 1. Диперхлорат 3,5диметил-2,6-дифенил-4- (1-оксиэтилдиметиламмоний)-тиап11;рилия С.1э ). К 1 г (2,7 ммоль) перхлората 3,5-диметил-2,6-дифенилтиапирилия в 15 мл абсолютного диоксана прикапывают раствор 0,24 г (2,7 ммоль) диметиламиноэтанола в 5 мл абсолютного диоксана. Смесь перемешивают в течение 3 ч. Затем к ней добавляют 40 мл абсолютного, эфира и прикапывают при перемешивании несколько капель 70%-ной хлорной кислоты до прекращения вьщеления кристаллов. Выпавщие кристаллы отделяют, промывают эфиром. Выход продукта 0,85г (57%), т.пл. I 11-1 1 ( переосажден эфиром из дихлорэтана). Найдено,%: С1 12,31; N 2,38; S 5,61, .OgNSCl2. Вычислено,%: С1 12,52; М 2,49-; S 5,68. Пример 2. Диперхлорат 3,5диметил-2, 6-дифенил-4- L ( 1 -оксипропил-3- (l1-метил-2-пирр6лидиний) тиапирилияК 1,5г (3,9 ммоль) перхлората . 5-диметил-2,6-дифенилтиапирилия в 10 мл абсолютного диоксана прикапывают цри перемешивании раствор 0,57г (3,9 ммоль) 3-(l-мeтил-2-пиppo лидил)-пpoпaнoлa- 1 в 8 мл абсолютного диоксана. Через 2 ч в реакционную смесь добавляют 30 мл абсолютного эфира и прикапывают при перемешивании несколько капель 70%-ной хлорной кислоты для прекращения выделения кристаллов. Осадок отфильтровывают и промывают эфиром. Выход диперхлората 3,5-диметил-2,6-дифенил-4- 1-оксипропил-3-(1-метил-2-пирролидиний)1,4 г (61%) ,т.пл. 156-157с переосажден эфиром из дихлорэтана Найдено,%: С1 11,60; N 2,50; S 5,39 C,2 -fH OgNSCl,2 л Вычислено,%: С1 11,47; N 2,26;S 5,17. Пример 3. Дипер.хлорат 3,5диметил-2,6-дифенил-4- 1-оксипропил-3- О1-метил-5-изобутйл-2-пирролидиний) j - тиапирилй { . (1 б). К 2г (5,4 ммоль) п-ерхлората 3j5-диметил-2,6--дифенилтиапирилия в 18 мл абсолютного диоксана прикапывают при перемешивании раствор 1,07г (5,4 ммоль) 3- (l -метил-5-изобутил2-пирроллидид -пропанола-1 в 10 мл абсолютного диоксана. Через 2,5 ч в реакционного смесь добавляют 100мл абсолютного эфира и прикапывают при перемешивании несколько капель 70%-ной хлорной кислоты до прекращения выделения кристаллов. Осадок отфильтровывают и промывают эфиром. Выход продукта 1,5 г (65%), т.пл. переосажден из дихлорэтана). Найдено,%: С1 10,02; N2,14; S 4,36 ,OQNSClz
Вычислено,%:С1 10,53; N 2,07; S 4,78.
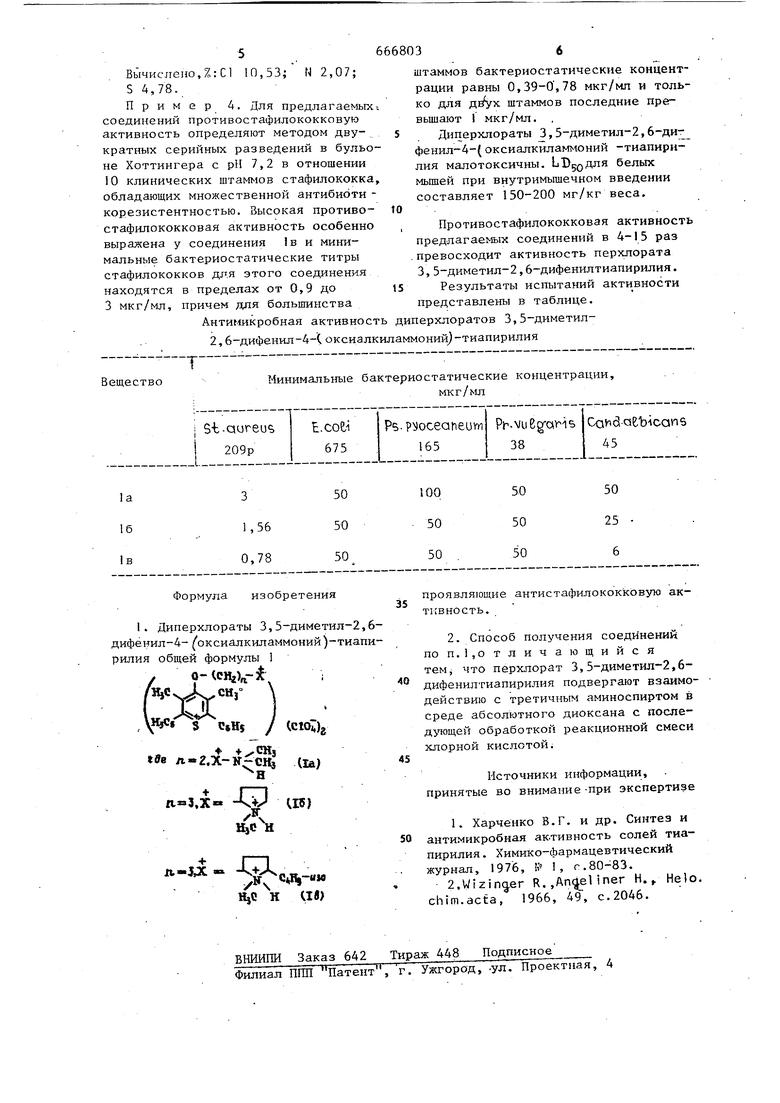
Пример 4. Для предлагаемых-, соединений противостафилококковую активность определяют методом двукратных серийных разведений в бульоне Хоттингера с рН 7,2 в отношении 10 клинических штаммов стафилококка, обладающих множественной антибиоти корезистентностью. Высокая противостафилококковая активность особенно выражена у соединения 1 в и минимальные бактериостатические титры стафилококков дг.я этого соединения находятся в пределах от 0,9 до 3 мкг/мл, причем для большинства
Антимикробная активность диперхлоратов 3,5-диметил2,6-дифенил-4-С оксиалкиламмоний) -тиапирилия Вещество Минимальные
штаммов бактериостатические концентрации равны 0,39-0,78 мкг/мл и только для штаммов последние превьш1ают 1 мкг/мл.
Диперхлораты 3,5-диметил-2,6-дифенш1 4-(оксиалкиламмоний -тиапирилия мапотоксичны. белых мьшей при внутримышечном введении составляет 150-200 мг/кг веса.
Противостафидококковая активность предлагаемых соединений в 4-15 раз .превосходит активность перхлората 3,5-диметил-2,6-дифенилтиапирилия. Результаты испытаний акти вности представлены в таблице. бактериостатические концентрации, мкг/мл

| название | год | авторы | номер документа |
|---|---|---|---|
| Гексахлорстаннаты бис-/(3,5-диметил-2,6-дифенил-4-тиопиранил)-оксиалкиламмония/,проявляющие антистафилококковую активность,и способ их получения | 1977 |
|
SU675817A1 |
| Способ получения тетрафторборатов тиапирилия | 1972 |
|
SU447041A1 |
| Способ получения солей селеназолия | 1977 |
|
SU711036A1 |
| Способ получения солей 4н-5,6-арено1,3-оксазин-4-ония | 1973 |
|
SU504773A1 |
| Соли бензо ( )-2,4-дифенил-5,6-лигидротиахромилия,проявляющие активность против стафилококков и грибов рода кандида | 1976 |
|
SU585683A1 |
| Способ получения производных перхлоратов бис-(пирилиа-,тиаприлиа-или селенопирилиа-)монометинцианинов | 1973 |
|
SU484215A1 |
| Способ получения бромбензилзамещенных солей пирилия или тиапирилия | 1973 |
|
SU469695A1 |
| Способ получения солей селенопирилия | 1991 |
|
SU1816762A1 |
| Способ получения 1,3,4=тиадиазолиевых солей | 1972 |
|
SU445668A1 |
| ПЕРХЛОРАТЫ ДИФЕНИЛЭТОКСИПОЛИМЕТИНЦИАНИНОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1995 |
|
RU2087459C1 |


Авторы
Даты
1982-01-23—Публикация
1977-02-18—Подача