1
Изобретение относится к новым химическим соединениям - азопроизводным б-аминохинолина общей формулы
О--Ч
Rгде R - метил, карбамоил;
R1 - Н, метил, /z-N, N-диметиламиностирил,
п-Ы-этил-Ы-хлорэтиламиностирил;
R2-зтил;
R3 - оксиэтил, цианоэтил;
A- ZnCir, СНзЗОГ, СГ.
Азопроизводные 6-аминохинолина могут быть использованы в качестве катионных красителей для окраски волокон полиакрилонитрильного тина.
Известны соединения на основе 4-аминохинолина 1.
Эти соединения получают диазотированием кватернизованного но азоту гетероциклического кольца 4-аминохинолина и сочетанием с К ,Ы-замен;енными анилинами.
Описаны также производные 2- и 4-аминохннолина, которые получают из 2- и 4-аминохинолина конденсацией с соответствующими
нитрозопроизводными с последующей кватернизацней полученных продуктов 2.
Эти соединения окрашивают полиамидные и цолиакрилонитрильные волокна в голубые и синие цвета.
Целью изобретения является получение новых соединений - азопропзводных 6-аминохинолпна указанной общей формулы, которые могут расширить цветовую гамму катионных красителей.
Это достигается тем, что в качестве исходного продукта для получения новых катионных красителей используют ранее не примемявшийся в этой области 6-аминохинолин или 6-аминохинальдин (2-метил-6-аминохинолин), Последний позволяет в дальнейшем ввести в молекулу стир1 льные заместители.
б-Аминохинолин (хинальдин) диазотируюти вводят в реакцию сочетания с замещенными анилинами с последующей кватернизацией продуктов сочетания.
Ниже приведена общая схема синтеза красителей.
,
сГ
(I)
(1Г)
--N.K ./ V-J R3
Tjl R ;(j
Ш)
:
-иГ
/ Т1
А:
Диазотирование 6-аминохинолина (6-аминохинальдина) (I) проводят в разбавленной соляной кислоте нитритом натрия. Реакция сочетания полученного диазосоединения (II) с N-замещенным анилином идет с хорошим выходом (60-70%) в кислой среде при 10°С. Продукты сочетания (III) выделяют путем подщелачивания реакционной массы раствором воды до рН 8.
Четвертичные производные (IV) получают кватернизацией азосоединений (III) диметилсульфатом или акриламидом в присутствии соляной кислоты при нагревании на кипящей водяной бане. Кватернизацию диметилсульфатом целесообразно проводить в среде органического растворителя (например, в бензоле).
Четвертичные производные, замещенные диалкиламиностирилами, получают конденсацией кватернизованных продуктов азосочетания (IV) с н-диалкиламинобензальдегидами. Введение диалкиламиностирильных заместителей позволяет углубить цвет красителей от оранжевого до красно-фиолетового.
Целевой продукт растворим в воде, спирте, ацетоне, нитрометане, уксусной кислоте.
Пример 1. 1,2-Димeтил-6-(/г-N-этил-Nциaиэтилaминoфeнилaзo) - хинолниийметилсульфат.
А. Диазотирование 6-аминохинальдина.
4,65 г (0,0294 моль) 6-аминохииальдипа растворяют в 29 мл 10%-ной соляной кислоты, охлаждают до 0°С, при перемещивании прикапывают 14,7 мл 2%-ного раствора нитрита натрия в воде. После 20 мин выдержки добавляют 14,7 г хлористого натрия и размещивают реакционную массу до растворения.
Б. Сочетание 6-хинальдиндиазоиия с Nэтил-Ы-цианэтил анилином.
5,5 г (0,0324 моль) Ы-этил-М-цианэтиланнлнпа растворяют в 60 мл 3%-ного раствора
соляпой кислоты, раствор охлаждают до 10°С 1 при перемешивании приливают к нему раствор хннальдиндиазония. После 2 ч размешивания при комнатной температуре реакционпую массу подщелачивают 10%-ным раствором соды до рП 8 и оставляют на ночь. Водный слой декантируют, остаток обрабатывают ацетоном и пропускают ацетоновый раствор через хроматографическую колонку с окисью
алюминия. Собирают первую фракцию (вторая фракция - темная полоса на старте).
После упаривания ацетона остается кристаллический продукт в количестве 6,95 г (70%); т. пл. 135-137° С (водный ацетон).
В. Кватернизация 1-метил-6-(/г-М-этил-Мцианэтиламииофенилазо) -хинолина диметилсульфатом.
1,6 г (0,00466 моль) 1-метил-6-(л-М-этил-Мцианэтиламинофеиилазо) -хинолина растворяют в 100 мл бензола, прикапывают при перемещиваиии 0,88 мл (0,0093 моль) диметилсульфата и нагревают реакционную массу на кипящей водяной бане в течение 3 ч. Продукт реакции выделяют в виде темного вязкого
масла, которое отделяют от растворителя, тщательно отмывают бензолом, а затем эфиром от пепрореагировавщего исходного красителя, сушат при 60° С.
После высушивапия получают целевой продукт в количестве 2,07 г (94%); т. пл. 163- 166° С (ацетон-;-эфир).
Пример 2. 1,2-Диметил-6-(л-К-этил-Ыоксоэтиламинофепилазо) - хииолинийхролцинкат.
Диазотироваиие, сочетание и кватернизацию азопродукта проводят, как в примере 1, однако целевой продукт не удается выделить I кристаллическом виде с анионом СПз5О4,
ПОЭТОМ} его получают с аниоиом-ZnCU
по следующей методике.
1,9 г 1,2-диметил-6-(/г-N-этил-N-oкcиэтиламинофенилазо) - хинолинийметилсульфата растворяют в 20 мл воды, добавляют 5 г хлористого натрия и но каплям 2,8 мл 70%-ного раствора хлористого цинка. Выделившийся осадок отфильтровывают, промывают 10%пым раствором хлористого патрия до нейтральной среды и сущат при 60° С.
Выход целевого иродукта 1,82 г (80%,), т. пл. 215-217° С (из ацетона + эфир).
Пример 3. 1-метил-2-(я-Ы, N-диметиламиностирил)-6-(л-Ы-этил-Н - цианэтиламинофеиплазо) -хинолипийметилсульфат.
0,5 г (0,00107 моль) 1,2-диметил-6-(л-Ыэтил-Ы-цианэтиламинофенилазо) - хинолинийметилсульфата растворяют в 15 мл уксусного ангидрида, добавляют 0,17 г (0,00107 моль) w-диметиламинобепзальдегида и кипятят реакционную массу 2 ч. После охлаждения конечный продукт осаждают из раствора эфиром, отфильтровывают, иесколько раз промывают эфиром на воронке и сушат.
Получают 0,48 г (75%) целевого продукта;
т. пл. 148-150° С. Пример 4. 1-Карбамоил-6-(/г-М-этил- цианэтиламинофенилазо) - хинолинийхлорпд. A.Диазотирование 6-ампнохпнолмна. 1 г (0,00695 моль) 6-амкнохинолика растворяют в 4 мл разбавленной (1:1) соляной кислоты, охлаждают до 0°С, при перемешивании прикапывают раствор 0,48 г (0,00695 моль) нитрита натрия и перемешивают реакциоинхю массу при 0° С 20 MHii. Б, Сочетание 6-диазохинолпиа с Х-этил-Nцианэтила1 илином. Реакцию сочетания и выделение продукта ироводят, как в примере 1. Выход целевого продукта составляет 50%; т. ил. 110-113°С (из водного этанола). B.Кватернизацпя 6-(п-Ы-этил-К-цианэтиламинофенилазо) -хинолина акриламидом. 0,83 г (0,00252 моль) 6-(/г-Ы-этил-Ы-цнаизтиламинофенилазо)-хинолина растворяют в 10 мл уксусной кислоты, добавляют 0,179 г (0,00252 моль) акриламида и 0,25 мл концентрированной соляной кислоты и греют реакционную смесь на кипящей водяной бане 2ч, после чего оставляют на ночь при комнатной температуре. Растворитель упаривают, остаток обрабатывают эфиром и сушат. Получают 0,75 г (67%) целевого продукта; т, пл,187-188 С (нз этанола). Полученные соединения (IV) окрашивают нолиакрилоннтрильное волокно в интенсивные оранжевые и красно-фиолетовые цвета из водных красильных ванн с рН 3-4 и ирактическн полностью выбираются волокном, Выкраскн на волокне имеют хорошую светоирочность, прочность к мокрой обработке н треиню устойчивы к нагреванию и действию органических растворителей. Новые катионные красители сравиимы по колористическим свойствам с известными отечественными кpacитeля ти тех же цветов: катионным оранжевым Ж, катионным желтокоричневым, катионным оранжевым 4К, катионным красно-фиолетовым, но значительно интенсивнее окрашивают полиакрилонитрильное волокно при одинаковой концентрации красителя в красильной ванне. Так, для получения стандартного тона достаточна концентрация красителя 0,5-0,8%, Данные колористических нспытаипй некоторых красителей па основе азопроизводных 6-аминохинолина (3%-ные выкраски на волокне) приведены в табл. 1, Т а б ,1 и ц а 1
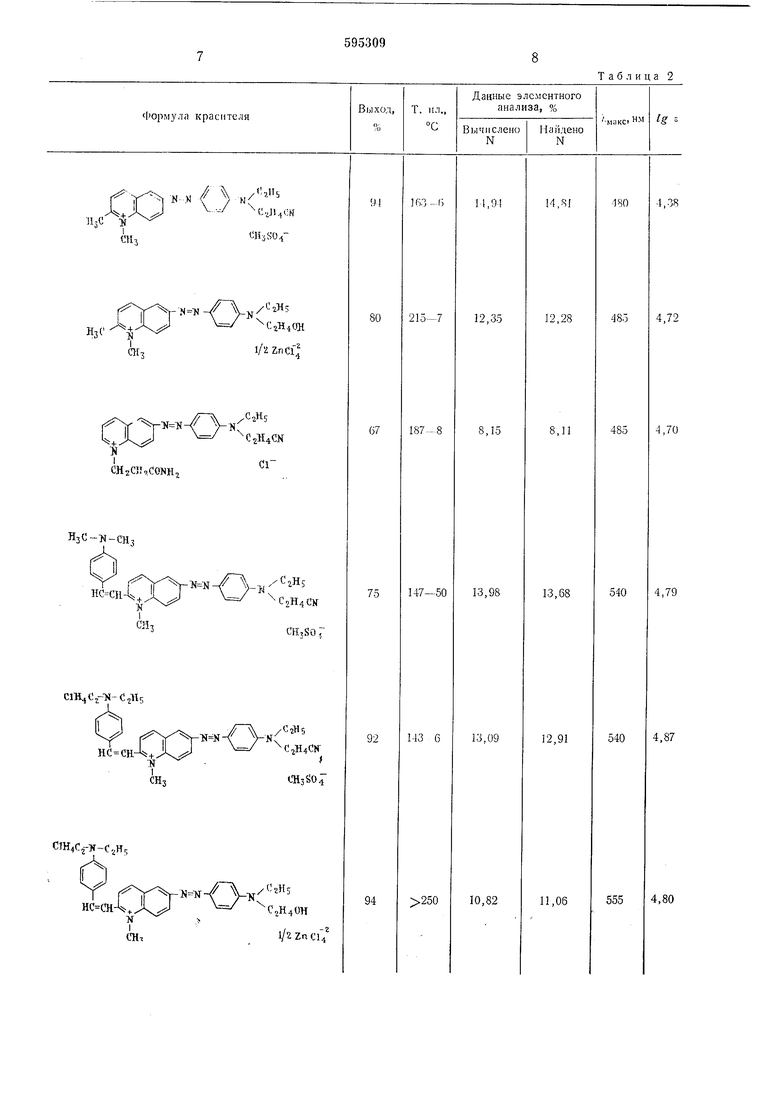
Таблица 2 9 Характеристики полученных кра представлены в табл. 2. Формула изобретения Азопроизводные 6-аминохинолина формулы
V./«
Г
А
где R - метил, карбамоил;
R - Н, метил, rt-N, N-диметиламиностирил, 15
д-М-этил-М-хлорэтиламиностирил;
Источники информации, принятые во внимание при экспертизе
1.Патент Франции № 1462723, кл. С 09В 29/22, опубл. 1967.
2.Патент Франции № 1198997, кл. С 09В 29/22, опубл. 1959.
3.Катионные красители. М., «Химия. 1971, с. 435. 595309 - этил; ителей R -оксиэтил, цианэтил; А - - ZnCir, CH,sor, cr общей катионных краситенроявляющие свойства лей.





Авторы
Даты
1978-02-28—Публикация
1975-12-19—Подача