где ш и W имеют вышеуказанные значения, или с проиэврдньм амина, полученным в результате реакции его с хлоридом фосфора, в среде растворителя при температуре от до температуры кипения.
Приме р. 1. Солянокислый Н -(1-бен зилпирролидинилт 2-метил)-2-метокси-5-этилсульфонилбензамид.
Вре.актор емкостью 6 л, снабженный механической тУ1еша кой и термометром, загружают 2160 мл метилэтилкетона, 400 г N -бензил-2-аминометилпирролидина и 540 г 2-метокси 5-з.тилсульфонилбензоилхлорида, поддерживая температуру 15-20 с, и перемешивают 3 ч при комнатной температуре, отфильтровывают кристаллы, промывают небольшим количеством ледяного метилэтилкетона и сушат-при; 50 с. Получают 850 г вещества, которые растворяют в 4250 мл 95%-ного изопропанола, фильтруют, охлаждают, отделяют кристаллы, промывают и сушат. Получают 700 г (75,5%) целевого соединения, т.пл. .
Пример 2. Солянокислый N -( бензилпирролидинил-2-метил)-2-1 етокси -5-метилсульфонилбензамид.
В реактор емкостью Ю л, снабженный механической мешалкой и термометром, загружают 3 л метилэтио 1кетона и 431 г N -бенэил-2-амиНометилпирролидина, ПОТОМ-прибавляют 555 г 2-метокси-5-метилсульфонилбенэоилхлорида, поддерживая теипературу-15 20 €, перемешивают 2 ч при комнатной температуре, отфильтровывают осадок, обрабаты-вают ледяным метилэтилкетоном, сушат при 50с и получают 335 г. вещества.
Для очистки это вещество переводят в основание при обработке водным раствором аммиака, а затем подкисляют основание, растворенное в 3л этанола, солянокислым этанолом. Образовавшуюся соль отфильтровывают, промьавают ледяным этанолом и сушат при 50 С, Выход 825 г (84,3%), т.пл. 153-156 С.
П р и м е р J 3. Фосфат N -(1-бензи -пирролидинил-2-метил)-2-метокси-1-амино-5-сульфамоилбензс1мида.
В колбу емкостью 4 л, снабженную механической мешалкой, термометром и обратным холодильником, загружают 500 г метилового эфира 2-метокси-4-амино-5-сульфамоилбензойной кислоты, 510 мл воды и 547 г 1 -бензил-2-аминометилпирролидина, нагревают 2.0 ч при 90-95°С. Твердое вещество, выг павшее в осадок после охлаждения, три раза экстрагируют 700 мл метиленхлорида. Экстракты объединяют, промывают водой, сушат над сульфатом магния и выпаривают в вакууме 450 г полученного продукта растворяют при, кипении в 1350 мл водыи прибавляют туда 250 мл 85%-ной фосфорной кислоты (рН 1). Кристаллы, образовавшиеся.
при охлаждении, растворяют в 1350 мл кипящей воды, потом прибавляют 40 г активированного угля. После горячего фильтрования и охлаждения полученного раствора образовавшиеся кристаллы отфильтровывают, промьшают водой и сушат в сушильном шкафу при . Получают 380 г фосфата N -(1-бензилпирролидинил-2-метил)-2-метокси-4-амино-5-сульфамоилбензамида, i т.пл. 184-18бс.
4.N - (1 -Бензилпирролидинил-2-метил) -2-метокси-4-амино-5-хлорбензамид.
В реактор емкостью б л, снабженный механической мешалкой, iобратным холодильником, термометром и трубкой для подвода газа, заливают 515 г метилового эфира 2-метокси-4-ацетамидо-5-хлорбензойной кислоты/i100 мл этиленгликоля и при перемешивании 1140 г N -бензил-2-аминометилпирролидина. Смесь 2 ч нагревают в атмосфере аргона при 120с и после охлаждения до 100°С прибавляют 500 мл 2,5 н. едкого натра, предварительно нагретого до 95-itfO C. Смесь кипятят с обратным холодильником в течение 30 мин. После добавления 1 л воды смесь охлаждают до . Органический слой декантируют и растворяют в 800 мл метиленхлорида, который использовали для -экстрагирования водной фазы, сушат над сульфатом магния, упаривают в вакууме, перекристаллизовывают остаток из ацетона, сушат в сушильном шкафу при и получают 35Ь г (47%) продукта, т.пл. 142-144с. И р и м -ё р 5. Солянокислый N (-бензилпирролидинйл-2-метил)-2-метокси-5-этилсульфонилбензамид.
В реактор, снабженный мешалкой и . холодильником, загружают 7,3 г 2-метокси-5-этилсульфонилбензойной кислоты, 200 мл тетрагидрофурана и 7,3 г карбонилдиимидозола. После перемешивания смеси при комнатной температуре в течение 30 мин прибавляют 9,2 rN -бензил-2-аминометилпирролидина, перемешивают при комнатной температуре и растворитель упаривают в вакууме.
Остаток растворяют в соляной кислоте, фильтруют, обрабатывают фильтрат едким натром до рН 12-13, экстрагируют хлороформом, экстракт сушат, фильтруют и упаривают в вакууме.
Полученный бензамид растворяют в этаноле, обрабатывают солянокислым этанолом, фильтруют, промывают, сушат и получают 8,55 г (63%) целевого вещества, т.пл. 170с.
Пример 6. N -(1-Бензилпирролидинил-2-метил)-2-метокси-4-амино-5-метилсульфамоилбензамид.
В реактор емкостью 8 л, снабженный мешалкой, термометром, капельной воронкой, загружают 220 г 2-матокси-4-амино-5-метилсуфамоилбензойнойкислоты, 217 мл воды и 85,5 г триэти амина, нагревают до до растворения, приливают 520 мл ацетона, охлаждают до и по каплям при добавляют 92 г этилхлорформиата. Смесь перемешивают 1,5 ч при , прибавляют 92 г 2-бенэил-2-аминометилпирролидина и после повышения температуры до комнатной перемешиваю еще 2 ч. Затем отгоняют ацетон, обрабатывают остаток 2 л воды и подщелачивают смесь 15 мл 20%-ного водного раствора аммиака. К выделившемуся основанию добавляют 85%-ную фосфорну кислоту и переосаждают основание путем обработки образовавшегося фосфата 20%-ным водным раствором аммиака. Выход 228 г (62%), т.пл. 88-92с.
Пример 7. Солянокислый N -(1-бензилпирролидинил-2-метил) -2,3-диметокси-5-сульфаМоилбензамид.
В реактор емкостью 4 л, снабженный механической мешалкой и термометром, загружают 1 л ацетона и 200 rN -бензил-2-ё1минометилпирролидина, охлаждают до и прибавляют 280 г 2,3-дметокс и-5-сулкфамоилбензоилхлорида, поддерживая температуру реакционной среды ниже . Смесь перемешивают еще 4 ч, отфильтровывают осадок,промывают на фильтре, сушат при 50С, растворяют при кипении в .600 мл диметилформамида, фильтруют, охлаждают отделяю кристаллы, промывают их, сушат при и получают 190 г (38,5%) целевого продукта, т.пл. 208209 С. . : . ,
Пример 8. N -(l-Бeнзилпиppoлидинил-2-мeтил) -2,З-диметокси-5-метилсульфамоилбензамид.
В реактор емкостью 2 л загружают 500 г этиленгликоля, в котором растворено 124 г метипового эфира 2,3-диметокси-5-метилсульфамоил6ензойной кислоты, при 50С. Прибавляют 98 г 1-бензил-2-аминометилпирролидина и полученный раствор выдерживают при 50°С до тех пор, пока проба не будет полностью растворима в разбавленных кислотах. После разбавления реакционной среды 2 л воды и последующего подкисления 70 мл концентрированной соляной кислоты раствор обрабатывают активированным углем и фильтруют. Основание осаждают 20%-ным раствором аммиака.
Твердый продукт, образовавшийся после Добавления небольшого количества эфира, отфильтровывают, промывают водой, сушат и перекристаллизовывают из абсолютного этанола. Выход 127 г (84,5%), т.пл. 121-122с./
Приме р 9. W - (1-Вензилпирролидинил-2-метил)-2-метокси-5-метил-сульфамоилбензамид.
В реактор емкостью 1 л, снабженный холодильником, загружают 238 г этилового эфира 2-метокси-5-метилсульфа|Моилбензойной кислоты, 78,5 г воды 5 и 198 г 1-бензил-2-амннометилпирролидина. Полученную суспензию нагревают при 90с до .тех пор, пока проба не будет полностью растворима в разбавленных кислотах. Затем смесь
10 обрабатывают 1550 мл воды и подкисляют концентрированной соляной кислотой. Полученный раствор обрабатывают активированным углем, фильтруют и подщелачивают 20%-ным водным растворо
15 аммиака. Твердый продукт, образующийся при добавлении небольшого количества эфира, Отфильтровывают, промыIвают водой, сушат при 45 С, перекрис:таллизовывают из кипящего абсолютного
20 спирта и получают 211 г (58,5%) целевого вещества, т.пл. 117-118,.
П р и м е р 10. N - (l-Eeнзилпиppoлtидинил-2-мeтил) -2-метокси-4-амиио25 -5-хлорбензамид.
Раствор 1,4 г треххлористого фосфора в 8 мл пиридина прибавляют по кап:лям при перемешивании, поддерживая температуру 0-5°С, к -раствору 3,5 г ;1-бензил-2-аминометилпирролидина в iпиридине. Продолжают перемешивание при 0-5с, потом при комнатной температуре .
35 После добавления 2 г 2-метокси, -4-амино-5-хлорбензойной кислоты к ;полученному раствору смесь нагревают при перемешивании в течение нескольких часов, охлаждают, удаляют раст 0 воритель, растворяют остаток в хлороформе, обрабатывают раствор водным раствором карбоната натри сушат над безводным сульфатом магния, концентрируют в вакууме и перекристал лизовывают остаток из ацетона. Получают 2,2 г (59,3%) целевого продукта, т.пл. 142-144с.
Пример 1. Солянокислый N -(1-бензил-2 пирролидинилметил)-2-метокси-5-сульфамоилбензамид,
В реактор емкостью 4 л.вводят 571 г этилового эфира 2-метокси-5-сульфамоилибензойной кислоты и 1320 г гликоля. Повышают температуру смеси до 70°С, прибавляют 420 г N -бензил-2-аминометилпирролидина, выдерживают 4 ч при 120°С, охлаждают, суспендируют в воде, отфильтровывают осадок, обрабатывают раствором 300 мл 36%-ной соляной кислоты в 5 л воды, перемешивают 2 ч, отфильтровывают осадок, промывают водой, сушат в сушильном шкафу при 50с и получают 900 г целевого продукта (93%), т.пл. 232- 235°С.
Формула изобретения
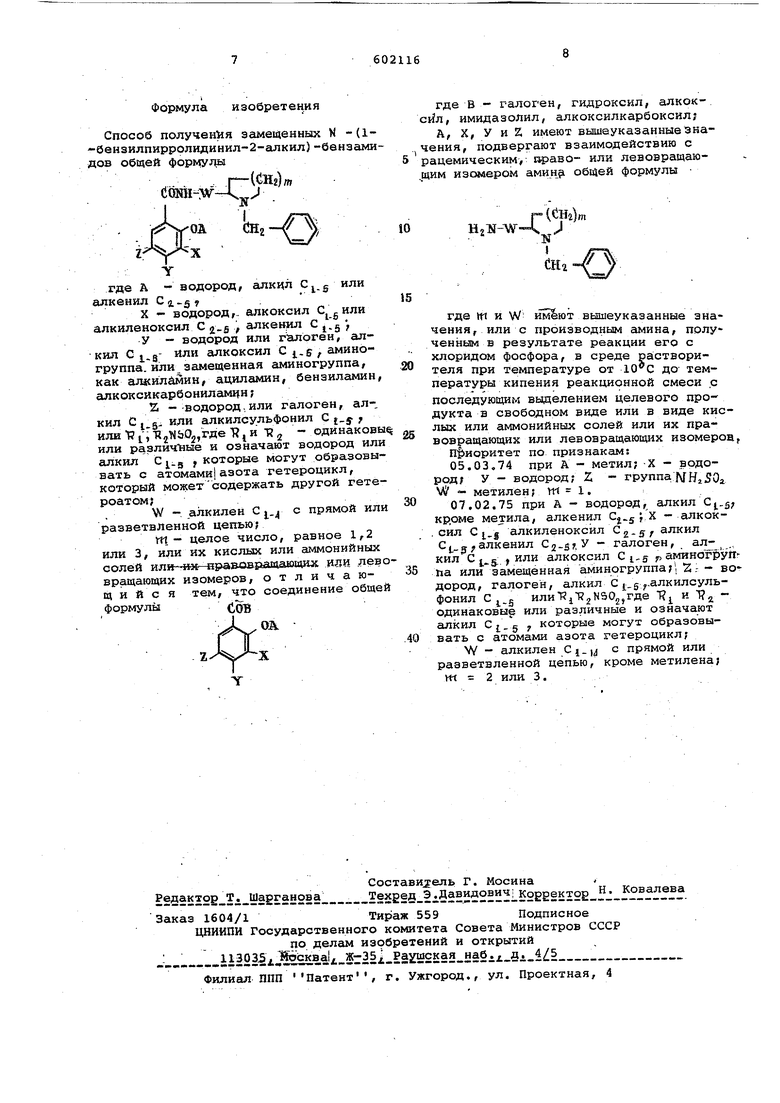
Способ получения замещенных N -(1-бензилпирролидинил-2-алкил)-бензамиfiOB общей фopмyJ
иНг)
CttNJW-Сх
где А - водород, алкил C.g или алкенил С ц.д у
К - водород,, апкоксил алкиленоксил С j.g алкенил С .g ,
У - водород или галоген, алкил С j.g- или алкоксил С j.-e , аминогруппа, или замещенная аминогруппа, как аякилййин, ациламин, бензиламин, алкоксикарбониле1мчн;
2 - -водород, или галоген, ал-, кил С I д, иди алкилсульФонил С j.j. , или 1 Т12«Ь02,где Т и Т 2 одинаковы или различТные и означают водород или алкнл , которые могут образовывать с атомами азота гетероцикл, который можетсодержать другой гетероатом;
V/ -. алкилен С , с прямой или разветвленной цепью;
Ш - целое число, равное 1,2 или 3, или их кислых или аммонийных солей ил -и«-нравовращающах или левовращающих изомеров, отличающийся тем, что соединение общей формулы СЪъ
.ож
где в - галоген, гидроксил, алкоксйл, имидазолил, алкоксилкарбоксил;
А, X, У и Z имеют вшивуказанныезна.чения, подвергают взаимодействию с 5 рацемическим, право- или леаоэращаю,щим изомером аминр об14ей формулы
, -«--Вг г. HjTS-W- k.
10
Uis
где m и W вышеуказанные значения, или с производным амина, полученным в результате реакции его с хлоридом фосфора, в среде раствори0теля при температуре от до температуры кипения реакцисзнной смеси с последующим выделением целевого продукта в свободном виде или в виде кислых или аммонийных солей или их пра5вовращающих или левовращающих изомеров,
приоритет по признакам:
05.03.74при А - метил;-Х - водород; У - водород; Z - группа KfHzSOi W «- метилен; W 1.
0
07.02.75при А - водород, алкил Cj.; кроме метила, алкенил C.j ;,х - алкок. сил С j.g алкиленоксил С 2-5 f злкил Cj g алкенил С2-5, У - галоген, алкил С j, , или алкоксил С - аминогруЛ5ha или замещенная аминогруппа;, %.- - водород, галоген, алкил С .д.алкилсульфонил С g илиRJR2N502,гдe Я и T,j одинаковы или различные и означают алкил , которые могут образовы0вать с атомами азота гетеродикл;
W - алкилен Cj.) с прямой или разветвленной цепью, кроме метилена; ш 2 или 3.




Авторы
Даты
1978-04-05—Публикация
1975-03-04—Подача