(54) СПОСОБ ПОЛУЧЕНИЯ АНАЛОГА ПЬХЮТАГЛЛИДИИА

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных простагландина | 1977 |
|
SU676162A3 |
| Способ получения производных 11-дезоксипростагландина | 1973 |
|
SU655308A3 |
| Способ получения 2-/6-карбметокси (этокси)-гексил/-циклопентен2-она-1 | 1978 |
|
SU789510A1 |
| Способ получения производных 3-карболкокси1-тиа-изохроман-1,1-диоксидов | 1970 |
|
SU493960A3 |
| Способ получения производных октагидрооксазоло (3,2-а) пирроло (2,1-с) пиразина | 1974 |
|
SU593664A3 |
| Способ получения трициклических соединений или их солей | 1975 |
|
SU591146A3 |
| Способ получения замещенных 2-винилхромонов или их солей | 1978 |
|
SU938743A3 |
| Способ получения производных аминопиррола или его солей | 1974 |
|
SU843738A3 |
| Способ получения 2-циклопропилхромонов или их солей | 1978 |
|
SU995706A3 |
| Способ получения аминоспиртов или их солей | 1970 |
|
SU578860A3 |

I
Иэобрегенне относится к способу получения не описанного в литературе аналога простаглаидина формулы
Предлагаемый способ получения aiianoi-,i простагландина заключается в rovf, что (;лс жный эфир обшей формулы 1
СООН
соон
10
он
обладающего фармакологической активностью.
Известен способ получения карбоновых кислот с помощью щелочного гидролиза сложных эфиров ij.
Использование известной реакции позволяет получать новое производное простаглаи-20 диИа, проявляющее фармакологическую активность.
иель изобретения - расщиреиие ассортимеита биологически активных соедииеинй. 25
в которой и представляет собой линейшлй или разветвленный алкнльиый радикпл, содержащий 1-7 атомов углерода, пооверглюг взаимодействию с гидроокисью щелочно1Х металла в спиртовой среде при комнатной температуре с последующей обработкой сил ной кислотой.
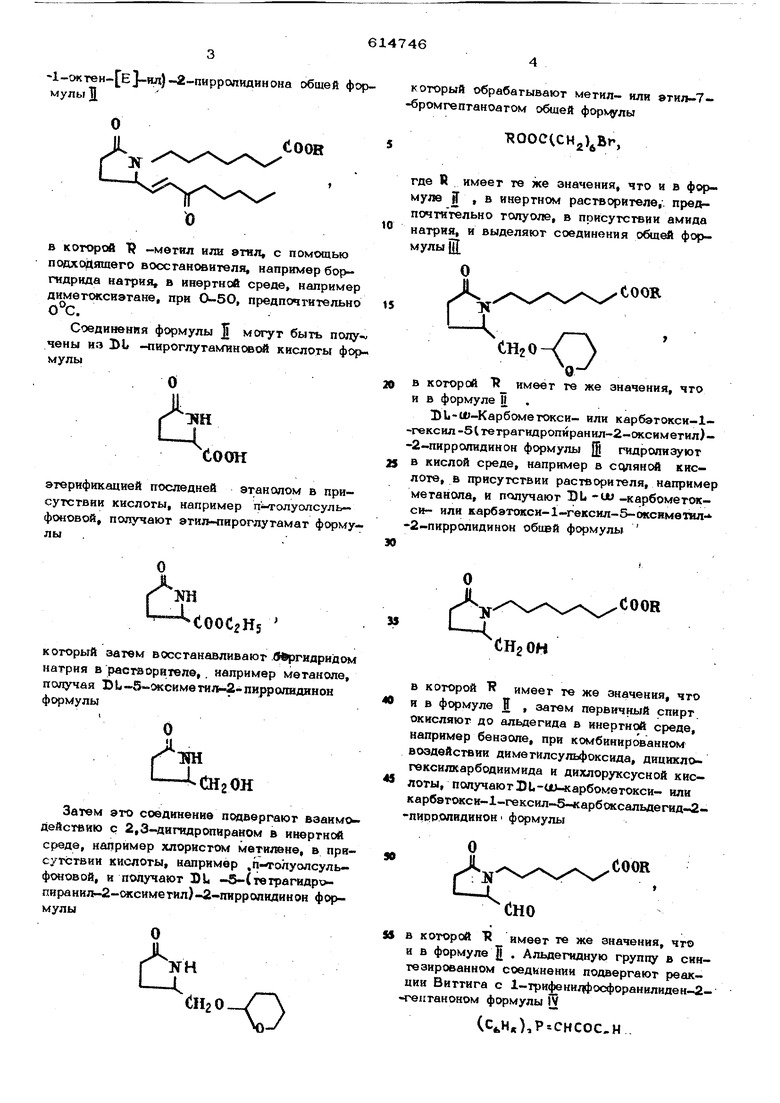
Соединения формулы Т, в которой Tt п|х.лставляет ообой метил нли этил, могут быть получены восстанхжлением 3)L - uu-карбометокси- или карбэтокси-1-гексип-5-(3-(Ж(:о-1-октен- Еj-Bin)-2-пирролидинона обшей формулы Д
ClOOR
R которой Т -метил или атнл, с помощью подходящего восстановителя, например бо(гидрида натрия, в инертной среде, например диметокснэтане, при , предпочтительно 0°С.
Соединения могут быть получены из DI -пироглутаминовЫ кислоты ф( мулы
(J
7«Н
Соон
этерификацией последней этанолом в присутствии кислоты, например п олуолсуль- фоювой, получают этил-пироглутамат формулы
О
NH
ид.
который затем восстанавливают б гидрндом натрия в растворвтело,. например метаноле, получая (жсиметил-2-пирропидинон формулы
Iо
тш
i-L
СНгОН
Затем это соединение подвергают взаимо Действию с 2,3-дигндрс«тираном в инертной среде, например хлористом метилене, в присутствии кислоты, например ,п- олуолсуль- фоновой, и получают DU -5-(гвтрагидр пиранил-2-сжсиметил)-2-пирролидинон формулы
О
IX
«„о
который обрабатывают метил- или 9тил-7-бромгептаноатом обшей
)4Вг,
где R имеет те же значения, что и в формуле JT , в инертном растворителе,, предпочтительно толуоле, в присутствии амида натрия, и выделяют соединения общей формулы jj
СООЕ
СИ, о-/Л
Ов которой т имеет те же значения, что и в формуле Н .
3)Ь-и;-Карбометокси- или карбэтокси-1-гексил-51 тетрагндропйранил-2-сжсиметил)- -2-пирролидинон формулы Ц гидропиауют в кислой среде, например в сс пяной кислоте, в присутствии растворителя, например метанола, и получают I)L -ч -карбометокси- или карбэтокси-i-гексил-б-оксиметил- -2-пирролидинон обивй формуль
эо
С ООН
35
СНгОн
в которой т имеет те же значения, что и в формуле Я , затем первичный спирт, окисляют до альдегида в инертной среде, например бензоле, при комбинированном воздействии диметилсульфоксида, дициклогексилкарбодиимида и дихлоруксусной кисSлоты, получаю т Ли-Ш-карбометокси- или карбэтокси-1-гексил-5-«арбоксальдегид-2-пирролидинон формулы
COOR
Сно
5Л В которой т имеет те же значения, что и в формуле Д . Альдегидную группу в синтезированном соединении подвергают реакции Виттига с 1-трифени/|фосфоранилиден-2-геитаноном формулы IV
(CfcH«),P CHCOC,H . с тем, чтобы получить соответственно DL-Ш -карбом«гокси- или карбэтоксн-1-гексил- -5-(3-oкco-l-oктeн- EJ-ил)-2-пирролидинон формулы И . Метил- или этил-7-бромгептаноат можно получить из пробковой кислоты (октаидиоеой кислоты), которую переводят в ме тилсжый или этиловый моноэфир, затем обр батывают эфир нитратом серебра, получают метил- или этилсуберат серебра и о рабатывают соль бромом в инертной среде, например четыреххлористом углероде. Фосфорсодержащее соединение формулы W может быть получено из дипентилкадмия (получают из пентилмагнийбромида и хлористого кадмия) и монохлорацетилхлорида. Полученный 1-хлор-2-гептан он обрабатывают трифенилфосфином, образующийся трифенил-2-оксогептилфосфорийхлорид формулы (t6H5)3PCH2 ioC5HiiCr с помощью водного раствора поташа перево дят в соединение формулы IV . Другие сложные эфиры формулы I могут быть получены по методике, приведенной выше для приготовления метилгжых и этиловых эфир ОБ формулы I . Пример. ПолученнеЭи - UU- арбсжси-1-гексил-5(З-окси-1-октек )-2-пирролидинона или DL -8-аза-11-деокси-ПГЕ . В круглодонную трехгорлую колбу емкс стью 250 мл, снабженную кеханической мешалкой, валивают 1ОО мл метанола и 2,6 г Dl,-u -кapбoмeтoкcи-l-гeкcил-5-lЗrOкcи-l-oктeн- E -ил)-2-пиppoлидинoнa. Образовавшийся раствор охлаяаают на бане с ледянсй водой до О С, затем медленно пр ливают 40 мл 0,5 н. раствора едкого натра оставляют на 2,5 ч при комнатной температуре, добавляют 20 мл воды, полученный водный раствор промывают 25%-ным раство ром солянсй кислоты до рН 2 и несколько раз экстрагируют этилацетатом. Органические фазы соединяют, промывают насыщенным раствором хлористого натрия, сушат и удаляют растворитель, Пол чают 2,1 г Ш5%) целевого соединения в виде частично o.iкристаллизсдаавшегося гигроскопичного ix-nii. Хроматография в тонком слое силика1х ли с применением смеси бензол-аиоксап-уксусная кислота (90:25:4) дает основное пятно Т f 0,3 и два пятна с Я О,39 и 1 соотетственно. ИК-спектр 1хлороформ), см , 1710 1С-0), 1665 (CO-N). Формула изобретений 1. Способ получения аналога простагланина формулы отличающийся тем, что сложный эфир обшвй формулы В которой т представляет линейный или разветвленный алкильный радикал, содержащий 1-7 атомов углерода, подвергают взаимодействию с гидроокисью щелочного металла в спиртовой среде при комнатной температуре с последующей обработкой сильней . кислотой, после чего целевой продукт выделяют. Источники информйции, принятые во внимание при жсспертизе: 1. Вайганд-Хельгетаг.Методы эксперимента в органической химии, М., Химия;, с. 366, 1968.
Авторы
Даты
1978-07-05—Публикация
1976-03-19—Подача